1 . 氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为________ 个。
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为________ 。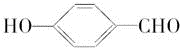 的沸点比
的沸点比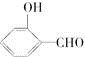 高,原因是
高,原因是__________________________ 。
(3)H+可与H2O形成H3O+,H3O+中O原子采用________ 杂化。H3O+中H—O—H键角比H2O中H—O—H键角大,原因为_____________________________________ 。
(1)氧元素基态原子核外未成对电子数为
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为
 的沸点比
的沸点比 高,原因是
高,原因是(3)H+可与H2O形成H3O+,H3O+中O原子采用
您最近一年使用:0次
名校
2 . 已知A、B、C、D、E、F是周期表前四周期的元素,原子序数依次增大。A的基态原子2p能级上有2个单电子;C是地壳中含量最多的元素;E的单质常温常压下为黄绿色气体,化学性质十分活泼,具有毒性;F位于ds区,最外能层有单电子,是热和电最佳导体之一;D与F不同周期,但最外能层电子数相等。
(1)写出基态C原子的电子排布式:____________ 。
(2)A、B、C三种元素第一电离能最大的是____________ 。(用元素符号表示),其原因是____________ 。
(3)B、C两元素形成的化合物B2C的分子空间构型为____________ 。与B2C互为等电子体的粒子的化学式为____________ 。(填一种)。
(4)D、E形成的一种离子化合物,在晶胞结构图中黑球表示E的位置,白球表示D的位置,已知该晶胞的边长为ncm,阿伏伽德罗常数为NA,求晶胞的密度ρ=_______ g/cm3(用含n、NA的计算式表示)。
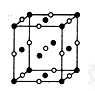
(5)由F原子形成的晶胞结构如图,F原子的半径为r,列式表示F原子在晶胞中的空间利用率:__________________ (不要求计算结果)。

(1)写出基态C原子的电子排布式:
(2)A、B、C三种元素第一电离能最大的是
(3)B、C两元素形成的化合物B2C的分子空间构型为
(4)D、E形成的一种离子化合物,在晶胞结构图中黑球表示E的位置,白球表示D的位置,已知该晶胞的边长为ncm,阿伏伽德罗常数为NA,求晶胞的密度ρ=

(5)由F原子形成的晶胞结构如图,F原子的半径为r,列式表示F原子在晶胞中的空间利用率:

您最近一年使用:0次
3 . 【化学选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大,其中非金属元素A的基态原子中成对电子数是未成时电子数的两倍,C元素在地壳中含量最高,D的单质是短周期中熔点最低的金属,E的合金是我国使用最早的合金。
(1)E元素的基态原子电子排布式为__________________ 。
(2)A的某种氢化物A2H2分子中含有___ 个σ键和____ 个π键。
(3)A 的含氧酸根离子AO3n-的空间构型是___________ 。
(4)B的最简单的氢化物的沸点比A 的最简单的氢化物的沸点高得多,其原因是_____ 。
(5)E的最高价氧化物对应的水化物溶解于氨水中生成的复杂化合物的化学式是______ 。
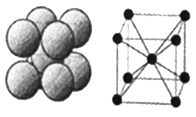
(6)下图是D单质的晶体堆积方式,这种堆积方式的晶胞中原子的配位数为____ ,若该原子的半径为rpm ,此晶体的密度ρ=______ g/cm3(用含r的代数式表示,阿伏伽德罗常数用NA表示)。
(1)E元素的基态原子电子排布式为
(2)A的某种氢化物A2H2分子中含有
(3)A 的含氧酸根离子AO3n-的空间构型是
(4)B的最简单的氢化物的沸点比A 的最简单的氢化物的沸点高得多,其原因是
(5)E的最高价氧化物对应的水化物溶解于氨水中生成的复杂化合物的化学式是
(6)下图是D单质的晶体堆积方式,这种堆积方式的晶胞中原子的配位数为

您最近一年使用:0次
2017-02-24更新
|
855次组卷
|
4卷引用:云南省红河州弥勒市中小学2018-2019学年高二下学期期末考试化学试题



