名校
解题方法
1 . 现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素.请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有____ 个方向,原子轨道呈__________ 形,C简单离子核外有______ 种运动状态不同的电子.
(2) 难溶于
难溶于 ,简要说明理由:
,简要说明理由:________________ .
(3) 分子的空间构型为
分子的空间构型为__________ ,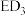 分子的
分子的 模型名称为
模型名称为__________ .
(4)下列气态分子 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为_______________ .
| 元素 | 相关信息 |
| A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 原子核外p电子数与s电子数相等 |
| C | 基态原子的价电子排布为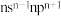 |
| D | 能层数与C相同,且电负性比C大 |
| E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)
 难溶于
难溶于 ,简要说明理由:
,简要说明理由:(3)
 分子的空间构型为
分子的空间构型为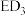 分子的
分子的 模型名称为
模型名称为(4)下列气态分子
 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为
您最近一年使用:0次
名校
2 . 按要求回答下列问题:
(1)请将下列几组物质的编号填写在空格上:①D与T ②金刚石与C60 ③CH2=CHCH3和CH2=CH2④CH4和CH3CH2CH3 ⑤CH3CH2CH(CH3)2和CH3(CH2)3CH3 ⑥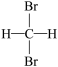 和
和 。互为同位素的是
。互为同位素的是_______ ;互为同系物的是_______ ;互为同分异构体的是_______ 。
前四周期元素A、B、M、D、E原子序数依次增大,其相关性质如表所示:
请根据以上情况,回答下列问题:
(2)A元素在周期表中的位置为____________ ,位于元素周期表的____ 区,其最高价氧化物对应水化物的阴离子的空间构型为____________ 。
(3)D的基态原子的电子占据的最高能层符号为____ ,最高能级的电子云形状为____________ 。
(4)ABD三种元素第一电离能由小到大的顺序为________________ (用元素符号表示)。BMD三种元素的简单离子的半径由大到小的顺序为________________ (用离子符号表示)。
(5)A和B形成的简单氢化物中,键角较大的是________ (填化学式),原因是________________ 。
(6)E的基态原子核外有____ 种运动状态不同的电子,该原子的简化电子排布式为_________________ 。
(1)请将下列几组物质的编号填写在空格上:①D与T ②金刚石与C60 ③CH2=CHCH3和CH2=CH2④CH4和CH3CH2CH3 ⑤CH3CH2CH(CH3)2和CH3(CH2)3CH3 ⑥
 和
和 。互为同位素的是
。互为同位素的是前四周期元素A、B、M、D、E原子序数依次增大,其相关性质如表所示:
| A | 2p能级电子半充满 |
| B | 与A同周期,且原子核外有2个未成对电子 |
| M | 前三周期元素中,M元素电负性最小 |
| D | 其基态原子的价层电子排布式为nsn-1npn+1 |
| E | 前四周期元素中,E元素基态原子未成对电子数最多 |
(2)A元素在周期表中的位置为
(3)D的基态原子的电子占据的最高能层符号为
(4)ABD三种元素第一电离能由小到大的顺序为
(5)A和B形成的简单氢化物中,键角较大的是
(6)E的基态原子核外有
您最近一年使用:0次
解题方法
3 . 下图为元素周期表的部分,元素①~⑥在表中的位置如图所示。

用化学用语 回答下列问题:
(1)⑥的元素符号为_______ ,元素⑤的基态原子核外共有_______ 个单电子。
(2)元素③、④的简单氢化物中,稳定性较高的是_______ ,原因是_______ 。
(3)元素①与元素②、③均能形成 分子,其中与②形成的
分子,其中与②形成的 分子的结构式为
分子的结构式为_______ ,一定条件下两种 分子能发生反应,产物无污染,写出该反应的化学方程式
分子能发生反应,产物无污染,写出该反应的化学方程式_______ 。
(4)单质⑤的晶胞结构如图所示,平均一个晶胞中含有_______ 个⑤原子,若⑤原子的原子半径为r,则该晶体的空间利用率为_______ 。(用含r的代数式表示,不必化简)


用
(1)⑥的元素符号为
(2)元素③、④的简单氢化物中,稳定性较高的是
(3)元素①与元素②、③均能形成
 分子,其中与②形成的
分子,其中与②形成的 分子的结构式为
分子的结构式为 分子能发生反应,产物无污染,写出该反应的化学方程式
分子能发生反应,产物无污染,写出该反应的化学方程式(4)单质⑤的晶胞结构如图所示,平均一个晶胞中含有

您最近一年使用:0次
名校
4 . 已知A、B、C、D、E为元素周期表中前四周期元素,且原子序数依次增大,A是短周期中原子半径最大的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素;E元素位于元素周期表的第11列。试回答下列有关的问题:
(1)E元素位于元素周期表的_______ 区。
(2)画出A、B、C中第一电离能最大的元素的原子结构式意图,_______ ;这三种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序_______ (写化学式)。
(3)D可形成化合物 。
。
① 中配体的
中配体的 模型名称是
模型名称是_______ 。该化合物中阴离子的中心原子的轨道杂化类型为_______ 。
② 中
中 的键角
的键角____ 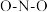 的键角(填“>”、<”、“=”),原因是
的键角(填“>”、<”、“=”),原因是____ 。
(1)E元素位于元素周期表的
(2)画出A、B、C中第一电离能最大的元素的原子结构式意图,
(3)D可形成化合物
 。
。①
 中配体的
中配体的 模型名称是
模型名称是②
 中
中 的键角
的键角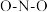 的键角(填“>”、<”、“=”),原因是
的键角(填“>”、<”、“=”),原因是
您最近一年使用:0次
解题方法
5 . X、Y、Z三种元素的结构信息如表所示。请根据信息回答下列问题:
(1)基态X原子中,核外电子占据最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(2)元素W与X处于同一周期,其基态原子中未成对电子数是核外电子总数的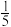 ,W的元素符号为
,W的元素符号为________ 。
(3)在第三周期中,第一电离能比Y大的主族元素有_________ (填元素符号)。
(4)YZ3分子中,Y原子的杂化轨道类型是________ ,其分子的立体构型为__________ 。
(5)Z的氢化物(H2Z)的稳定性高于Y的氢化物(H2Y),其原因是_________ 。
(6)H2Z在特定条件下得到一个H+形成H3Z+,从结构角度对上述过程分析错误的是________
| 元素 | 结构信息 |
| X | 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2 |
| Y | 基态原子的3p轨道上有4个电子 |
| Z | 元素Z的原子最外层电子数是其内层的3倍 |
(2)元素W与X处于同一周期,其基态原子中未成对电子数是核外电子总数的
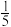 ,W的元素符号为
,W的元素符号为(3)在第三周期中,第一电离能比Y大的主族元素有
(4)YZ3分子中,Y原子的杂化轨道类型是
(5)Z的氢化物(H2Z)的稳定性高于Y的氢化物(H2Y),其原因是
(6)H2Z在特定条件下得到一个H+形成H3Z+,从结构角度对上述过程分析错误的是________
| A.中心原子的杂化轨道类型发生了改变 |
| B.中心原子的价层电子对数发生了改变 |
| C.微粒的立体结构发生了改变 |
| D.微粒中键角发生了改变 |
您最近一年使用:0次



