按要求回答下列问题:
(1)请将下列几组物质的编号填写在空格上:①D与T ②金刚石与C60 ③CH2=CHCH3和CH2=CH2④CH4和CH3CH2CH3 ⑤CH3CH2CH(CH3)2和CH3(CH2)3CH3 ⑥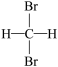 和
和 。互为同位素的是
。互为同位素的是_______ ;互为同系物的是_______ ;互为同分异构体的是_______ 。
前四周期元素A、B、M、D、E原子序数依次增大,其相关性质如表所示:
请根据以上情况,回答下列问题:
(2)A元素在周期表中的位置为____________ ,位于元素周期表的____ 区,其最高价氧化物对应水化物的阴离子的空间构型为____________ 。
(3)D的基态原子的电子占据的最高能层符号为____ ,最高能级的电子云形状为____________ 。
(4)ABD三种元素第一电离能由小到大的顺序为________________ (用元素符号表示)。BMD三种元素的简单离子的半径由大到小的顺序为________________ (用离子符号表示)。
(5)A和B形成的简单氢化物中,键角较大的是________ (填化学式),原因是________________ 。
(6)E的基态原子核外有____ 种运动状态不同的电子,该原子的简化电子排布式为_________________ 。
(1)请将下列几组物质的编号填写在空格上:①D与T ②金刚石与C60 ③CH2=CHCH3和CH2=CH2④CH4和CH3CH2CH3 ⑤CH3CH2CH(CH3)2和CH3(CH2)3CH3 ⑥
 和
和 。互为同位素的是
。互为同位素的是前四周期元素A、B、M、D、E原子序数依次增大,其相关性质如表所示:
| A | 2p能级电子半充满 |
| B | 与A同周期,且原子核外有2个未成对电子 |
| M | 前三周期元素中,M元素电负性最小 |
| D | 其基态原子的价层电子排布式为nsn-1npn+1 |
| E | 前四周期元素中,E元素基态原子未成对电子数最多 |
(2)A元素在周期表中的位置为
(3)D的基态原子的电子占据的最高能层符号为
(4)ABD三种元素第一电离能由小到大的顺序为
(5)A和B形成的简单氢化物中,键角较大的是
(6)E的基态原子核外有
更新时间:2024-04-30 13:08:47
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是中学教材中元素周期表的一部分,其中标出A~R15种元素,试根据它们回答下列问题(填具体元素符号 或化学式):

(1)最高价氧化物对应的水化物中酸性最强的是_____ ,单质中氧化性最强的是_____ ,第三周期元素形成的简单离子中半径最小的是______ 。
(2)C与E可形成一种具有漂白性的物质,它含有的化学键为_____ 。
(3)Q在元素周期表中的位置是____ ,B、C可形成化合物B2C,该化合物的核外电子总数为____ 。
(4)P的最高价氧化物对应的水化物与B的最高价氧化物对应的水化物的离子方程式:_____ 。
(5)元素E与元素F相比,金属性较强的是____ (用元素符号表示),下列表述中能证明这一事实的是______ (填序号)。
a.与酸反应时,每个F原子比每个E原子失电子数多
b.E的氢化物比F的氢化物稳定
c.E和F的单质与水反应E较剧烈
d.最高价氧化物对应水化物碱性E比F强

(1)最高价氧化物对应的水化物中酸性最强的是
(2)C与E可形成一种具有漂白性的物质,它含有的化学键为
(3)Q在元素周期表中的位置是
(4)P的最高价氧化物对应的水化物与B的最高价氧化物对应的水化物的离子方程式:
(5)元素E与元素F相比,金属性较强的是
a.与酸反应时,每个F原子比每个E原子失电子数多
b.E的氢化物比F的氢化物稳定
c.E和F的单质与水反应E较剧烈
d.最高价氧化物对应水化物碱性E比F强
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
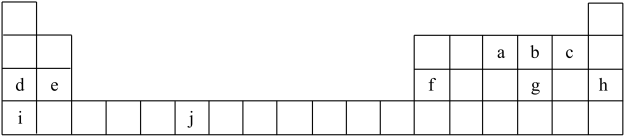
(1)f的离子结构示意图为_______ 。g的基态原子有_______ 种能量不同的电子,其能量最高的电子所占据的原子轨道的形状是_______ 形。
(2)j元素在元素周期表的位置是_______ ,属于_______ 区。
(3)表中所示元素电负性最大的是_______ (填元素符号);b、d、e的单核离子半径最小的是_______ (填离子符号);d和i的最高价氧化物的水化物碱性较强的是_______ (填化学式)。
(4)a、b、c的第一电离能从大到小排序为_______ (填元素符号)。
(5)g的两种氧化物的分子空间构型分别为_______ ,_______ 。
(6)不含化学键的分子晶体为_______ (填化学式)。
(7)i和j属于同一周期,但金属j的熔沸点比金属i高,原因是_______ 。

(1)f的离子结构示意图为
(2)j元素在元素周期表的位置是
(3)表中所示元素电负性最大的是
(4)a、b、c的第一电离能从大到小排序为
(5)g的两种氧化物的分子空间构型分别为
(6)不含化学键的分子晶体为
(7)i和j属于同一周期,但金属j的熔沸点比金属i高,原因是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W的气态氢化物具有相同的电子数,X的单质只有氧化性.
(1)写出实验室制取W2反应的离子方程式______ .
(2)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究YX2和W2的性质.
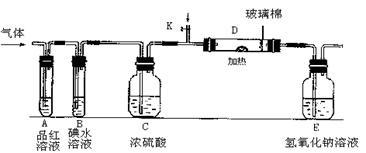
①分别通入YX2和W2,在装置A中观察到的现象是否相同(填“相同”或“不相同”)__ ;若装置D中装的是铁粉,当通入W2时D中观察到的现象为______ ;若装置D中装的是五氧化二钒,当通入YX2时,打开K通入适量X2,化学反应方程式为___ ;
②若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,则该反应的化学方程式为______ .
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入过量(填字母)_____ ,可以看到白色沉淀生成,其原因为___ (写出其中一种即可).
(4)若由元素Y和X组成—2价酸根Z,Z中Y和X的质量比为Y:X=4:3,当W2与含Z的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生.写出W2与Z的溶液完全反应产生浅黄色沉淀的离子方程式______ .
(1)写出实验室制取W2反应的离子方程式
(2)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究YX2和W2的性质.

①分别通入YX2和W2,在装置A中观察到的现象是否相同(填“相同”或“不相同”)
②若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,则该反应的化学方程式为
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入过量(填字母)
| A.氨水 | B.稀盐酸 | C.稀硝酸 | D.氯化钙 |
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素R、T、X、Y、Z原子序数依次增大,最外层电子数之和为22,R原子的最外层电子数是其内层电子数的2倍,T是地壳中含量最高的元素, 与T2-具有相同的电子层结构,Z与T同主族
与T2-具有相同的电子层结构,Z与T同主族
(1)T与X形成的化合物中含___________ (填“离子”或“共价”)键;写出X和Z形成的简单化合物的电子式:___________ 。
(2)Z的气态简单氢化物的热稳定性比T的___________ (填“强”或“弱”,下同);Z的最高价氧化物对应水化物的酸性比R的___________ 。
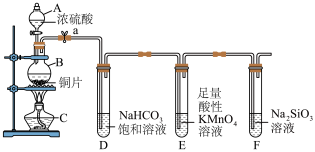
(3)某化学兴趣小组用如图装置探究元素R、Y的非金属性相对强弱:___________ 。
②试管D中通入过量 时发生反应的离子方程式为
时发生反应的离子方程式为___________ (已知酸性强弱:亚硫酸>碳酸)。
③装置E中酸性 溶液需要足量的原因是
溶液需要足量的原因是___________ 。
④能说明元素R的非金属性比元素Y的非金属性强的实验现象为___________ 。
 与T2-具有相同的电子层结构,Z与T同主族
与T2-具有相同的电子层结构,Z与T同主族(1)T与X形成的化合物中含
(2)Z的气态简单氢化物的热稳定性比T的
(3)某化学兴趣小组用如图装置探究元素R、Y的非金属性相对强弱:
②试管D中通入过量
 时发生反应的离子方程式为
时发生反应的离子方程式为③装置E中酸性
 溶液需要足量的原因是
溶液需要足量的原因是④能说明元素R的非金属性比元素Y的非金属性强的实验现象为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】元素a、b、c、d、e为前20号主族元素,原子序数依次增大。b元素原子最外层电子数与核外电子总数之比为2:3;c的氢化物能与其最高价氧化物对应的水化物反应生成一种盐;a与b、c均可以形成电子总数为10的分子;d元素的氧化物能使品红溶液褪色,且加热后品红颜色复原;e原子是前20号主族元素中原子半径最大的。请回答:
(1)bd2的电子式_________ ;e的最高价氧化物的水化物所含化学键类型为_______ 、________
(2)在只由a、b两种元素组成的化合物中,如果化合物的质量相同,在氧气中完全燃烧时消耗氧气最多的是________ ;
(3)d的最高价氧化物对应的水化物是铅蓄电池的电解质溶液。正极板上覆盖有二氧化铅,负极板上覆盖有铅,① 写出放电时负极的电极反应式:______________________________ ;
② 铅蓄电池放电时,溶液的pH将_________ (填增大、减小或不变)。当外电路上有0.5mol电子通过时,溶液中消耗电解质的物质的量为___________ 。
(1)bd2的电子式
(2)在只由a、b两种元素组成的化合物中,如果化合物的质量相同,在氧气中完全燃烧时消耗氧气最多的是
(3)d的最高价氧化物对应的水化物是铅蓄电池的电解质溶液。正极板上覆盖有二氧化铅,负极板上覆盖有铅,① 写出放电时负极的电极反应式:
② 铅蓄电池放电时,溶液的pH将
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、W、R是5种短周期元素,原子序数依次增大。已知由X组成的单质是最理想的气体燃料,Y与X形成的化合物YX4是天然气的主要成分,Z的原子最外层电子数是次外层电子数的3倍,W、R处于同一周期,W是该周期中金属性最强的元素,W与R能形成化合物WR。请回答下列问题:
(1)Z在元素周期表中的位置是________ ;R的原子结构示意图是_________ ;R的最高价氧化物对应水化物的化学式为_________ 。
(2)工业上常用化合物WR冶炼W的单质,若要得到2.3 t W,则至少需要WR的质量是_____ 。
(3)W与Z形成的化合物W2Z2,可作供氧剂,其反应原理是________ (用化学方程式表示)。
(4)Y的最高价氧化物与过量W的最高价氧化物对应水化物的溶液反应,有关的离子方程式为____ 。
(5)在一定条件下,R单质能与硫反应生成一种用途广泛的硫化剂S2R2。S2R2与足量水反应有黄色沉淀生成,同时生成能使品红溶液褪色的无色气体,则该反应的化学方程式是______ 。
(1)Z在元素周期表中的位置是
(2)工业上常用化合物WR冶炼W的单质,若要得到2.3 t W,则至少需要WR的质量是
(3)W与Z形成的化合物W2Z2,可作供氧剂,其反应原理是
(4)Y的最高价氧化物与过量W的最高价氧化物对应水化物的溶液反应,有关的离子方程式为
(5)在一定条件下,R单质能与硫反应生成一种用途广泛的硫化剂S2R2。S2R2与足量水反应有黄色沉淀生成,同时生成能使品红溶液褪色的无色气体,则该反应的化学方程式是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】由氧元素形成的常见物质有H2O、H2O2、O2和O3等。
(1)基态氧原子的电子排布式是_______ 。
(2)H2O分子的VSEPR模型是_______ 形。
(3)对H2O2分子结构的研究,曾有以下推测:

①根据测定H2O2分子中_______ (填字母序号),确定其结构一定不是甲。
a.H-O键长 b.O-O键能 c.H-O-O键角
②由于H2O2不稳定,很难得到晶体。20世纪40年代初,卢嘉锡等化学家用尿素( )与H2O2形成较稳定的尿素过氧化氢复合物晶体,进而测得H2O2结构为乙。上述晶体中尿素与H2O2分子交替排列且二者中的O均与另外分子的H之间形成氢键。
)与H2O2形成较稳定的尿素过氧化氢复合物晶体,进而测得H2O2结构为乙。上述晶体中尿素与H2O2分子交替排列且二者中的O均与另外分子的H之间形成氢键。
a.H2O2为_______ (填“极性”或“非极性”)分子。
b.用“X—H…Y”表示出上述晶体中形成的氢键:_______ 。
(4)O2的晶胞为立方体,结构如下。
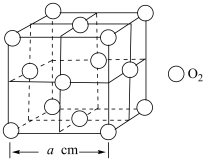
根据图中信息,可计算O2晶体密度是_____ g·cm-3。
(5)已知O3分子空间结构为V形,中心O为sp2杂化。除σ键外,O3分子中还形成了含4个电子的大π键。每个O3分子中用于成键的电子总数是_____ 个,中心O提供参与成键的电子数是_____ 个。
(1)基态氧原子的电子排布式是
(2)H2O分子的VSEPR模型是
(3)对H2O2分子结构的研究,曾有以下推测:

①根据测定H2O2分子中
a.H-O键长 b.O-O键能 c.H-O-O键角
②由于H2O2不稳定,很难得到晶体。20世纪40年代初,卢嘉锡等化学家用尿素(
 )与H2O2形成较稳定的尿素过氧化氢复合物晶体,进而测得H2O2结构为乙。上述晶体中尿素与H2O2分子交替排列且二者中的O均与另外分子的H之间形成氢键。
)与H2O2形成较稳定的尿素过氧化氢复合物晶体,进而测得H2O2结构为乙。上述晶体中尿素与H2O2分子交替排列且二者中的O均与另外分子的H之间形成氢键。a.H2O2为
b.用“X—H…Y”表示出上述晶体中形成的氢键:
(4)O2的晶胞为立方体,结构如下。

根据图中信息,可计算O2晶体密度是
(5)已知O3分子空间结构为V形,中心O为sp2杂化。除σ键外,O3分子中还形成了含4个电子的大π键。每个O3分子中用于成键的电子总数是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铊(Tl)在工业中的用途非常广泛。从某铅锌厂的富铊灰(主要成分为 PbO、FeO、 )中回收铊的工艺流程如图所示:
)中回收铊的工艺流程如图所示:
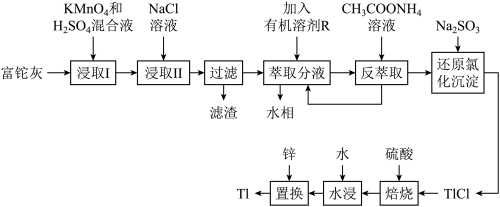
已知:
①在氯化物—硫酸水溶液中,Tl以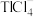 形式存在
形式存在
②已知萃取过程的反应原理为
③常温下 ,
,
请回答下列问题:
(1)Tl与Al同主族,写出基态Tl原子的价电子排布式___________ 。
(2)写出“浸取Ⅰ”中 发生反应的离子方程式
发生反应的离子方程式___________ 。
(3)“萃取分液”过程若在实验室进行,必须使用的玻璃仪器有烧杯、___________ (填名称)。
(4)常温下,向“萃取”过程后的水相中加入 NaOH 溶液,调pH 回收铁。已知水相中 mol/L,控制 pH 范围为
mol/L,控制 pH 范围为___________ (已知当溶液中离子浓度小于 时,通常认为该离子沉淀完全)。
时,通常认为该离子沉淀完全)。
(5)请从化学平衡的角度解释“反萃取”过程中加入 ,溶液的原因
,溶液的原因_________________ 。
(6)写出“还原氯化沉淀”中反应的离子方程式___________ 。
(7)已知a kg富铊灰中 的质量分数为 b%,经过上述流程后最终得到纯铊为c kg,则产率为
的质量分数为 b%,经过上述流程后最终得到纯铊为c kg,则产率为___________ (用含字母a、b、c的表达式表示)。
 )中回收铊的工艺流程如图所示:
)中回收铊的工艺流程如图所示:
已知:
①在氯化物—硫酸水溶液中,Tl以
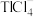 形式存在
形式存在②已知萃取过程的反应原理为

③常温下
 ,
,
请回答下列问题:
(1)Tl与Al同主族,写出基态Tl原子的价电子排布式
(2)写出“浸取Ⅰ”中
 发生反应的离子方程式
发生反应的离子方程式(3)“萃取分液”过程若在实验室进行,必须使用的玻璃仪器有烧杯、
(4)常温下,向“萃取”过程后的水相中加入 NaOH 溶液,调pH 回收铁。已知水相中
 mol/L,控制 pH 范围为
mol/L,控制 pH 范围为 时,通常认为该离子沉淀完全)。
时,通常认为该离子沉淀完全)。(5)请从化学平衡的角度解释“反萃取”过程中加入
 ,溶液的原因
,溶液的原因(6)写出“还原氯化沉淀”中反应的离子方程式
(7)已知a kg富铊灰中
 的质量分数为 b%,经过上述流程后最终得到纯铊为c kg,则产率为
的质量分数为 b%,经过上述流程后最终得到纯铊为c kg,则产率为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】艾姆斯实验室已制造出包含钙、钾、铁和砷以及少量镍的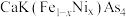 新型化合物材料,回答下列问题:
新型化合物材料,回答下列问题:
(1)化合物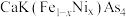 中的Fe属于元素周期表中
中的Fe属于元素周期表中___________ 区,基态Fe原子的原子结构示意图为___________ 。
(2)杀虫剂 中As原子采取
中As原子采取___________ 杂化。
(3) 基态价层电子排布式
基态价层电子排布式___________ 。
(4)在稀氨水介质中, 与丁二酮肟(分子式为
与丁二酮肟(分子式为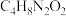 )反应可生成鲜红色沉淀,其分子结构如图所示,该分子中存在的化学键有)
)反应可生成鲜红色沉淀,其分子结构如图所示,该分子中存在的化学键有)___________ 。
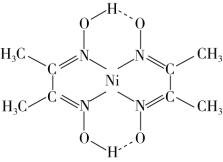
a.氢键 b. 键 c.
键 c. 键 d.配位键
键 d.配位键
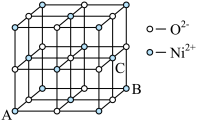
(5) 晶胞结构如下图所示,其中
晶胞结构如下图所示,其中 的配位数为
的配位数为___________ , 填入
填入 所形成的
所形成的___________ (填“四面体”或“八面体”)空隙中。
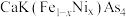 新型化合物材料,回答下列问题:
新型化合物材料,回答下列问题:(1)化合物
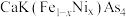 中的Fe属于元素周期表中
中的Fe属于元素周期表中(2)杀虫剂
 中As原子采取
中As原子采取(3)
 基态价层电子排布式
基态价层电子排布式(4)在稀氨水介质中,
 与丁二酮肟(分子式为
与丁二酮肟(分子式为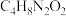 )反应可生成鲜红色沉淀,其分子结构如图所示,该分子中存在的化学键有)
)反应可生成鲜红色沉淀,其分子结构如图所示,该分子中存在的化学键有)
a.氢键 b.
 键 c.
键 c. 键 d.配位键
键 d.配位键(5)
 晶胞结构如下图所示,其中
晶胞结构如下图所示,其中 的配位数为
的配位数为 填入
填入 所形成的
所形成的
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】碳族化合物在研究和生产中有许多重要用途,请回答下列问题:
(1)已知SiH4中硅元素为+4价,则H、C、O、Si的电负性由大到小的顺序为_______ 。
(2)基态锗原子(Ge)的简化电子排布式为_______ 。
(3)氮化硅(Si3N4)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N-Si-N_______ Si-N-Si(填“>”、“<”或“=”)。

(4)基态硅原子核外电子的空间运动状态有_______ 种,太阳能电池板主要材料为单晶硅或多晶硅,硅与氢能形成一系列二元化合物如SiH4、Si2H6等,丁硅烯(Si4H8)中σ键与π键的个数比为_______ ,其中硅的杂化方式是_______ 。
(1)已知SiH4中硅元素为+4价,则H、C、O、Si的电负性由大到小的顺序为
(2)基态锗原子(Ge)的简化电子排布式为
(3)氮化硅(Si3N4)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N-Si-N

(4)基态硅原子核外电子的空间运动状态有
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】一种新型硫酸盐功能电解液由 和
和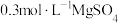 混合组成,电化学测试表明该电解液构建的
混合组成,电化学测试表明该电解液构建的 、
、 电池可以稳定循环500次以上。
电池可以稳定循环500次以上。
(1) 中三种原子的半径由小到大的顺序是
中三种原子的半径由小到大的顺序是_____ (用元素符号表示),其中电负性最大的元素是_____ (填名称)。
(2)第一电离能 的原因是
的原因是_____ 。
(3) 中,基态
中,基态 核外电子的空间运动状态有
核外电子的空间运动状态有_____ 种, 中
中 键和
键和 键的数目之比为
键的数目之比为_____ 。
(4) 中磷原子的杂化类型是
中磷原子的杂化类型是_____ 。
(5)N、O两种元素形成的简单氢化物的键角:
_____  (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是_____ 。
(6) 的立方晶胞结构如图所示。已知晶胞的边长为npm,设
的立方晶胞结构如图所示。已知晶胞的边长为npm,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
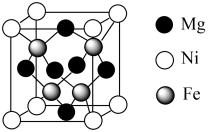
①
_____ 。
②该晶体密度是_____  (用含n、
(用含n、 的代数式表示)。
的代数式表示)。
 和
和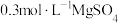 混合组成,电化学测试表明该电解液构建的
混合组成,电化学测试表明该电解液构建的 、
、 电池可以稳定循环500次以上。
电池可以稳定循环500次以上。(1)
 中三种原子的半径由小到大的顺序是
中三种原子的半径由小到大的顺序是(2)第一电离能
 的原因是
的原因是(3)
 中,基态
中,基态 核外电子的空间运动状态有
核外电子的空间运动状态有 中
中 键和
键和 键的数目之比为
键的数目之比为(4)
 中磷原子的杂化类型是
中磷原子的杂化类型是(5)N、O两种元素形成的简单氢化物的键角:

 (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是(6)
 的立方晶胞结构如图所示。已知晶胞的边长为npm,设
的立方晶胞结构如图所示。已知晶胞的边长为npm,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
①

②该晶体密度是
 (用含n、
(用含n、 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氢能是一种极具发展潜力的清洁能源,下列物质都是具有广阔应用前景的储氢材料。回答下列问题:
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原产物为_____ 。
(2)Ti-Fe合金室温下吸、放氢的速率快,Ti元素在周期表中的位置是____ 。
(3) (氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成。
进行合成。
① 中涉及的元素H、B、N电负性最大的是
中涉及的元素H、B、N电负性最大的是______ 。
②键角:
_____  (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是_______ 。
(4)Fe-Mg合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
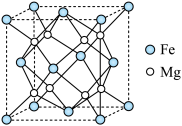
①距离Mg原子最近的Fe原子个数是___________ 。
②若该晶胞的棱长为anm,阿伏加德罗常数的值为 ,则该合金的密度为
,则该合金的密度为___________  。
。
③若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下 的体积约为
的体积约为___________ L。
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原产物为
(2)Ti-Fe合金室温下吸、放氢的速率快,Ti元素在周期表中的位置是
(3)
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成。
进行合成。①
 中涉及的元素H、B、N电负性最大的是
中涉及的元素H、B、N电负性最大的是②键角:

 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是(4)Fe-Mg合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离Mg原子最近的Fe原子个数是
②若该晶胞的棱长为anm,阿伏加德罗常数的值为
 ,则该合金的密度为
,则该合金的密度为 。
。③若该晶体储氢时,
 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下 的体积约为
的体积约为
您最近半年使用:0次



