解题方法
1 . A、B、D、E、F五种元素的原子序数依次增大,且均为元素周期表前四周期元素,其中基态A原子的最外层电子数是最内层电子数的2倍;基态B原子的2p轨道上有3个未成对电子;基态D原子的s能级和p能级的电子总数相等;E和D可形成淡黄色固体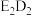 ;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:
;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:
(1)基态F原子价电子排布式___________ ;F原子的核外电子运动状态有___________ 种;空间运动状态有___________ 种。
(2) 的空间结构是
的空间结构是___________ , 的中心原子采取
的中心原子采取___________ 杂化; 中
中 的键角
的键角___________ (填大于、小于或等于) 中
中 的键角。
的键角。
(3)已知 是直线形分子,且有对称性,则
是直线形分子,且有对称性,则 分子的结构式为
分子的结构式为___________ ;其中 键与
键与 键的个数比为
键的个数比为___________ 。
(4) 比
比 稳定,请用原子结构知识解释其原因:
稳定,请用原子结构知识解释其原因:___________ 。
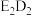 ;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:
;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:(1)基态F原子价电子排布式
(2)
 的空间结构是
的空间结构是 的中心原子采取
的中心原子采取 中
中 的键角
的键角 中
中 的键角。
的键角。(3)已知
 是直线形分子,且有对称性,则
是直线形分子,且有对称性,则 分子的结构式为
分子的结构式为 键与
键与 键的个数比为
键的个数比为(4)
 比
比 稳定,请用原子结构知识解释其原因:
稳定,请用原子结构知识解释其原因:
您最近半年使用:0次
名校
解题方法
2 . 现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素.请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有____ 个方向,原子轨道呈__________ 形,C简单离子核外有______ 种运动状态不同的电子.
(2) 难溶于
难溶于 ,简要说明理由:
,简要说明理由:________________ .
(3) 分子的空间构型为
分子的空间构型为__________ ,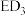 分子的
分子的 模型名称为
模型名称为__________ .
(4)下列气态分子 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为_______________ .
| 元素 | 相关信息 |
| A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 原子核外p电子数与s电子数相等 |
| C | 基态原子的价电子排布为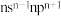 |
| D | 能层数与C相同,且电负性比C大 |
| E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)
 难溶于
难溶于 ,简要说明理由:
,简要说明理由:(3)
 分子的空间构型为
分子的空间构型为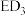 分子的
分子的 模型名称为
模型名称为(4)下列气态分子
 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为
您最近半年使用:0次
名校
3 . X、Y、Z、Q、M、R、T、W是原子序数依次增大的前四周期元素,其中X元素的原子核外只有一个电子;X与Y原子序数之和等于Z的原子序数;Z元素的气态氢化物极易溶于水,可用作制冷剂;Q基态原子核外s能级电子总数与p能级电子总数相等;M基态原子核外有6个原子轨道排有电子,且只有1个未成对电子;R最高价氧化物的水化物是一种强酸;T为s区元素且基态原子各能层没有未成对电子;W最外层只有1个电子,其内层各能级所有轨道电子均成对。
(1)Y的基态原子最高能层符号为___________ ,Z基态原子有___________ 种不同运动状态的电子。
(2)Y、Z、Q与分别X形成的10电子化合物,键角由大到小的顺序是___________ (用分子式表示)。X与Q组成的原子个数1:1的化合物的电子式为___________ 。
(3)W在元素周期表中的位置为___________ ,其基态原子的价电子轨道表示式为___________ 。
(4)下列说法不正确的是___________ 。
A.X、Y、Z都能与Q形成原子个数之比为1:1的化合物
B.Y、Z、Q的第一电离能依次逐渐增大
C.简单离子半径大小:R>T>M
D.W的焰色试验与原子核外电子跃迁吸收能量有关
E.M同周期元素氧化物的晶体类型按离子晶体、共价晶体、分子晶体的顺序过渡
(1)Y的基态原子最高能层符号为
(2)Y、Z、Q与分别X形成的10电子化合物,键角由大到小的顺序是
(3)W在元素周期表中的位置为
(4)下列说法不正确的是
A.X、Y、Z都能与Q形成原子个数之比为1:1的化合物
B.Y、Z、Q的第一电离能依次逐渐增大
C.简单离子半径大小:R>T>M
D.W的焰色试验与原子核外电子跃迁吸收能量有关
E.M同周期元素氧化物的晶体类型按离子晶体、共价晶体、分子晶体的顺序过渡
您最近半年使用:0次
名校
4 . 按要求回答下列问题:
(1)请将下列几组物质的编号填写在空格上:①D与T ②金刚石与C60 ③CH2=CHCH3和CH2=CH2④CH4和CH3CH2CH3 ⑤CH3CH2CH(CH3)2和CH3(CH2)3CH3 ⑥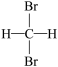 和
和 。互为同位素的是
。互为同位素的是_______ ;互为同系物的是_______ ;互为同分异构体的是_______ 。
前四周期元素A、B、M、D、E原子序数依次增大,其相关性质如表所示:
请根据以上情况,回答下列问题:
(2)A元素在周期表中的位置为____________ ,位于元素周期表的____ 区,其最高价氧化物对应水化物的阴离子的空间构型为____________ 。
(3)D的基态原子的电子占据的最高能层符号为____ ,最高能级的电子云形状为____________ 。
(4)ABD三种元素第一电离能由小到大的顺序为________________ (用元素符号表示)。BMD三种元素的简单离子的半径由大到小的顺序为________________ (用离子符号表示)。
(5)A和B形成的简单氢化物中,键角较大的是________ (填化学式),原因是________________ 。
(6)E的基态原子核外有____ 种运动状态不同的电子,该原子的简化电子排布式为_________________ 。
(1)请将下列几组物质的编号填写在空格上:①D与T ②金刚石与C60 ③CH2=CHCH3和CH2=CH2④CH4和CH3CH2CH3 ⑤CH3CH2CH(CH3)2和CH3(CH2)3CH3 ⑥
 和
和 。互为同位素的是
。互为同位素的是前四周期元素A、B、M、D、E原子序数依次增大,其相关性质如表所示:
| A | 2p能级电子半充满 |
| B | 与A同周期,且原子核外有2个未成对电子 |
| M | 前三周期元素中,M元素电负性最小 |
| D | 其基态原子的价层电子排布式为nsn-1npn+1 |
| E | 前四周期元素中,E元素基态原子未成对电子数最多 |
(2)A元素在周期表中的位置为
(3)D的基态原子的电子占据的最高能层符号为
(4)ABD三种元素第一电离能由小到大的顺序为
(5)A和B形成的简单氢化物中,键角较大的是
(6)E的基态原子核外有
您最近半年使用:0次
名校
5 . 某原科经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大。元素A、B、C、D、E的原子结构等信息如下:
请回答下列问题:(用A、B、C、D、E所对应的元素符号作答)
(1)E的二价离子的电子排布式为___________ ;E位于元素周期表的___________ 。
(2)A2B2D4常用作除锈剂,1mol A2B2D4分子中含有σ键数目为___________ ,用质谱法测得该物质的最大质荷比为___________ 。
(3)元素As与C同族。推测As的氢化物 的空间构型
的空间构型___________ ;C元素的氢化物的键角___________  的键角(填>,<或=,下同),原因是
的键角(填>,<或=,下同),原因是___________ ;在水中溶解度:CH3___________ AsH3,原因是___________ 。
(4)S元素与D同族, 的一种三聚体环状结构如图所示,该结构中
的一种三聚体环状结构如图所示,该结构中 键长有两类,一类键长约140pm,另一类键长约为169pm,较长的键为
键长有两类,一类键长约140pm,另一类键长约为169pm,较长的键为___________ (填a或b)。
| 元素性质或原子结构 | |
| A | 周期表中原子半径最小的元素 |
| B | 原子核外有三种不同的能级且各个能级所填充的电子数相同 |
| C | 最外层P轨道半充满 |
| D | 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 |
| E | 位于ds区且原子的最外层电子数与A的相同 |
(1)E的二价离子的电子排布式为
(2)A2B2D4常用作除锈剂,1mol A2B2D4分子中含有σ键数目为
(3)元素As与C同族。推测As的氢化物
 的空间构型
的空间构型 的键角(填>,<或=,下同),原因是
的键角(填>,<或=,下同),原因是(4)S元素与D同族,
 的一种三聚体环状结构如图所示,该结构中
的一种三聚体环状结构如图所示,该结构中 键长有两类,一类键长约140pm,另一类键长约为169pm,较长的键为
键长有两类,一类键长约140pm,另一类键长约为169pm,较长的键为
您最近半年使用:0次
名校
解题方法
6 . 现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素。请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向,C简单离子核外有___________ 种运动状态不同的电子。
(2)A2B2难溶于CS2,简要说明理由:______________ 。
(3)ED3分子的VSEPR模型名称为____________ ,空间构型为____________ 。
(4)下列气态分子BCl3、CCl4、H2O和BeCl2中,其键角由大到小的顺序为_____________ 。
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:RCO﹣>﹣F>﹣Cl>﹣Br>﹣I>﹣C≡CH>﹣C6H5>﹣H,则下列物质酸性由强到弱的顺序是___________ (填序号)。
A.CH3COOH B.ClCH2COOH C.HC≡CCH2COOH D.C6H5CH2COOH
元素 | 相关信息 |
A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B | 原子核外p电子数与s电子数相等 |
C | 基态原子的价电子排布为nsn-1npn+1 |
D | 能层数与C相同,且电负性比C大 |
E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)A2B2难溶于CS2,简要说明理由:
(3)ED3分子的VSEPR模型名称为
(4)下列气态分子BCl3、CCl4、H2O和BeCl2中,其键角由大到小的顺序为
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:RCO﹣>﹣F>﹣Cl>﹣Br>﹣I>﹣C≡CH>﹣C6H5>﹣H,则下列物质酸性由强到弱的顺序是
A.CH3COOH B.ClCH2COOH C.HC≡CCH2COOH D.C6H5CH2COOH
您最近半年使用:0次
名校
解题方法
7 . a~h为元素周期表中前四周期相应元素。
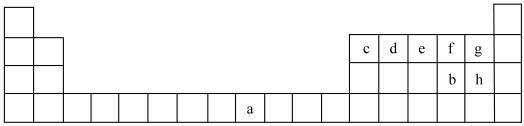
回答下列问题:
(1)元素a基态原子的价电子排布式为_______ 。
(2)元素d与b形成的稳定化合物属于_______ 分子(填“极性”或“非极性”)。
(3)df2、bf2与SiO2三个物质熔点由高到低的顺序为_______ (填化学式),理由为_______ 。
(4)化合物cg3分子的空间结构为_______ ,其中心原子的杂化方式为_______ ;键角cg3_______ eg3(填“>”“=”或“<”);a~h元素组成的含氧酸根离子中,空间结构与cg3相同的一种是_______ (填离子符号)。

回答下列问题:
(1)元素a基态原子的价电子排布式为
(2)元素d与b形成的稳定化合物属于
(3)df2、bf2与SiO2三个物质熔点由高到低的顺序为
(4)化合物cg3分子的空间结构为
您最近半年使用:0次
名校
8 . W、R、X、Y、Z是原子序数依次增大的前四周期元素,其元素性质或原子结构如表:
回答下列问题:
(1)W的基态原子有_______ 种不同运动状态的电子,Z的价电子排布图为_______ 。
(2)W、R、X的简单氢化物中,三元素的原子的轨道杂化方式均为_______ ,键角由大到小的顺序是_______ (用对应的分子式表示),原因是_______ 。
(3)已知:羧酸的酸性可用pKa(pKa= -lg Ka)的大小来衡量,pKa越小,酸性越强。
由表可见,酸性:三氯乙酸_______ 三氟乙酸(填“大于”“小于”或“等于”),从键的极性角度解释原因:_______ 。
(4)联氨(N2H4)也叫肼,常用于火箭推进剂。N2H4_______ (填“难”或“易”)溶于水,原因_______ 。
| 元素 | 元素性质或原子结构 |
| W | 基态原子L能层所有能级上电子数相同 |
| R | 第二周期元素基态原子中未成对电子最多 |
| X | 基态原子核外s能级上电子总数与p能级上电子总数相等,且第一电离能低于同周期相邻元素 |
| Y | 最外层电子数是次外层电子数的一半 |
| Z | 最外层只有1个电子,其他内层各能级所有轨道电子均成对 |
(1)W的基态原子有
(2)W、R、X的简单氢化物中,三元素的原子的轨道杂化方式均为
(3)已知:羧酸的酸性可用pKa(pKa= -lg Ka)的大小来衡量,pKa越小,酸性越强。
| 羧酸 | pKa |
| 三氯乙酸(CCl3COOH) | 0.65 |
| 三氟乙酸(CF3COOH) | 0. 23 |
(4)联氨(N2H4)也叫肼,常用于火箭推进剂。N2H4
您最近半年使用:0次
9 .  是周期表中
是周期表中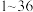 号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多.
号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多.
(1) 的电子式为
的电子式为______________ , 中含有的化学键类型为
中含有的化学键类型为______________ .
(2)B、C两种元素的第三电离能由大到小的顺序为______________ (填元素符号)
(3)E在元素周期表中位置为______________ ,位于元素周期表的______________ 区.
(4)比较:①键角大小:
______________  ;②在水中的溶解性大小
;②在水中的溶解性大小
______________  ;
;
 是周期表中
是周期表中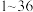 号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多.
号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多.(1)
 的电子式为
的电子式为 中含有的化学键类型为
中含有的化学键类型为(2)B、C两种元素的第三电离能由大到小的顺序为
(3)E在元素周期表中位置为
(4)比较:①键角大小:

 ;②在水中的溶解性大小
;②在水中的溶解性大小
 ;
;
您最近半年使用:0次
10 . 下表是元素周期表的一部分,表中所列代码字母分别代表一种化学元素。
试回答下列问题:
(1)J的元素符号为___________ ,在周期表中位于___________ 区。
(2)请写出基态I原子的核外电子表示式:___________ ;基态C原子的价层电子轨道表示式:___________ 。
(3)元素A、B、G、H的电负性值从大到小的顺序是___________ (用元素符号表示)。
(4)元素A、B、C形成的最简单氢化物中键角最大的是___________ (用氢化物化学式表示),其中B的最简单氢化物空间构型为___________ 。
(5)写出G单质与强碱 溶液反应的离子反应方程式
溶液反应的离子反应方程式___________ 。
| A | B | C | D | E | |||||||||||||
| F | G | H | |||||||||||||||
| L | I | J | M | K | N |
(1)J的元素符号为
(2)请写出基态I原子的核外电子表示式:
(3)元素A、B、G、H的电负性值从大到小的顺序是
(4)元素A、B、C形成的最简单氢化物中键角最大的是
(5)写出G单质与强碱
 溶液反应的离子反应方程式
溶液反应的离子反应方程式
您最近半年使用:0次



