名校
1 . 新冠病毒曾经伤害人类,也是曾经让你惧怕的病毒,但它却只不过是蛋白质包裹着的DNA而已,使用适当浓度的84消毒液、双氧水等消毒剂即可将其杀死。但是两者混合使用,消毒效果几乎降为零。回答下列问题:
(1)上述两种消毒剂中有效成分的电子式为_______ 、_______ ,两者结构中都含有_______ (填 “离子键”、“极性共价键”或“非极性共价键”)。
(2)如图所示是家用制取84消毒液的装置,以石墨为电极电解饱和食盐水,则阳极为_______ (填“a”或“b”)。
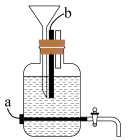
将湿润的淀粉碘化钾试纸靠近导管处,未显蓝色。此制备的总反应的离子方程式为_______ 。
(3)上述两种消毒剂混合使用,有无毒气体产生,该化学反应方程式为_______ ,其中被还原的元素为_______ 。
利用75%酒精也可以消杀新冠病毒。如果将84消毒液与之混用以提高消杀效果,那你有可能会中毒。因为此时会产生氯仿,进而继续被氧化为光气,光气是具有烂苹果气味的毒气,其分子结构如图所示:

(4)请你从化学键角度阐述光气中C-Cl键长大于C=O键长的原因_______ 。
(5)若把光气分子中的氯原子换成氟原子,推测F-C-F键角_______ 111.8°(填“<”、 “>”或“=”),理由为_______ 。
当氯酸的浓度大于40%时,会发生分解反应:aHClO3=bO2↑+cCl2↑+dHClO4+eH2O。将湿润的淀粉碘化钾试纸较长时间地靠近产生的气体,则试纸先变蓝后又变回白色。
(6)aHClO3=bO2↑+cCl2↑+dHClO4+eH2O,用单线桥法标出该反应的电子转移方向,并利用电子守恒写出关于b、c、d的数学表达式_______ 。
(7)HClO4的结构式为_______ ,基态氯原子核外能量最高的电子存在_______ 种不同的空间运动状态,基态氧原子的价电子中有_______ 对成对电子。
(8)使变蓝的试纸又变白的原因为_______ 。
(9)氯元素在自然界有35Cl和37Cl两种同位素,已知氯元素的近似相对原子质量为35.5,则37Cl所占的质量分数为_______ % (保留4位有效数字)。
(1)上述两种消毒剂中有效成分的电子式为
(2)如图所示是家用制取84消毒液的装置,以石墨为电极电解饱和食盐水,则阳极为

将湿润的淀粉碘化钾试纸靠近导管处,未显蓝色。此制备的总反应的离子方程式为
(3)上述两种消毒剂混合使用,有无毒气体产生,该化学反应方程式为
利用75%酒精也可以消杀新冠病毒。如果将84消毒液与之混用以提高消杀效果,那你有可能会中毒。因为此时会产生氯仿,进而继续被氧化为光气,光气是具有烂苹果气味的毒气,其分子结构如图所示:

(4)请你从化学键角度阐述光气中C-Cl键长大于C=O键长的原因
(5)若把光气分子中的氯原子换成氟原子,推测F-C-F键角
当氯酸的浓度大于40%时,会发生分解反应:aHClO3=bO2↑+cCl2↑+dHClO4+eH2O。将湿润的淀粉碘化钾试纸较长时间地靠近产生的气体,则试纸先变蓝后又变回白色。
(6)aHClO3=bO2↑+cCl2↑+dHClO4+eH2O,用单线桥法标出该反应的电子转移方向,并利用电子守恒写出关于b、c、d的数学表达式
(7)HClO4的结构式为
(8)使变蓝的试纸又变白的原因为
(9)氯元素在自然界有35Cl和37Cl两种同位素,已知氯元素的近似相对原子质量为35.5,则37Cl所占的质量分数为
您最近半年使用:0次
名校
2 . 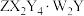 是一种白色晶体,不溶于水,用于陶瓷上釉等。W、X、Y、Z为前20号元素,原子序数依次增加且加和为35,已知X原子最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,
是一种白色晶体,不溶于水,用于陶瓷上釉等。W、X、Y、Z为前20号元素,原子序数依次增加且加和为35,已知X原子最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,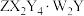 热分解可制备ZY,该化合物的热重曲线如图所示,下列叙述错误的是
热分解可制备ZY,该化合物的热重曲线如图所示,下列叙述错误的是

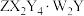 是一种白色晶体,不溶于水,用于陶瓷上釉等。W、X、Y、Z为前20号元素,原子序数依次增加且加和为35,已知X原子最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,
是一种白色晶体,不溶于水,用于陶瓷上釉等。W、X、Y、Z为前20号元素,原子序数依次增加且加和为35,已知X原子最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,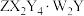 热分解可制备ZY,该化合物的热重曲线如图所示,下列叙述错误的是
热分解可制备ZY,该化合物的热重曲线如图所示,下列叙述错误的是
| A.第一电离能:Y>X>Z |
B.键角: |
C.Z、X可以组成含有共价键的离子化合物 |
D.600℃热分解后生成固体化合物 |
您最近半年使用:0次
名校
3 . W、X、Y、Z、M五种短周期元素,原子序数依次增大。W元素的原子最外层电子数是次外层的3倍;X元素的原子核外s能级上的电子总数与p能级上的电子总数相等,且第一电离能都高于同周期相邻元素;Y元素是地壳中含量最多的金属元素;Z元素的单质可作半导体材料;M基态原子核外有9种不同空间运动状态的电子,且只有一个不成对电子。下列说法正确的是
A.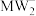 的键角比 的键角比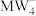 的键角大 的键角大 |
| B.第一电离能:W>Z>M>X>Y |
| C.原子半径:W>X>Y>Z>M |
| D.ZW2的熔点比ZM4的熔点高 |
您最近半年使用:0次
2023-10-04更新
|
363次组卷
|
2卷引用:湖南省长沙市长郡中学2024届高三上学期月考(2)化学试题
名校
解题方法
4 . X、Y、Z、Q、W是原子序数依次增大的前四周期元素,其中X是宇宙中含量最多的元素; 元素原子最高能级的不同轨道都有电子,并且自旋方向相同;
元素原子最高能级的不同轨道都有电子,并且自旋方向相同; 元素原子的价层电子排布是
元素原子的价层电子排布是 ;Q、W元素原子的最外层均只有1个电子,但
;Q、W元素原子的最外层均只有1个电子,但 元素原子中只有两种形状的电子云,
元素原子中只有两种形状的电子云, 元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是
元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是
 元素原子最高能级的不同轨道都有电子,并且自旋方向相同;
元素原子最高能级的不同轨道都有电子,并且自旋方向相同; 元素原子的价层电子排布是
元素原子的价层电子排布是 ;Q、W元素原子的最外层均只有1个电子,但
;Q、W元素原子的最外层均只有1个电子,但 元素原子中只有两种形状的电子云,
元素原子中只有两种形状的电子云, 元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是
元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是A.电负性: | B.键角: |
C. 的阴阳离子比为 的阴阳离子比为 | D.W元素位于元素周期表的d区 |
您最近半年使用:0次
名校
解题方法
5 . X、Y、Z、W为原子序数依次增大的前四周期元素,基态原子中,X为元素周期表中半径最小的原子,Z是地壳中含量最多的元素,W原子的价电子排布为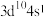 ,X、Y、Z、W形成的阳离子如图所示,下列说法正确的是
,X、Y、Z、W形成的阳离子如图所示,下列说法正确的是

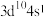 ,X、Y、Z、W形成的阳离子如图所示,下列说法正确的是
,X、Y、Z、W形成的阳离子如图所示,下列说法正确的是
| A.原子半径:Z>Y>X |
| B.该阳离子中心离子的配位数为6 |
| C.氢化物的沸点:Z>Y |
D.两种配体中的键角: |
您最近半年使用:0次
2023-08-06更新
|
330次组卷
|
3卷引用:广东省六校2024届高三第一次联考化学试题
解题方法
6 . 短周期主族元素X、Y、Z原子序数依次递增,其序数和为13,可组成固态储氢材料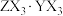 。Z是空气中含量最高的元素。下列说法错误的是
。Z是空气中含量最高的元素。下列说法错误的是
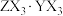 。Z是空气中含量最高的元素。下列说法错误的是
。Z是空气中含量最高的元素。下列说法错误的是| A.第一电离能:Y>Z | B.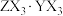 中存在配位键 中存在配位键 |
| C.Z、Y轨道杂化类型相同 | D.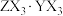 中 中 小于120° 小于120° |
您最近半年使用:0次
名校
解题方法
7 . X、Y、Z、Q、W是原子序数依次增大的前四周期元素,其中X是宇宙中含量最多的元素;在同周期元素中,第一电离能数值比Y大的元素有2种;Z元素原子的价层电子排布是 ;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法错误的是
;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法错误的是
 ;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法错误的是
;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法错误的是| A.电负性:X<Y<Z | B.键角: |
C. 的阴阳离子比为 的阴阳离子比为 | D.W元素位于元素周期表的ds区 |
您最近半年使用:0次
2023-01-01更新
|
516次组卷
|
2卷引用:浙江省镇海中学2022-2023学年高三上学期12月模拟考试化学试题
名校
8 . A、B、C、D、E五种短周期元素。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上有3个未成对的电子;C元素在地壳中含量最高;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E的最外层电子数与其核外电子总数之比为3:8。
;E的最外层电子数与其核外电子总数之比为3:8。
(1)B的元素符号为_______ ,D元素在周期表中位置为_______ 。
(2)A、C形成的简单氢化物的键角顺序_______ (填化学式),并分析原因:_______ 。
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
(4)元素的非金属性C_______ (填“>”或“<”)E,并用化学原理证明(用化学方程式表示)_______ 。
 ;E的最外层电子数与其核外电子总数之比为3:8。
;E的最外层电子数与其核外电子总数之比为3:8。(1)B的元素符号为
(2)A、C形成的简单氢化物的键角顺序
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是
(4)元素的非金属性C
您最近半年使用:0次
解题方法
9 . X、Y、Z、W为原子序数依次增大的前四周期元素,基态原子中,X为元素周期表中半径最小的原子,Z是地壳中含量最多的元素,W原子的价电子排布为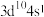 ,X、Y、Z、W形成的阳离子如图所示,下列说法正确的是
,X、Y、Z、W形成的阳离子如图所示,下列说法正确的是
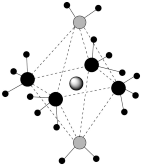
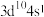 ,X、Y、Z、W形成的阳离子如图所示,下列说法正确的是
,X、Y、Z、W形成的阳离子如图所示,下列说法正确的是
| A.原子半径:Z>Y>X |
| B.氢化物的沸点:Z>Y |
| C.常温下可以用铁制容器盛装Y的最高价氧化物对应水化物的浓溶液 |
D.两种配体中的键角: |
您最近半年使用:0次
解题方法
10 . 铝是地壳中含量最高的金属,其单质和化合物具有广泛的应用价值。请回答下列问题:
(1)AlCl3易溶于水、四氯化碳等,熔融时生成可挥发的二聚物(Al2Cl6),结构如图所示:
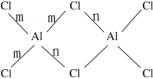
①基态氯原子价电子轨道表示式为_______ 。
②从键的形成角度分析m键和n键的区别_______ 。
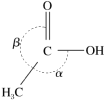
(2)LiAlH4是一种强还原剂,能将乙酸(结构如下图所示)直接还原成乙醇。CH3COOH CH3CH2OH
CH3CH2OH
①AlH 的空间构型是
的空间构型是________ 。
②CH3COOH分子中键角α______ β(填“>”、“=”或“<”),原因是________ 。
(3)铝和氮可形成一种具有四面体结构单元的高温结构陶瓷,其晶胞如图所示:
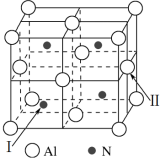
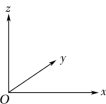
①晶胞中Al的配位数是___________ ,若该晶胞的参数为a pm,则该晶体的密度为___________ g·cm-3.(用NA表示阿伏加德罗常数的值)
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,如晶胞中I的分数坐标为( ,
, ,
, ),试写出晶胞中II的分数坐标
),试写出晶胞中II的分数坐标___________ 。
(1)AlCl3易溶于水、四氯化碳等,熔融时生成可挥发的二聚物(Al2Cl6),结构如图所示:

①基态氯原子价电子轨道表示式为
②从键的形成角度分析m键和n键的区别
(2)LiAlH4是一种强还原剂,能将乙酸(结构如下图所示)直接还原成乙醇。CH3COOH
 CH3CH2OH
CH3CH2OH
①AlH
 的空间构型是
的空间构型是②CH3COOH分子中键角α
(3)铝和氮可形成一种具有四面体结构单元的高温结构陶瓷,其晶胞如图所示:


①晶胞中Al的配位数是
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,如晶胞中I的分数坐标为(
 ,
, ,
, ),试写出晶胞中II的分数坐标
),试写出晶胞中II的分数坐标
您最近半年使用:0次



