名校
1 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)写出元素符号A:_______ ,B:_______ ,E_______ ,G:_______ 。
(2)C、D、E三种元素的原子半径由大到小的顺序为_______ (用元素符号表示)。
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:_______ ,_______ ,_______ 。
(4)已知元素A、B形成的 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为_______ 。
(5)G元素可形成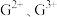 ,其中较稳定的是
,其中较稳定的是 ,试从核外电子排布的角度解释其原因:
,试从核外电子排布的角度解释其原因:_______ 。
(6)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是_______ 化合物(填“离子”或“共价”)。根据“对角线规则”,元素周期表中某些处于对角的元素,它们的化合物性质具有相似性,则M的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为_______ 。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 电离能数据(单位: ):738、1451、7733、10540、13630…… ):738、1451、7733、10540、13630…… |
| E | 基态原子最外层电子排布式为: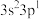 |
| F | 基态原子的最外层p轨道上2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 其中一种氧化物是有磁性的黑色固体 |
(2)C、D、E三种元素的原子半径由大到小的顺序为
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:
(4)已知元素A、B形成的
 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为(5)G元素可形成
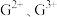 ,其中较稳定的是
,其中较稳定的是 ,试从核外电子排布的角度解释其原因:
,试从核外电子排布的角度解释其原因:(6)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
您最近一年使用:0次
名校
解题方法
2 . A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,相关信息如下表:
请用化学用语填空:
(1)A元素在元素周期表中的位置___________ ;C元素和F元素的电负性比较,较小的是___________ (填元素符号)。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的电子式为___________ ,B元素所形成的单质分子中σ键与π键数目之比为___________ 。
(3)F元素原子的价电子的轨道表示式是___________ ;G的高价阳离子的溶液与H单质反应的离子方程式为___________ ;元素X与元素E在周期表中呈对角线关系,且元素X的最高价氧化物的水化物也具有两性,试写出X元素的最高价氧化物的水化物与D元素的最高价氧化物的水化物反应的化学方程式___________ 。
| 元素 | 元素相关信息 |
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为 |
| F | 基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反 |
| G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
| H | 是我国使用最早的合金中的最主要元素 |
(1)A元素在元素周期表中的位置
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的电子式为
(3)F元素原子的价电子的轨道表示式是
您最近一年使用:0次
名校
解题方法
3 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)元素F简单离子的价电子排布式为___________ ;写出元素G在周期表中的位置___________ 。
(2)B与氢元素形成的简单气态氢化物的空间构型为___________ ,C与氢元素形成的简单气态氢化物的VSEPR模型为___________ 。
(3)C、D、E三种元素的简单离子半径由大到小的顺序为___________ (用元素符号表示)。
(4)已知元素A、B形成的 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为___________ 。
(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是___________ 化合物(填“离子”或“共价”);M的最高价氧化物对应的水化物与NaOH溶液反应的化学方程式为___________ 。
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 电离能数据(单位: ):738、1451、7733、10540、13630…… ):738、1451、7733、10540、13630…… |
| E | 基态原子最外层电子排布式为: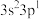 |
| F | 基态原子的最外层p轨道上2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 其中一种氧化物是有磁性的黑色固体 |
(2)B与氢元素形成的简单气态氢化物的空间构型为
(3)C、D、E三种元素的简单离子半径由大到小的顺序为
(4)已知元素A、B形成的
 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO
 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
名校
4 . 回答下列问题
(1)某届奥运会上,有个别运动员因服用兴奋剂被取消参赛资格.以下是其中检测出的两种兴奋剂的结构:___________ ,1molX与足量的氢气反应,最多消耗________ 
②1molY与足量NaOH溶液反应消耗_____________ mol NaOH,1molY与足量的饱和溴水反应,消耗_________ 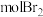 。
。
(2)短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素形成的化合物甲的结构为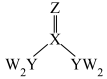 ,其中各原子的最外层均处于稳定结构。W与X、Y、Z均可形成电子数相等的分子,
,其中各原子的最外层均处于稳定结构。W与X、Y、Z均可形成电子数相等的分子, 常温常压下为常见的液体。
常温常压下为常见的液体。
①物质甲的1个分子中存在____________ 个 键
键
②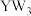 分子中的键角
分子中的键角___________ 120°(填“>”,“<”,“=”)
③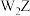 的稳定性
的稳定性__________ 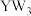 (填“>”,“<”,“=”)
(填“>”,“<”,“=”)
(1)某届奥运会上,有个别运动员因服用兴奋剂被取消参赛资格.以下是其中检测出的两种兴奋剂的结构:
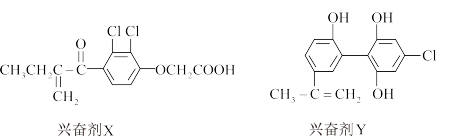

②1molY与足量NaOH溶液反应消耗
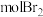 。
。(2)短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素形成的化合物甲的结构为
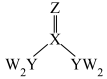 ,其中各原子的最外层均处于稳定结构。W与X、Y、Z均可形成电子数相等的分子,
,其中各原子的最外层均处于稳定结构。W与X、Y、Z均可形成电子数相等的分子, 常温常压下为常见的液体。
常温常压下为常见的液体。①物质甲的1个分子中存在
 键
键②
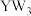 分子中的键角
分子中的键角③
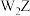 的稳定性
的稳定性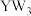 (填“>”,“<”,“=”)
(填“>”,“<”,“=”)
您最近一年使用:0次
名校
解题方法
5 . 现有五种元素,其中Y、Z、W为同周期主族元素,Q为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)Q位于第______ 族______ 区。
(2)离子ZW 的空间结构为:
的空间结构为:___________ ;化合物X2W的价层电子对互斥模型为___________ 。
(3)比较ZX 和ZX3的键角∠XZX的大小:ZX
和ZX3的键角∠XZX的大小:ZX
_____ (填“>”“=”或“<”)ZX3。
(4)化合物X3Y–Y≡Z中,Y元素原子的杂化形式有___________ ,该化合物中σ键和π键的个数之比为___________ 。
| X元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| Y元素基态原子的最外层中p能级的电子数等于前一能层电子 |
| Z元素基态原子的未成对电子数目是同周期最多的 |
| W元素基态原子最外能层的p能级中有一个轨道填充2个电子 |
| Q在周期表的第七列 |
(2)离子ZW
 的空间结构为:
的空间结构为:(3)比较ZX
 和ZX3的键角∠XZX的大小:ZX
和ZX3的键角∠XZX的大小:ZX
(4)化合物X3Y–Y≡Z中,Y元素原子的杂化形式有
您最近一年使用:0次
2023-03-14更新
|
110次组卷
|
2卷引用:山东省曹县第一中学2022-2023学年高二下学期2月月考化学试题
名校
6 . 联合国将2019年定为“国际化学元素周期表年”。元素周期表前四周期的元素a、b、c、d、e、f的原子序数依次增大。a、b、d的价电子层中未成对电子均只有1个,a的基态原子核外有3种不同能量的电子,b、d的单质均能与水剧烈反应,b-和d+核外电子数相差8,c的最外层电子数为其电子层数的2倍,补充维生素D可促进人体对元素e的吸收,f的价电子层中的未成对电子数为4.回答下列问题:
(1)a、b、c的电负性由小到大的顺序为___________ (用元素符号表示)。基态f原子的核外电子排布式为___________ 。
(2)ab3分子中心原子的杂化方式为___________ ,其键角为___________ 。
(3)c的简单氢化物与同族相邻两种元素所形成的简单氢化物沸点由高到低的顺序为___________ (用化学式表示),理由:___________ 。
(4)CO与f形成的f(CO)5常温下是一种浅黄色液体,f(CO)5的空间构型为___________ ,提供孤电子对的原子是___________ (填元素符号),CO分子中σ键与π键数目之比为___________ 。
(1)a、b、c的电负性由小到大的顺序为
(2)ab3分子中心原子的杂化方式为
(3)c的简单氢化物与同族相邻两种元素所形成的简单氢化物沸点由高到低的顺序为
(4)CO与f形成的f(CO)5常温下是一种浅黄色液体,f(CO)5的空间构型为
您最近一年使用:0次
7 . 化合物G是某化工生产中的重要中间体,其合成路线如下:
(注Me: Et:
Et: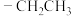 )
)
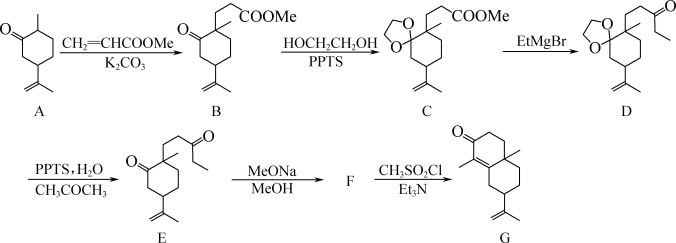
(1)A→B的反应类型为_______ 。
(2)1mol有机物B中所含π键的数目为_______ mol。
(3)E→F的反应类型为加成反应,则F的结构简式为_______ 。
(4)E的一种同分异构体同时满足下列条件,写出一种该同分异构体的结构简式:_______ 。
①能与 溶液发生显色反应;②有四种不同化学环境的氢原子。
溶液发生显色反应;②有四种不同化学环境的氢原子。
(5)已知: ,写出以
,写出以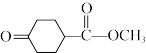 、
、 和
和 为原料制备
为原料制备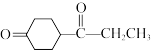 的合成路线流程图
的合成路线流程图_______ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
(注Me:
 Et:
Et: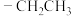 )
)
(1)A→B的反应类型为
(2)1mol有机物B中所含π键的数目为
(3)E→F的反应类型为加成反应,则F的结构简式为
(4)E的一种同分异构体同时满足下列条件,写出一种该同分异构体的结构简式:
①能与
 溶液发生显色反应;②有四种不同化学环境的氢原子。
溶液发生显色反应;②有四种不同化学环境的氢原子。(5)已知:
 ,写出以
,写出以 、
、 和
和 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
2022-11-24更新
|
313次组卷
|
2卷引用:江苏省百校联考2022-2023学年高二下学期5月第一次考试化学试题
8 . A、B、C、D、E是原子序数依次增大的短周期主族元素,已知基态A、E原子中有两个未成对电子,基态B、C、D原子中均有一个未成对电子。基态A原子中只有两种电子云轮廓不同的能级,且两种能级上的电子总数相等,E的单质能形成一种类似于金刚石结构的共价晶体。
(1)B、C的元素名称分别为_______ 、_______ 。
(2)B和E可组成一种五原子共价化合物,该化合物的电子式为_______ 。
(3)请写出能比较出A和B的非金属性强弱反应的化学方程式:_______ 。
(4)将D的单质加入C的最高价氧化物对应水化物的溶液中,产生的现象是_______ ,写出发生反应的化学方程式:_______ 。
(5)1 mol E的单质晶体中含有_______ molE-E键。
(1)B、C的元素名称分别为
(2)B和E可组成一种五原子共价化合物,该化合物的电子式为
(3)请写出能比较出A和B的非金属性强弱反应的化学方程式:
(4)将D的单质加入C的最高价氧化物对应水化物的溶液中,产生的现象是
(5)1 mol E的单质晶体中含有
您最近一年使用:0次
名校
9 . 化合物G是某化工生产中的重要中间体,其合成路线如下:
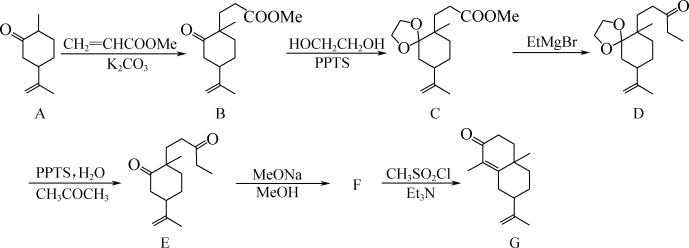
Me: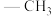 Et:
Et: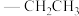
(1)1mol有机物B中所含π键的数目为_______ mol。
(2)D中含有_______ 个手性碳原子。
(3)E→F的反应类型为加成反应,则F的结构简式为_______ 。
(4)C的一种同分异构体同时满足下列条件,写出一种该同分异构体的结构简式:_______ 。
①能与 溶液发生显色反应。
溶液发生显色反应。
②有四种不同化学环境的氢原子。
(5)已知: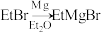 。写出以
。写出以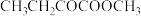 和
和 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图_______ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。

Me:
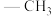 Et:
Et: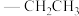
(1)1mol有机物B中所含π键的数目为
(2)D中含有
(3)E→F的反应类型为加成反应,则F的结构简式为
(4)C的一种同分异构体同时满足下列条件,写出一种该同分异构体的结构简式:
①能与
 溶液发生显色反应。
溶液发生显色反应。②有四种不同化学环境的氢原子。
(5)已知:
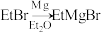 。写出以
。写出以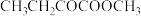 和
和 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
名校
10 . 现有五种元素,其中Y、Z、W为同周期主族元素,Q为第四周期元素,这五种元素的原子序数依次增大。请根据下列相关信息,回答问题。
(1)Q位于第_______ 族,它位于周期表的_______ 区。
(2)离子 的空间构型为:
的空间构型为:_______ ;化合物2W的价层电子对互斥模型为_______ 。
(3)比较 和
和 的键角
的键角 的大小:
的大小:
_______ (填“>”或“<”) ,请用价层电子对互斥理论解释:
,请用价层电子对互斥理论解释:_______ 。
(4)化合物 中,Y元素原子的杂化形式有
中,Y元素原子的杂化形式有_______ ,该化合物中σ键和π键的个数之比为_______ 。
| X元素的核外电子数和电子层数相等,也是宇宙中含量最丰富的元素 |
| Y元素基态原子的最外层中p能级的电子数等于前一能层中电子总数 |
| Z元素基态原子的未成对电子数目是同周期中最多的 |
| W元素基态原子最外能层的p能级中有一个轨道填充2个电子 |
| Q在周期表的第七列 |
(2)离子
 的空间构型为:
的空间构型为:(3)比较
 和
和 的键角
的键角 的大小:
的大小:
 ,请用价层电子对互斥理论解释:
,请用价层电子对互斥理论解释:(4)化合物
 中,Y元素原子的杂化形式有
中,Y元素原子的杂化形式有
您最近一年使用:0次



