1 . 钕铁硼磁铁是目前为止具有最强磁力的永久磁铁。生产钕铁硼磁铁的主要原材料有稀土金属钕、高纯铁、铝、硼等。回答下列问题:
(1)钕(Nd)为60号元素,在周期表中位于第___________ 周期。基态硼原子中占据最高能级的电子,电子云轮廓图形状为___________ 。Fe2+的价电子排布图___________
(2)铜能与类卤素(CN)2反应生成Cu(CN)2,1 mol (CN)2分子中含有π键的数目为___________ 。
(3)Cu2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]SO4中,N、O、S三种元素的第一电离能从大到小的顺序为___________ 。
②[Cu(NH3)4]SO4中,不存在的化学键的类型有___________ (填选项)。
A.离子键 B.配位键 C.非极性键 D.极性键
③[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为___________ 。
(1)钕(Nd)为60号元素,在周期表中位于第
(2)铜能与类卤素(CN)2反应生成Cu(CN)2,1 mol (CN)2分子中含有π键的数目为
(3)Cu2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]SO4中,N、O、S三种元素的第一电离能从大到小的顺序为
②[Cu(NH3)4]SO4中,不存在的化学键的类型有
A.离子键 B.配位键 C.非极性键 D.极性键
③[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
您最近一年使用:0次
解题方法
2 . 近年来,我国工程建设自主创新能力实现大跨越,尤其在新材料研究方面有重大突破,回答下列问题:
(1)钛是一种新兴的结构材料,比钢轻、比铝硬。基态钛原子的价电子排布式为_____ , 与钛同周期的元素中,基态原子的未成对电子数与钛相间的有_____ 种;
(2)铁能与三氮唑(结构见图甲)形成多种配合物。
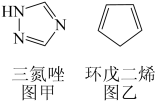
①l mol三氮唑中所含σ键的数目为_____ mol; 碳原子杂化方式是____ ;
②三氮唑的沸点为260°C,与之结构相似且相对分子质量接近的环戊二烯(结构见图乙)的沸点为42.5℃,前者沸点较高的原因是_____ 。
(3)碳化钨是耐高温耐磨材料。图丙为碳化钨晶体的部分结构,碳原子嵌入金属的晶格间隙,并不破坏原有金属的晶格,形成填隙化合物。
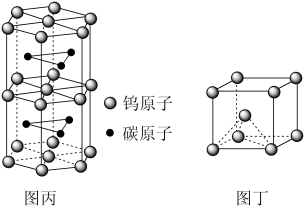
①在该结构中,每个钨原子周围距离其最近的碳原子有_____ 个:
②假设该部分晶体的体积为Vcm3,碳化钨的摩尔质量为M g•mol-1,密度为d g•cm-3,则阿伏加德罗常数的值NA用上述数据表示为_____ 。
③金属镁的晶体结构与碳化钨相似,金属镁的晶胞可用图丁表示,已知镁原子的半径为r pm,晶胞高为h pm,求晶胞中镁原子的空间利用率_______ (用化简后含字时π、r和h的代数式表示)
(1)钛是一种新兴的结构材料,比钢轻、比铝硬。基态钛原子的价电子排布式为
(2)铁能与三氮唑(结构见图甲)形成多种配合物。

①l mol三氮唑中所含σ键的数目为
②三氮唑的沸点为260°C,与之结构相似且相对分子质量接近的环戊二烯(结构见图乙)的沸点为42.5℃,前者沸点较高的原因是
(3)碳化钨是耐高温耐磨材料。图丙为碳化钨晶体的部分结构,碳原子嵌入金属的晶格间隙,并不破坏原有金属的晶格,形成填隙化合物。

①在该结构中,每个钨原子周围距离其最近的碳原子有
②假设该部分晶体的体积为Vcm3,碳化钨的摩尔质量为M g•mol-1,密度为d g•cm-3,则阿伏加德罗常数的值NA用上述数据表示为
③金属镁的晶体结构与碳化钨相似,金属镁的晶胞可用图丁表示,已知镁原子的半径为r pm,晶胞高为h pm,求晶胞中镁原子的空间利用率
您最近一年使用:0次
2021-03-14更新
|
437次组卷
|
2卷引用:吉林省长春市普通高中2021届高三质量监测(二)(二模)理综化学试题
3 . Li、Fe、As、Zn等均为重要的合金材料,回答下列问题:
(1)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因是______ 。
(2)KSCN和K4[Fe(CN)6]常用于检验Fe3+,SCN-的立体构型为______ ,K4[Fe(CN)6]中所含元素第一电离能由大到小的顺序为______ 。Fe与Co既在同一周期,又在同一族,Co3+通常易形成六配位的配合物,已知CoCl3·6H2O有多种结构,若取1molCoCl3·6H2O溶解于水后滴加足量的硝酸银溶液,能够形成2mol沉淀,则CoCl3·6H2O中配离子为______ 。
(3)H3AsO3的酸性弱于H3AsO4的原因为______ 。含砷有机物“对氨基苯胂酸”的结构简式如图,As原子轨道杂化类型为______ ,1mol对氨基苯胂酸含σ键数目为______ 。

(4)锌和镉位于同副族,而锌与铜相邻。现有4种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10。失去1个电子需要的能量由大到小排序是______ (填字母)。
A.④②①③ B.④②③① C.①②④③ D.①④③②
若Zn基态原子将次外层1个d电子激发进入最外层的np能级,则该激发态原子的价电子排布式为______ 。
(1)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因是
(2)KSCN和K4[Fe(CN)6]常用于检验Fe3+,SCN-的立体构型为
(3)H3AsO3的酸性弱于H3AsO4的原因为

(4)锌和镉位于同副族,而锌与铜相邻。现有4种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10。失去1个电子需要的能量由大到小排序是
A.④②①③ B.④②③① C.①②④③ D.①④③②
若Zn基态原子将次外层1个d电子激发进入最外层的np能级,则该激发态原子的价电子排布式为
您最近一年使用:0次



