1 . NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,33.6LSO3和NO2的混合物中含有分子的数目为1.5NA |
| B.14g硅单质中含硅硅单键的数目为1NA |
| C.2.3gNa与氧气完全反应,反应中转移的电子数介于0.1NA到0.2NA之间 |
| D.常温下,1 L pH=1的H2SO4溶液中H+的数目为0.2NA |
您最近一年使用:0次
解题方法
2 . 锌及其化合物在工农业生产及科学研究中具有广泛的用途。回答下列问题:
(1)Zn位于元素周期表的___________ 区,基态Zn2+的核外电子排布式为___________ 。
(2)氨基酸锌是研究最早和使用最广泛的第三代锌添加剂,该添加剂具有优良的营养功能。如图1是氨基酸锌的结构简式。
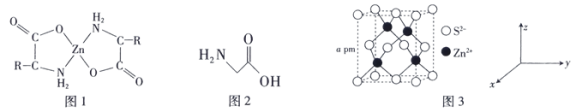
①组成氨基酸锌的C、N、O的电负性由大到小的顺序是___________ 。
②氨基酸锌的Zn2+形成配位键,其中提供空轨道的原子是___________ 。
③最简单的氨基酸是甘氨酸(结构简式如图2),其结构中π键与σ键的数量比为___________ 。
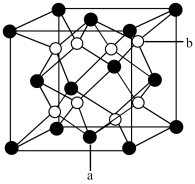
(3)ZnS可用于制白色颜料、玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS的晶胞如图3所示。
①上图中 的坐标有
的坐标有 、
、 ,与
,与 距离最近的
距离最近的 还有
还有___________ (填坐标)。
②Zn2+占据___________ (填“八面体”或“四面体”)空隙,空隙利用率为___________ %。
③ZnS的密度为___________  。
。
(1)Zn位于元素周期表的
(2)氨基酸锌是研究最早和使用最广泛的第三代锌添加剂,该添加剂具有优良的营养功能。如图1是氨基酸锌的结构简式。

①组成氨基酸锌的C、N、O的电负性由大到小的顺序是
②氨基酸锌的Zn2+形成配位键,其中提供空轨道的原子是
③最简单的氨基酸是甘氨酸(结构简式如图2),其结构中π键与σ键的数量比为
(3)ZnS可用于制白色颜料、玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS的晶胞如图3所示。
①上图中
 的坐标有
的坐标有 、
、 ,与
,与 距离最近的
距离最近的 还有
还有②Zn2+占据
③ZnS的密度为
 。
。
您最近一年使用:0次
2021-07-05更新
|
127次组卷
|
2卷引用:江西省赣抚吉名校2022届高三上学期8月联合考试化学试题
3 . 2019年诺贝尔化学奖授予约翰·B·古迪纳夫、M·斯坦利·威廷汉、吉野彰等三位科学家,以表彰他们在锂电池研究作出的卓越贡献。常用的锂电池用镍钴锰酸锂Li(NiCoMn)O2或磷酸铁锂(LiFePO4)等为正极材料。请回答下列问题:
(1)Ni在元素周期表的位置是______ 区(填分区),基态Fe原子的价电子排布式为______ 。
(2)1 mol配合物[Co(NH3)4Cl2]Cl含σ键数目为______ NA。
(3)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是______ ,HPO3中心原子的杂化方式是______ ,写出与PO 互为等电子体的离子
互为等电子体的离子______ (写离子符号,任写两个)。
(4)硫化锂 Li2S 的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若a处微粒的坐标是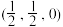 则b处微粒的坐标是
则b处微粒的坐标是______ ;S2-的配位数是______ ;若硫化锂晶体的密度为ρ g·cm-3,则Li+与S2- 的最短距离是______ nm(用含ρ、NA的计算式表示)。
(1)Ni在元素周期表的位置是
(2)1 mol配合物[Co(NH3)4Cl2]Cl含σ键数目为
(3)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是
 互为等电子体的离子
互为等电子体的离子(4)硫化锂 Li2S 的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若a处微粒的坐标是
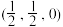 则b处微粒的坐标是
则b处微粒的坐标是
您最近一年使用:0次
解题方法
4 . S、Se 、N、Fe等元素及其化合物在科学研究和工业生产中具有重要的作用。
(1)臭鼬排放的臭气主要成分为3﹣MBT,键线式如图所示:

0.1mol 3﹣MBT中含有σ键数目为___________ (NA为阿伏加德罗常数的值)。3﹣MBT的沸点低于(CH3)2C=CHCH2OH,主要原因是___________ 。
(2)2020年12月17日,采撷月壤的嫦娥五号荣耀归来。嫦娥五号探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质。硒为第四周期第VIA族元素,其氧化物有SeO2和SeO3两种,SeO3分子的立体构型为___________ ,与其互为等电子体的阴离子为 ___________ (举一例)。
(3)铁氰化钾,化学式为K3[Fe(CN)6],主要应用于制药、电镀、造纸、钢铁生产等工业,其煅烧分解生成KCN、FeC2、N2、(CN)2等物质。
①K3[Fe(CN)6]中所涉及的各元素的第一电离能由大到小的顺序为___________ 。
②(CN)2分子中存在碳碳键,C原子的杂化轨道类型为___________ 。
③下列选项是部分同学画的基态氮原子的核外电子排布图,其中违背泡利原理的是___________ (填序号,下同),违背洪特规则的是___________ 。
A.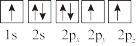 B.
B. 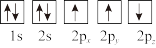 C.
C. 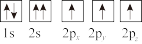
(4)如图是金属铁晶体中的一个晶胞。
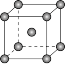
①该晶体中原子总体积占晶体体积的比值为___________ (用含π的最简代数式表示)。
②铁原子的半径为rpm,其晶体密度为___________ g•cm﹣3(用含有r、NA的最简代数式表示)。
(1)臭鼬排放的臭气主要成分为3﹣MBT,键线式如图所示:

0.1mol 3﹣MBT中含有σ键数目为
(2)2020年12月17日,采撷月壤的嫦娥五号荣耀归来。嫦娥五号探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质。硒为第四周期第VIA族元素,其氧化物有SeO2和SeO3两种,SeO3分子的立体构型为
(3)铁氰化钾,化学式为K3[Fe(CN)6],主要应用于制药、电镀、造纸、钢铁生产等工业,其煅烧分解生成KCN、FeC2、N2、(CN)2等物质。
①K3[Fe(CN)6]中所涉及的各元素的第一电离能由大到小的顺序为
②(CN)2分子中存在碳碳键,C原子的杂化轨道类型为
③下列选项是部分同学画的基态氮原子的核外电子排布图,其中违背泡利原理的是
A.
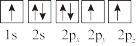 B.
B. 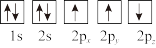 C.
C. 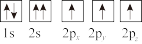
(4)如图是金属铁晶体中的一个晶胞。

①该晶体中原子总体积占晶体体积的比值为
②铁原子的半径为rpm,其晶体密度为
您最近一年使用:0次



