1 . 下列元素或化合物的性质变化顺序不正确的是
A.第一电离能: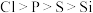 |
B.电负性: |
C.价层电子对互斥理论中, 键电子对数计入中心原子的价层电子对数 键电子对数计入中心原子的价层电子对数 |
| D.第四周期元素中,锰原子价电子层中未成对电子数最多 |
您最近一年使用:0次
名校
解题方法
2 . 下列说法正确的是
A. 分子的VSEPR模型: 分子的VSEPR模型: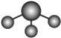 |
B.甲基是推电子基团,所以结合氢离子的能力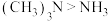 |
C.乙二胺( )的沸点比三甲胺 )的沸点比三甲胺 高的原因是乙二胺存在分子间氢键,三甲胺存在分子内氢键 高的原因是乙二胺存在分子间氢键,三甲胺存在分子内氢键 |
D.由铝原子核形成的下列三种微粒:a.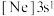 、b. 、b.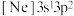 、c. 、c.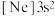 ,再失去一个电子所需最低能量由大到小的顺序是:c>a>b ,再失去一个电子所需最低能量由大到小的顺序是:c>a>b |
您最近一年使用:0次
名校
3 . 乙炔水化法、乙烯氧化法是工业上制备乙醛的两个重要方法,反应原理分别为:
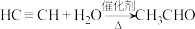 ,
,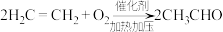 。以下叙述正确的是
。以下叙述正确的是
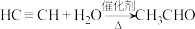 ,
,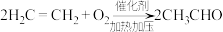 。以下叙述正确的是
。以下叙述正确的是A. 的电子式为 的电子式为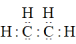 |
| B.根据价层电子互斥模型,18g水的中心原子含有2mol孤电子对 |
C.乙烯氧化法中,生成0.1mol乙醛时,转移的电子数约为 |
D.标准状况下,11.2L乙醛中含有π键的数目约为 |
您最近一年使用:0次
名校
4 . 乙炔水化法、乙烯氧化法是工业上制备乙醛的两个重要方法,反应原理分别为: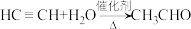 ,
,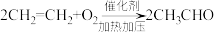 。以下叙述错误的是
。以下叙述错误的是
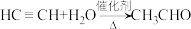 ,
,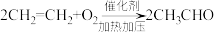 。以下叙述错误的是
。以下叙述错误的是A. 的电子式 的电子式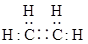 |
B.根据价层电子互斥模型,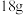 水的中心原子含有 水的中心原子含有 孤电子对 孤电子对 |
C.乙烯氧化法中,生成 乙醛时,转移的电子数约为 乙醛时,转移的电子数约为 |
D.标准状况下, 乙醛中含有 乙醛中含有 键的数目约为 键的数目约为 |
您最近一年使用:0次
名校
5 . 烯烃催化制备醛的反应机理如下,下列说法错误的是
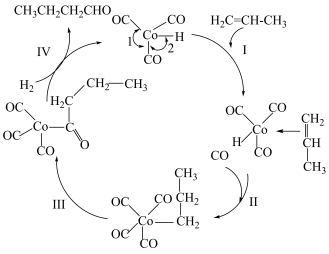

A.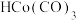 反应前后质量和化学性质没有发生变化 反应前后质量和化学性质没有发生变化 |
| B.步骤Ⅰ中钴的配位数和化合价都发生了变化 |
C.键角: |
D.总反应式为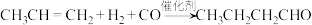 |
您最近一年使用:0次
解题方法
6 . 下列说法正确的是
| A.对Na原子光谱呈现双线的解释是电子自旋 |
| B.价层电子对互斥理论中,π键电子对数可以计入中心原子的价层电子对数 |
| C.含有极性键的分子一定是极性分子 |
| D.NaCl熔化和干冰升华克服的作用力类型相同 |
您最近一年使用:0次
7 . I.可以由下列反应合成三聚氰胺:CaO+3C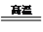 CaC2+CO, CaC2+N2
CaC2+CO, CaC2+N2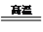 CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和_____ (填化学式), 由此可以推知CN22-的空间构型为_______ 。
(2)三聚氰胺(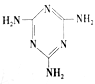 )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(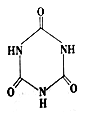 )
)
后,三聚氰酸与三聚氰胺分子相互之间通过______ 结合,在肾脏内易形成结石。
II.碳元素形成的单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔触的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图所示,该物质的化学式为_________ 。
 CaC2+CO, CaC2+N2
CaC2+CO, CaC2+N2 CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。(1)CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和
(2)三聚氰胺(
 )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸( )
)后,三聚氰酸与三聚氰胺分子相互之间通过
II.碳元素形成的单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔触的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图所示,该物质的化学式为

您最近一年使用:0次
名校
解题方法
8 . 下列说法不正确的是( )
| A.苯分子中每个碳原子的sp2杂化轨道中的其中一个形成大π键 |
| B.Na3N与NaH均为离子化合物,都能与水反应放出气体,且与水反应所得溶液均能使酚酞溶液变红 |
| C.配离子[Cu(En)2]2+(En是乙二胺的简写)中的配位原子是C原子,配位数为4 |
| D.H2O中的孤对电子数比H3O+的多,故H2O的键角比H3O+的键角小 |
您最近一年使用:0次



