1 . 下列元素或化合物的性质变化顺序不正确的是
A.第一电离能: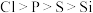 |
B.电负性: |
C.价层电子对互斥理论中, 键电子对数计入中心原子的价层电子对数 键电子对数计入中心原子的价层电子对数 |
| D.第四周期元素中,锰原子价电子层中未成对电子数最多 |
您最近半年使用:0次
名校
解题方法
2 . 下列各组微粒的中心原子杂化类型相同但微粒的空间结构不同的是
A. 、 、 | B. 、 、 | C. 、 、 | D. 、 、 |
您最近半年使用:0次
名校
3 . 乙炔水化法、乙烯氧化法是工业上制备乙醛的两个重要方法,反应原理分别为: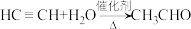 ,
,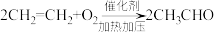 。以下叙述错误的是
。以下叙述错误的是
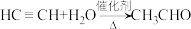 ,
,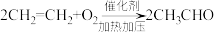 。以下叙述错误的是
。以下叙述错误的是A. 的电子式 的电子式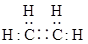 |
B.根据价层电子互斥模型,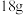 水的中心原子含有 水的中心原子含有 孤电子对 孤电子对 |
C.乙烯氧化法中,生成 乙醛时,转移的电子数约为 乙醛时,转移的电子数约为 |
D.标准状况下, 乙醛中含有 乙醛中含有 键的数目约为 键的数目约为 |
您最近半年使用:0次
名校
4 . 为有效缓解“碳达峰”,一种利用有机胺协助CO2氢化还原为CH3OH的过程如下,下列说法正确的是
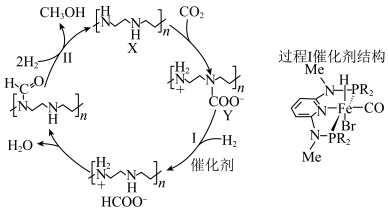

| A.过程Ⅱ中涉及非极性键的断裂与生成 |
| B.化合物X和Y中N原子的杂化方式不同 |
| C.催化剂中P形成配位键后R-P-R键角变小 |
D.该过程的总反应方程式为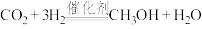 |
您最近半年使用:0次
名校
5 . 前四周期元素X、Y、Z、W原子序数依次增大,X和Z同主族,基态Y原子核外电子的运动状态有9种,基态Z原子4p能级上有三个单电子,常温下W2是一种深红棕色液体。回答下列问题:
(1)基态W原子的价电子排布式为_______ ,基态X、Z原子核外电子的空间运动状态数之比为_______ 。
(2)同周期第一电离能小于X的元素有_______ 种。
(3)键角大小:XY3_______ ZY3(填“>”“=”或“<”,下同),原子半径大小:W_______ Z。
(4)ZY5中Z的价层电子对数为_______ 。
(1)基态W原子的价电子排布式为
(2)同周期第一电离能小于X的元素有
(3)键角大小:XY3
(4)ZY5中Z的价层电子对数为
您最近半年使用:0次
名校
解题方法
6 . 下列说法正确的是
A. 分子的VSEPR模型: 分子的VSEPR模型: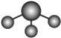 |
B.甲基是推电子基团,所以结合氢离子的能力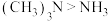 |
C.乙二胺( )的沸点比三甲胺 )的沸点比三甲胺 高的原因是乙二胺存在分子间氢键,三甲胺存在分子内氢键 高的原因是乙二胺存在分子间氢键,三甲胺存在分子内氢键 |
D.由铝原子核形成的下列三种微粒:a.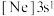 、b. 、b.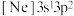 、c. 、c.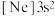 ,再失去一个电子所需最低能量由大到小的顺序是:c>a>b ,再失去一个电子所需最低能量由大到小的顺序是:c>a>b |
您最近半年使用:0次
名校
解题方法
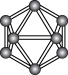
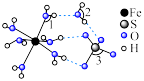
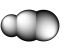
7 . 观察下列模型并结合信息,判断有关说法错误的是
| 晶体硼结构单元(有12个B原子) |  |  分子 分子 | HCN | |
| 结构模型示意图 |
|
|
|
|
A.晶体硼的结构单元中含有30个 键,含20个正三角形 键,含20个正三角形 |
B. 结构中键角1、2、3由大到小的顺序:3>1>2 结构中键角1、2、3由大到小的顺序:3>1>2 |
C.固态硫 中S原子为 中S原子为 杂化 杂化 |
D. 的结构式为 的结构式为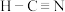 |
您最近半年使用:0次
2024-03-30更新
|
1030次组卷
|
2卷引用:山东省实验中学2023-2024学年高三(一模)调研考试化学试题
解题方法
8 . 下列关于 、
、 和
和 的说法正确的是
的说法正确的是
A. 为分子晶体 为分子晶体 | B. 为非极性分子 为非极性分子 |
C. 的VSEPR构型为V形 的VSEPR构型为V形 | D.基态Cl原子的核外电子有17种空间运动状态 |
您最近半年使用:0次
9 . 用价电子对互斥(VSEPR)理论可以预测许多分子或离子的空间结构,有时也能用来推测键角大小,下列判断正确的是
| A.SO2、CS2、HI都是直线形分子 |
| B.BF3键角为120°,SnF2键角大于120° |
| C.COCl2、BF3、SO3都是平面三角形分子 |
| D.PCl3、NH3、PCl5都是三角锥形分子 |
您最近半年使用:0次
名校
解题方法
10 . 物质的光学性质在科研中有重要的用途。回答下列问题:
Ⅰ.一种比率光声探针M与Cu2+配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:___________ ,M中键角F-B-F___________  中键角F-B-F(填“>”、“<”或“=”);基态
中键角F-B-F(填“>”、“<”或“=”);基态 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为___________ 。
(2)均为平面结构的吡咯(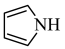 )和吡啶(
)和吡啶(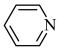 )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为___________ ,原因是___________ 。
Ⅱ.铪(Hf)的卤化物八面体离子是构建卤化物钙钛矿的基本发光单元,其构建的某晶胞结构如图所示。 的配位数为
的配位数为___________ ,阴离子形成的八面体空隙有___________ 个。
(4)该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Hf-Hf最近距离为
,则Hf-Hf最近距离为___________ nm。
Ⅰ.一种比率光声探针M与Cu2+配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
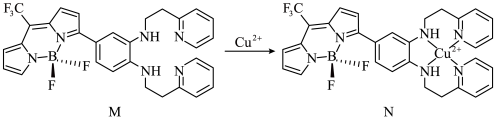
 中键角F-B-F(填“>”、“<”或“=”);基态
中键角F-B-F(填“>”、“<”或“=”);基态 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为(2)均为平面结构的吡咯(
 )和吡啶(
)和吡啶( )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为Ⅱ.铪(Hf)的卤化物八面体离子是构建卤化物钙钛矿的基本发光单元,其构建的某晶胞结构如图所示。
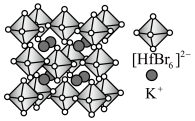
 的配位数为
的配位数为(4)该晶体的密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Hf-Hf最近距离为
,则Hf-Hf最近距离为
您最近半年使用:0次
2024-03-14更新
|
950次组卷
|
4卷引用:山东省烟台市2024届高三一模化学试题
山东省烟台市2024届高三一模化学试题2024届山东省高三下学期第一次练兵考试一模化学试题山东省德州市2023-2024学年高三下学期一模考试化学试题(已下线)化学(山东卷03)-2024年高考押题预测卷