名校
解题方法
1 . 下列有关物质结构与性质说法正确的是
A.酸性: |
B.沸点: |
C.键角: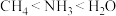 |
D.熔点:对硝基苯酚>邻硝基苯酚(硝基为 ) ) |
您最近一年使用:0次
2023-11-17更新
|
272次组卷
|
2卷引用:2023—2024学年高二上学期化学期末考试模拟试题(一)
名校
解题方法
2 . 回答下列问题:
(1)根据价层电子对互斥理论,当价层电子对数为5时,轨道形状为三角双锥形,孤电子对数不同则分子空间结构不同,孤电子对数为1、2、3时,对应的分子或离子空间结构分别为变形四面体、 形、直线形,则
形、直线形,则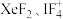 的空间构型分别为
的空间构型分别为_______ 、_______ 。
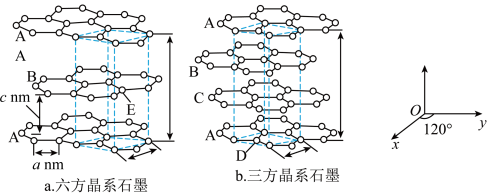
(2)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图a所示,图中用虚线标出了石墨的一个六方晶胞。若按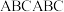 方式堆积而成,则如图
方式堆积而成,则如图 所示,图中用虚线标出了石墨的一个三方晶胞。
所示,图中用虚线标出了石墨的一个三方晶胞。 原子的分数坐标为
原子的分数坐标为_______ 。该六方石墨晶体的密度为_______  。
。
配合物在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂的研制、自组装超分子等方面有广泛的应用。回答下列问题:
(3)茜草中的茜素与 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。
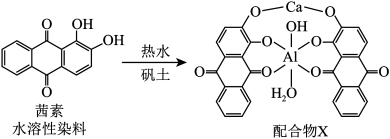
配合物 中
中 的配体除
的配体除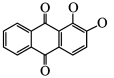 外还有
外还有_______ ,茜素水溶性较好的主要原因是_______ 。
(4)向 溶液中滴加
溶液中滴加 溶液后,经提纯、结晶可得到
溶液后,经提纯、结晶可得到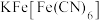 普鲁士蓝蓝色晶体。实验表明,
普鲁士蓝蓝色晶体。实验表明, 通过配位键构成了晶体的骨架。其局部结构如图1,记为I型立方结构。将I型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为II型立方结构,下层左后的小立方体
通过配位键构成了晶体的骨架。其局部结构如图1,记为I型立方结构。将I型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为II型立方结构,下层左后的小立方体 未标出)。
未标出)。
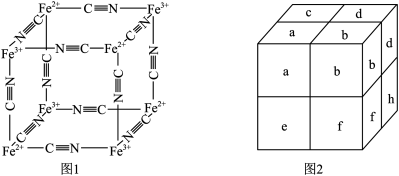
①可溶性氧化物(如 )有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是
)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是_______ 。
②若 位于II型立方结构的棱心和体心上,则
位于II型立方结构的棱心和体心上,则 位于II型立方结构的
位于II型立方结构的_______ 上;若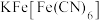 的摩尔质量为
的摩尔质量为 ,该蓝色晶体密度为
,该蓝色晶体密度为 ,II型立方结构的边长为
,II型立方结构的边长为 ,则阿伏加德罗常数的值可表示为
,则阿伏加德罗常数的值可表示为_______ 。
(1)根据价层电子对互斥理论,当价层电子对数为5时,轨道形状为三角双锥形,孤电子对数不同则分子空间结构不同,孤电子对数为1、2、3时,对应的分子或离子空间结构分别为变形四面体、
 形、直线形,则
形、直线形,则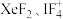 的空间构型分别为
的空间构型分别为(2)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图a所示,图中用虚线标出了石墨的一个六方晶胞。若按
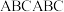 方式堆积而成,则如图
方式堆积而成,则如图 所示,图中用虚线标出了石墨的一个三方晶胞。
所示,图中用虚线标出了石墨的一个三方晶胞。 原子的分数坐标为
原子的分数坐标为 。
。
配合物在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂的研制、自组装超分子等方面有广泛的应用。回答下列问题:
(3)茜草中的茜素与
 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。
配合物
 中
中 的配体除
的配体除 外还有
外还有(4)向
 溶液中滴加
溶液中滴加 溶液后,经提纯、结晶可得到
溶液后,经提纯、结晶可得到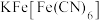 普鲁士蓝蓝色晶体。实验表明,
普鲁士蓝蓝色晶体。实验表明, 通过配位键构成了晶体的骨架。其局部结构如图1,记为I型立方结构。将I型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为II型立方结构,下层左后的小立方体
通过配位键构成了晶体的骨架。其局部结构如图1,记为I型立方结构。将I型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为II型立方结构,下层左后的小立方体 未标出)。
未标出)。
①可溶性氧化物(如
 )有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是
)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是②若
 位于II型立方结构的棱心和体心上,则
位于II型立方结构的棱心和体心上,则 位于II型立方结构的
位于II型立方结构的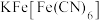 的摩尔质量为
的摩尔质量为 ,该蓝色晶体密度为
,该蓝色晶体密度为 ,II型立方结构的边长为
,II型立方结构的边长为 ,则阿伏加德罗常数的值可表示为
,则阿伏加德罗常数的值可表示为
您最近一年使用:0次
2023-11-04更新
|
350次组卷
|
2卷引用:山东省实验中学2024届高三上学期10月一诊考试化学试题
名校
解题方法
3 . 氮(N)形成的单质及它形成的化合物有重要的研究和应用价值,回答下列问题:
(1)已知NO 与CO2互为等电子体,NO
与CO2互为等电子体,NO 的结构式为
的结构式为_______ ,中心原子N的杂化方式为_______ 。
(2)NH4BF4(四氟硼酸铵)可用作铝或铜的焊接助熔剂,能腐蚀玻璃,有重要的化工用途。下列说法正确的是________ 。
(3)向硫酸铜溶液中通入过量氨气,得到深蓝色溶液,生成配合物[Cu(NH3)4]SO4,其中1mol阳离子[Cu(NH3)4]2+中含有σ键数目为________ 。向该深蓝色溶液中加入乙醇,得到深蓝色晶体,该深蓝色晶体为________ (填化学式)。
(4)请从结构角度解释HNO3的酸性比HNO2强的原因________ 。
(1)已知NO
 与CO2互为等电子体,NO
与CO2互为等电子体,NO 的结构式为
的结构式为(2)NH4BF4(四氟硼酸铵)可用作铝或铜的焊接助熔剂,能腐蚀玻璃,有重要的化工用途。下列说法正确的是
| A.核素15N的中子数为7 | B.F元素位于元素周期表p区 |
C.BF 的空间构型为正四面体形 的空间构型为正四面体形 | D.NH4BF4中存在离子键、共价键、氢键和范德华力 |
(4)请从结构角度解释HNO3的酸性比HNO2强的原因
您最近一年使用:0次
4 . 下列分子属于极性分子的是
| A.SiCl4 | B.PCl5 | C.OF2 | D.P4 |
您最近一年使用:0次
解题方法
5 . 下列有关化学用语表述错误的是
A. 的电子式: 的电子式: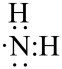 |
B.氮化硅与金刚石结构相似,其分子式为: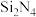 |
C. 的VSEPR模型: 的VSEPR模型: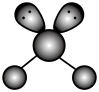 |
D.氮化镁的电子式为: |
您最近一年使用:0次
名校
解题方法
6 . 下列分类正确的是
A.VSEPR模型相同: 和 和 | B.晶体类型相同:石英和干冰 |
C.极性分子: 和 和 | D.基态原子价层 相同:Cr和Cu 相同:Cr和Cu |
您最近一年使用:0次
2023-07-22更新
|
202次组卷
|
2卷引用:山东省德州市夏津县第一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
7 . 我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、P、Ni、Fe 等元素。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________ (填标号,下同),用光谱仪可捕捉到发射光谱的是___________ 。___________ 。
(3)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所示。___________ 。
②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为___________ 。
③立方相氮化硼晶胞边长为apm, NA代表阿伏加德罗常数的值,则该晶体的密度为___________ g·cm-3。
(4)FeSO4·7H2O的结构如图所示,FeSO4·7H2O中∠1、∠2、∠3由大到小的顺序是___________ 。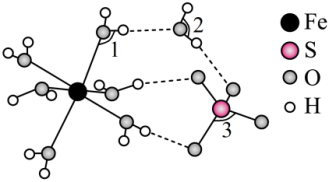
(5)镍的某种氧化物常用作催化剂,其晶胞有如图结构特征:镍离子形成面心立方结构,氧离子填充在镍离子构成的八面体空隙中,填充率为100%。
①从该晶胞中能分割出来的结构图有___________ (填标号)。___________ 个,该距离为___________ pm(用含ρ和NA的代数式表示)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.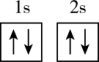 B.
B.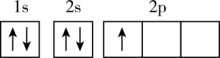 C.
C.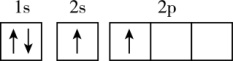 D.
D.
(3)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所示。

②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为
③立方相氮化硼晶胞边长为apm, NA代表阿伏加德罗常数的值,则该晶体的密度为
(4)FeSO4·7H2O的结构如图所示,FeSO4·7H2O中∠1、∠2、∠3由大到小的顺序是

(5)镍的某种氧化物常用作催化剂,其晶胞有如图结构特征:镍离子形成面心立方结构,氧离子填充在镍离子构成的八面体空隙中,填充率为100%。
①从该晶胞中能分割出来的结构图有
a.  b.
b.  c.
c. d.
d. 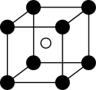 e.
e.
您最近一年使用:0次
2023-07-21更新
|
339次组卷
|
3卷引用:山东省青岛市第二中学2022-2023学年高二5月月考化学试题
解题方法
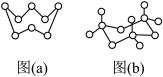
8 . 硫及其化合物用途很广,图(a)为 的结构,图(b)为固体
的结构,图(b)为固体 中存在的三聚分子。下列说法不正确的是
中存在的三聚分子。下列说法不正确的是
 的结构,图(b)为固体
的结构,图(b)为固体 中存在的三聚分子。下列说法不正确的是
中存在的三聚分子。下列说法不正确的是
A. 的熔、沸点比 的熔、沸点比 的熔、沸点高很多 的熔、沸点高很多 |
B. 分子的空间构型为平面三角形 分子的空间构型为平面三角形 |
C.图(a)和图(b)分子中S原子的杂化轨道类型均为 |
| D.图(a)和图(b)均存在大π键 |
您最近一年使用:0次
解题方法
9 . 下列化学用语错误的是
A. 的电子式: 的电子式: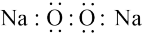 |
B. 的价层电子对互斥理论模型: 的价层电子对互斥理论模型: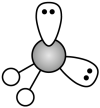 |
C.基态C原子的价层电子轨道表示式: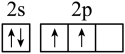 |
D.用原子轨道描述氯化氢分子中化学键的形成: |
您最近一年使用:0次
解题方法
10 . 下列有关化学用语正确的是
A.np能级的原子轨道图: |
B.H2O的VSEPR模型: |
C.HF分子间的氢键: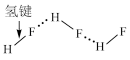 |
D.激发态的B原子轨道表示式: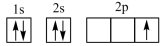 |
您最近一年使用:0次



