名校
1 . 卤素单质及其化合物在工农业生产中有着广泛的应用。回答下列问题:
(1)类卤素 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):
①硫氰酸和异硫氰酸分子中 键和
键和 键个数之比
键个数之比___________ (填“相等”或“不相等”)。
②异硫氰酸中N的杂化轨道类型是___________ 。
③硫氰酸的电子式为___________ 。
(2) 的VSEPR模型是
的VSEPR模型是___________ , 的中心原子的价层电子对数是
的中心原子的价层电子对数是___________ 。
(3)键角:
___________ (填“>”“<”或“=”) ,判断的理由为
,判断的理由为___________ 。
(4)酸性:三氟乙酸( )
)___________ (填“>”或“<”) ,判断的理由为
,判断的理由为___________ 。
(5) 与水反应的化学方程式为
与水反应的化学方程式为___________ (该反应为非氧化还原反应)。
(1)类卤素
 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):①硫氰酸和异硫氰酸分子中
 键和
键和 键个数之比
键个数之比②异硫氰酸中N的杂化轨道类型是
③硫氰酸的电子式为
(2)
 的VSEPR模型是
的VSEPR模型是 的中心原子的价层电子对数是
的中心原子的价层电子对数是(3)键角:

 ,判断的理由为
,判断的理由为(4)酸性:三氟乙酸(
 )
) ,判断的理由为
,判断的理由为(5)
 与水反应的化学方程式为
与水反应的化学方程式为
您最近半年使用:0次
解题方法
2 .  、
、 、
、 等含磷化合物是重要的化工原料,其中
等含磷化合物是重要的化工原料,其中 经常以
经常以 的形式存在。
的形式存在。 的分子空间结构具有对称性,模型如图所示(其中短线代表单键或双键),下列说法错误的是
的分子空间结构具有对称性,模型如图所示(其中短线代表单键或双键),下列说法错误的是
 、
、 、
、 等含磷化合物是重要的化工原料,其中
等含磷化合物是重要的化工原料,其中 经常以
经常以 的形式存在。
的形式存在。 的分子空间结构具有对称性,模型如图所示(其中短线代表单键或双键),下列说法错误的是
的分子空间结构具有对称性,模型如图所示(其中短线代表单键或双键),下列说法错误的是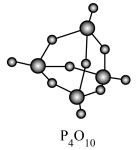
A. 中含有σ键和π键 中含有σ键和π键 |
B. 是非极性分子 是非极性分子 |
C. 分子的空间构型为三角锥形 分子的空间构型为三角锥形 |
D. 中所有原子都满足 中所有原子都满足 稳定结构 稳定结构 |
您最近半年使用:0次
解题方法
3 . 下列化学用语或图示表达正确的是
A.HCl的电子式: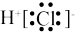 | B.基态碳原子的轨道表示式: |
C.中子数为7的氮原子: | D. 的VSEPR模型: 的VSEPR模型: |
您最近半年使用:0次
2024-04-16更新
|
272次组卷
|
2卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
解题方法
4 . 已知:常温下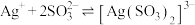 ,
,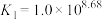 ,
,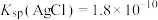 ,某实验小组利用AgCl与Na2SO3反应生成
,某实验小组利用AgCl与Na2SO3反应生成 来“分银”,“分银”时,
来“分银”,“分银”时, 的浓度与溶液pH的关系如图1;
的浓度与溶液pH的关系如图1; 与H+形成的微粒的浓度分数
与H+形成的微粒的浓度分数 随溶液pH变化的关系如图2,下列叙述错误的是
随溶液pH变化的关系如图2,下列叙述错误的是
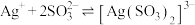 ,
,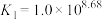 ,
,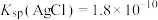 ,某实验小组利用AgCl与Na2SO3反应生成
,某实验小组利用AgCl与Na2SO3反应生成 来“分银”,“分银”时,
来“分银”,“分银”时, 的浓度与溶液pH的关系如图1;
的浓度与溶液pH的关系如图1; 与H+形成的微粒的浓度分数
与H+形成的微粒的浓度分数 随溶液pH变化的关系如图2,下列叙述错误的是
随溶液pH变化的关系如图2,下列叙述错误的是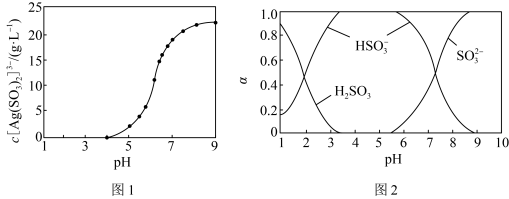
A. 中的∠O—S—O小于 中的∠O—S—O小于 中的∠O—S—O 中的∠O—S—O |
| B.“分银”时,pH需控制的范围大约是8~9 |
C. 溶液中存在 溶液中存在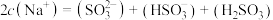 |
D.AgCl与 反应生成 反应生成 和 和 ,该反应的平衡常数 ,该反应的平衡常数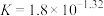 |
您最近半年使用:0次
解题方法
5 . 结构决定性质,下列关于物质结构或性质及有关解释不正确的是
| A.稳定性:H2O>H2S,是由于水分子间存在氢键 |
| B.酸性:一氟乙酸>一氯乙酸,是由于F的电负性大于Cl,F—C的极性大于Cl—C的极性 |
| C.键角:NCl3>PCl3,是由于N的电负性比P大,N的成键电子对之间距离较近,斥力较大 |
| D.溶解度:O3在CCl4中的溶解度高于在水中的溶解度,是由于O3的极性微弱 |
您最近半年使用:0次
6 . 短周期元素甲、乙、丙、丁、戊在元素周期表中的相对位置如图所示,已知戊的非金属性最强且其基态原子p轨道只有一个未成对电子。下列说法错误的是
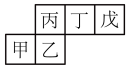
| A.简单离子半径:丁>戊 | B.第一电离能:丙<丁<戊 |
| C.简单氢化物的沸点:乙<丙 | D.简单氢化物的键角:甲>乙 |
您最近半年使用:0次
7 . 下列化学用语或图示表达正确的是
A.NaOH的电子式: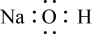 |
B.基态Cu的价层电子排布式: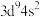 |
C.基态硅原子的价层电子轨道表示式: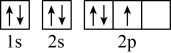 |
D. 分子的空间结构: 分子的空间结构: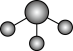 |
您最近半年使用:0次
名校
解题方法
8 . 下列说法正确的是
A. 的第一电离能高于 的第一电离能高于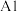 ,则 ,则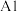 的金属性强于 的金属性强于 |
B. 是非极性分子,则 是非极性分子,则 也是非极性分子 也是非极性分子 |
| C.分子晶体中分子间作用力越大,对应的物质越稳定 |
| D.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
您最近半年使用:0次
名校
解题方法
9 . 下列化学用语表述正确的是
A. 的价电子排布式: 的价电子排布式: | B. 的球棍模型: 的球棍模型: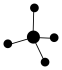 |
C. 的电子式: 的电子式: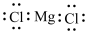 | D. 分子的VSEPR模型: 分子的VSEPR模型: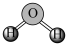 |
您最近半年使用:0次
名校
解题方法
10 . 实验室中常用NaOH对NO、NO2的尾气进行吸收,反应方程式NO+NO2+2NaOH=2NaNO2+H2O,下列说法错误的是
| A.NaNO2中既有共价键也有离子键 |
B.氮原子的价层电子轨道表示式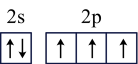 |
| C.水的VSEPR模型为四面体形 |
| D.NO、NO2均为酸性氧化物 |
您最近半年使用:0次



