名校
解题方法
1 . 下列说法正确的是
| A.杂化轨道只用于形成σ键 |
B. 分子N原子的杂化方式为 分子N原子的杂化方式为 |
C. 的VSEPR模型为三角锥形 的VSEPR模型为三角锥形 |
D.HF分子间氢键可表示为: |
您最近半年使用:0次
2 . 下列表示不正确 的是
A.硝化甘油的结构简式: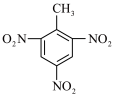 | B.中子数为20的氯离子: |
C.2-丁烯的实验式: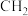 | D. 的价层电子对互斥(VSEPR)模型: 的价层电子对互斥(VSEPR)模型: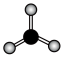 |
您最近半年使用:0次
7日内更新
|
213次组卷
|
2卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题
名校
解题方法
3 . 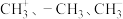 都是重要的有机反应中间体,有关它们的说法正确的是
都是重要的有机反应中间体,有关它们的说法正确的是
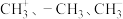 都是重要的有机反应中间体,有关它们的说法正确的是
都是重要的有机反应中间体,有关它们的说法正确的是A.它们的碳原子均采取 杂化,其中 杂化,其中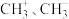 的结构示意图分别为: 的结构示意图分别为: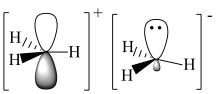 |
B. 与 与 形成的化合物中含有离子键 形成的化合物中含有离子键 |
C. 的键角和比 的键角和比 的键角小 的键角小 |
D. 与 与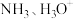 互为等电子体,VSEPR立体构型均为四面体形 互为等电子体,VSEPR立体构型均为四面体形 |
您最近半年使用:0次
名校
解题方法
4 . 燃油汽车尾气中含有CO和氮氧化物,在 的催化作用下,发生反应:
的催化作用下,发生反应: ,可降低污染。其反应历程和相对能量变化如图所示:
,可降低污染。其反应历程和相对能量变化如图所示:不正确 的是
 的催化作用下,发生反应:
的催化作用下,发生反应: ,可降低污染。其反应历程和相对能量变化如图所示:
,可降低污染。其反应历程和相对能量变化如图所示: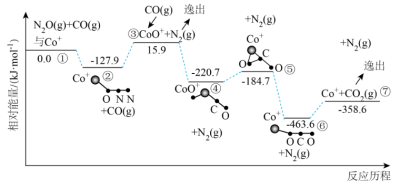
A. 分子的中心原子是N,分子中O—N—N的键角大于 分子的中心原子是N,分子中O—N—N的键角大于 分子中O—N—O的键角 分子中O—N—O的键角 |
| B.历程中决定反应速率的变化过程是②→③ |
C.总反应分两步进行,已知 参与第一步反应,则第二步反应为: 参与第一步反应,则第二步反应为: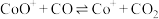 |
D.恒容、绝热下模拟反应: ,体系的温度、 ,体系的温度、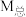 (平均相对分子质量)、压强恒定均能说明反应达到平衡状态 (平均相对分子质量)、压强恒定均能说明反应达到平衡状态 |
您最近半年使用:0次
解题方法
5 . 下列表示不正确 的是
A.质子数为92、中子数为146的U原子: |
B.HClO的电子式: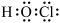 |
C.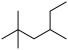 的名称:2,2,4-三甲基己烷 的名称:2,2,4-三甲基己烷 |
D.H2S的价层电子对互斥(VSEPR)模型: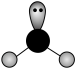 |
您最近半年使用:0次
名校
解题方法
6 . 下列分子或离子的空间结构和中心原子的杂化方式均正确的是
A. 平面三角形 平面三角形  杂化 杂化 | B. 平面三角形 平面三角形  杂化 杂化 |
C. V形 V形  杂化 杂化 | D. 三角锥形 三角锥形  杂化 杂化 |
您最近半年使用:0次
2024-04-21更新
|
212次组卷
|
2卷引用:浙江省舟山中学2023-2024学年高二下学期4月月考化学试题
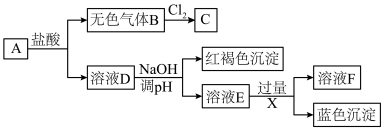
7 . 某固体混合物A由FeSO4、ZnCl2和Cu(NO3)2组成,3种物质的物质的量之比为1∶1∶1。进行如下实验:
②一些阳离子的开始沉淀至完全沉淀的范围:Fe2+(6.3~8.3)、Fe3+(1.5~2.8)、Zn2+(5.4~8.0)、Cu2+(4.7~6.2)。
③Ag2SO4微溶于硝酸。
请回答:
(1)气体B的主要成分为_____________ ,2mol气体B与1mol Cl2化合生成2mol C,C的空间构型为_____________ 。
(2)溶液F中除OH-、Cl-外的阴离子还有_____________ 。
(3)下列说法正确的是 。
(4)请设计实验检验A中的氯离子_______________ 。
(5)新制蓝色沉淀的悬浊液中通入SO2,产生紫红色固体,写出该反应离子方程式:_____________ 。
②一些阳离子的开始沉淀至完全沉淀的范围:Fe2+(6.3~8.3)、Fe3+(1.5~2.8)、Zn2+(5.4~8.0)、Cu2+(4.7~6.2)。
③Ag2SO4微溶于硝酸。
请回答:
(1)气体B的主要成分为
(2)溶液F中除OH-、Cl-外的阴离子还有
(3)下列说法正确的是 。
A.根据实验中的转化关系可得: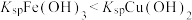 |
| B.调pH范围应控制在2.8~5.4 |
| C.X可以使用氨水或NaOH |
| D.气体B是形成光化学烟雾的罪魁祸首之一 |
(4)请设计实验检验A中的氯离子
(5)新制蓝色沉淀的悬浊液中通入SO2,产生紫红色固体,写出该反应离子方程式:
您最近半年使用:0次
名校
解题方法
8 . 下列表示不正确 的是
A.乙烯的分子结构示意图: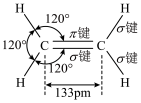 |
B.碳原子的价层电子排布式: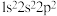 |
C.甲基的电子式: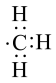 |
D.碳酸根的价层电子对互斥(VSEPR)模型: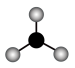 |
您最近半年使用:0次
名校
9 . 将X与BeCl2按物质的量比1:1溶于环己烷(溶剂)中得白色沉淀化合物Y,化学式为Be2Cl4I4S4,Y结构如下,下列说法正确的是
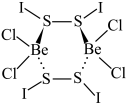
A.X的Lewis结构式为: |
| B.该白色沉淀溶于水会析出游离出S2I2.因为О亲核性强于硫 |
| C.从酸碱反应的角度看X与BeCl2反应,X是酸 |
| D.Y中各元素化学环境相同,其中Be原子的杂化方式与BeCl2一样,都为sp2 |
您最近半年使用:0次
解题方法
10 . 下列化学用语使用正确的是
A.甲胺的电子式: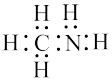 | B.某烷烃名称为2,5-二甲基戊烷 |
C.中子数为7的碳原子: | D. 的价层电子对互斥模型: 的价层电子对互斥模型: |
您最近半年使用:0次



