名校
1 . 将X与BeCl2按物质的量比1:1溶于环己烷(溶剂)中得白色沉淀化合物Y,化学式为Be2Cl4I4S4,Y结构如下,下列说法正确的是
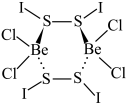
A.X的Lewis结构式为: |
| B.该白色沉淀溶于水会析出游离出S2I2.因为О亲核性强于硫 |
| C.从酸碱反应的角度看X与BeCl2反应,X是酸 |
| D.Y中各元素化学环境相同,其中Be原子的杂化方式与BeCl2一样,都为sp2 |
您最近一年使用:0次
真题
解题方法
2 . 氮和氧是构建化合物的常见元素。
(1)某化合物的晶胞如图,其化学式是_______ ,晶体类型是_______ 。
(2)下列说法正确的是_______。
(3)① ,其中
,其中 的N原子杂化方式为
的N原子杂化方式为_______ ;比较键角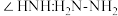 中的
中的
_______  中的
中的 (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由_______ 。
②将 与
与 按物质的量之比1:2发生化合反应生成A,测得A由2种微粒构成,其中之一是
按物质的量之比1:2发生化合反应生成A,测得A由2种微粒构成,其中之一是 。比较氧化性强弱:
。比较氧化性强弱:
_______  (填“>”、“<”或“=”);写出A中阴离子的结构式
(填“>”、“<”或“=”);写出A中阴离子的结构式_______ 。
已知: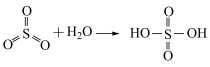
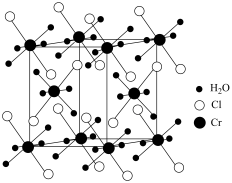
(1)某化合物的晶胞如图,其化学式是
(2)下列说法正确的是_______。
A.电负性: | B.离子半径: |
C.第一电离能: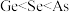 | D.基态 2+的简化电子排布式: 2+的简化电子排布式: |
(3)①
 ,其中
,其中 的N原子杂化方式为
的N原子杂化方式为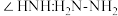 中的
中的
 中的
中的 (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由②将
 与
与 按物质的量之比1:2发生化合反应生成A,测得A由2种微粒构成,其中之一是
按物质的量之比1:2发生化合反应生成A,测得A由2种微粒构成,其中之一是 。比较氧化性强弱:
。比较氧化性强弱:
 (填“>”、“<”或“=”);写出A中阴离子的结构式
(填“>”、“<”或“=”);写出A中阴离子的结构式
您最近一年使用:0次
解题方法
3 . 连二硫酸锰(MnS2O6,其中Mn为+2价)是一种常用的果蔬保鲜剂,易溶于水,室温下其水溶液在pH为2.8~3.5时最稳定。回答下列问题:
【探究】制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。

(1)装置A中装有70%H2SO4的仪器名称为___________ ,装置B的作用是___________ 。
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是___________ ,实验时需要向C中通入稍过量的SO2,目的是___________ 。
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为___________ ,判断反应完成的现象是___________ 。
(4)连二硫酸结构式为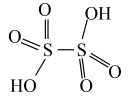 ,推断连二硫酸中S原子上
,推断连二硫酸中S原子上_________ 孤电子对(填“有”或“无”),已知甲磺酸的结构简式为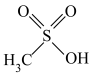 ,连二硫酸H-O的极性
,连二硫酸H-O的极性________ 甲磺酸H-O的极性(填“大于”“小于”或“等于”)。
【探究】制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。

(1)装置A中装有70%H2SO4的仪器名称为
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为
(4)连二硫酸结构式为
 ,推断连二硫酸中S原子上
,推断连二硫酸中S原子上 ,连二硫酸H-O的极性
,连二硫酸H-O的极性
您最近一年使用:0次
解题方法
4 . 磷酸铁锂电池是以磷酸铁锂(LiFePO4)为正极材料的锂离子电池,具有循环寿命长、安全性能好、无环境污染等特点。
(1)磷酸铁锂具有橄榄石结构,空间骨架结构不易发生形变,化学性质稳定。
①基态 的价层电子排布式为
的价层电子排布式为_______ 。
②Li、P、O三种元素的电负性由大到小的顺序是_______ 。
(2)硫酸亚铁(FeSO4)可用于制备磷酸铁锂。
①根据价层电子对互斥理论可知, 的空间结构为
的空间结构为_______ 。
②比较S原子和O原子的第一电离能大小,并从原子结构的角度说明理由:_______ 。
(3)草酸亚铁(FeC2O4)也可用于制备磷酸铁锂。草酸根离子的结构简式为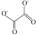 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为_______ 。
(4)磷酸铁(FePO4)与磷酸铁锂结构相似,其中 围绕
围绕 和
和 分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,
分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,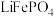 中的
中的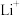 会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
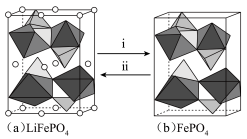
①i表示_______ (填“充电”或“放电”)过程。
②已知Li+的脱嵌率= 。某时刻,若正极材料中Li+的脱嵌率为
。某时刻,若正极材料中Li+的脱嵌率为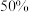 ,则其中
,则其中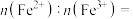
_______ 。
(1)磷酸铁锂具有橄榄石结构,空间骨架结构不易发生形变,化学性质稳定。
①基态
 的价层电子排布式为
的价层电子排布式为②Li、P、O三种元素的电负性由大到小的顺序是
(2)硫酸亚铁(FeSO4)可用于制备磷酸铁锂。
①根据价层电子对互斥理论可知,
 的空间结构为
的空间结构为②比较S原子和O原子的第一电离能大小,并从原子结构的角度说明理由:
(3)草酸亚铁(FeC2O4)也可用于制备磷酸铁锂。草酸根离子的结构简式为
 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为(4)磷酸铁(FePO4)与磷酸铁锂结构相似,其中
 围绕
围绕 和
和 分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,
分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,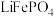 中的
中的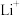 会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
①i表示
②已知Li+的脱嵌率=
 。某时刻,若正极材料中Li+的脱嵌率为
。某时刻,若正极材料中Li+的脱嵌率为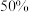 ,则其中
,则其中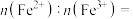
您最近一年使用:0次
名校
解题方法
5 . 2022年9月9日,国家航天局、国家原子能机构联合在北京发布嫦娥五号最新科学成果,中核集团核工业北京地质研究院科研团队首次在月球上发现的新矿物,被命名为“嫦娥石”,我国成为世界上第三个在月球发现新矿物的国家。
回答下列问题:
(1)中核集团核工业北京地质研究院科研团队,通过晶体___________ 实验等一系列高新技术手段,成功解译其晶体结构。
(2)嫦娥石是一种陨磷钠镁钙石类矿物,基态P、Na、Mg、Ca四种元素的原子第一电离能由大到小的顺序为___________ 。
(3)从晶体结构上看,嫦娥石可以分为两大部分,其中阴离子结构单元为[Fe(PO4)6]16-,请写出Fe2+的基态价层电子排布式___________ ,PO 的VSEPR模型名称为
的VSEPR模型名称为___________ 。
(4)从结构角度分析Fe3+比Fe2+稳定的原因___________ 。
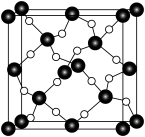
(5)嫦娥石的一种伴生矿物为方石英,方石英结构和金刚石相似,其晶胞结构如图所示,Si-O键长为anm,∠AED=109°28′,已知阿伏伽德罗常数为NA,则方石英晶体的的密度为___________ g·cm-3(列出计算式即可)。

回答下列问题:
(1)中核集团核工业北京地质研究院科研团队,通过晶体
(2)嫦娥石是一种陨磷钠镁钙石类矿物,基态P、Na、Mg、Ca四种元素的原子第一电离能由大到小的顺序为
(3)从晶体结构上看,嫦娥石可以分为两大部分,其中阴离子结构单元为[Fe(PO4)6]16-,请写出Fe2+的基态价层电子排布式
 的VSEPR模型名称为
的VSEPR模型名称为(4)从结构角度分析Fe3+比Fe2+稳定的原因
(5)嫦娥石的一种伴生矿物为方石英,方石英结构和金刚石相似,其晶胞结构如图所示,Si-O键长为anm,∠AED=109°28′,已知阿伏伽德罗常数为NA,则方石英晶体的的密度为

您最近一年使用:0次
2023-08-12更新
|
396次组卷
|
2卷引用:浙江省金丽衢十二校2022-2023学年高三上学期第一次联考化学试题
解题方法
6 . 含硅化合物在生活中的应用非常广泛。请回答下列问题:
(1)祖母绿宝石的主要成分化学式为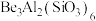 ,
, 与
与 的第一电离能大小关系为:
的第一电离能大小关系为:
___________ 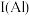 。
。
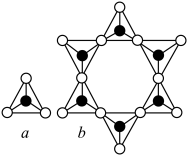
(2)硅酸盐的阴离子结构丰富多样,有些是有限数目的硅氧四面体构建的简单阴离子,如图所示,最简单的硅酸盐阴离子a的化学式为 ,则六元环状硅酸盐阴离子b的化学式是
,则六元环状硅酸盐阴离子b的化学式是___________ (不能用最简式表示)。
(3)工业制备高纯硅,先用焦炭在电炉中将石英还原为粗硅,再将粗硅与 在300℃反应生成
在300℃反应生成 ,氯原子的价层电子排布式为
,氯原子的价层电子排布式为___________ , 的空间构型为
的空间构型为___________ 。
(4)硅的各种卤化物的沸点如下表,沸点依次升高的原因是___________ 。
(5)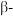 石英是晶质石英(
石英是晶质石英( )的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为
)的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为___________ ,请用价层电子对互斥模型解释图中键角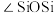 并不是
并不是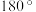 的原因是
的原因是___________ 。
(1)祖母绿宝石的主要成分化学式为
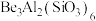 ,
, 与
与 的第一电离能大小关系为:
的第一电离能大小关系为:
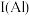 。
。(2)硅酸盐的阴离子结构丰富多样,有些是有限数目的硅氧四面体构建的简单阴离子,如图所示,最简单的硅酸盐阴离子a的化学式为
 ,则六元环状硅酸盐阴离子b的化学式是
,则六元环状硅酸盐阴离子b的化学式是
(3)工业制备高纯硅,先用焦炭在电炉中将石英还原为粗硅,再将粗硅与
 在300℃反应生成
在300℃反应生成 ,氯原子的价层电子排布式为
,氯原子的价层电子排布式为 的空间构型为
的空间构型为(4)硅的各种卤化物的沸点如下表,沸点依次升高的原因是
 |  | 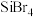 |  | |
| 沸点/K | 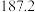 | 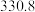 | 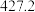 | 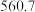 |
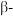 石英是晶质石英(
石英是晶质石英( )的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为
)的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为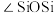 并不是
并不是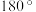 的原因是
的原因是
您最近一年使用:0次
解题方法
7 . 卤化物、氢化物在科研和生活中占有重要地位。回答下列问题:
(1)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是 。
(2) 的VSEPR模型名称为
的VSEPR模型名称为____________ 。
(3)二氟氮烯(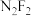 )分子中,每个原子均满足八电子稳定结构,则
)分子中,每个原子均满足八电子稳定结构,则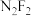 的结构式为
的结构式为____________ 。
(4)C、N、O三种元素都能与H元素形成含A-A(A表示C、N、O元素)键的氢化物。氢化物中A-A键的键能( )如下表:
)如下表:
A-A键的键能依次降低的原因是____________________________________________________________ 。
(5)第三代太阳能电池利用有机金属卤化物碘化铅甲胺( )半导体作为吸光材料。
)半导体作为吸光材料。 的晶胞如图所示,其中
的晶胞如图所示,其中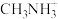 位于顶点(大空心球)位置。已知
位于顶点(大空心球)位置。已知 晶体的晶胞参数为a nm,阿伏加德罗常数的值为
晶体的晶胞参数为a nm,阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为____________  。(用最简式表达)
。(用最简式表达)

(1)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是 。
A. | B. | C. | D. |
 的VSEPR模型名称为
的VSEPR模型名称为(3)二氟氮烯(
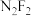 )分子中,每个原子均满足八电子稳定结构,则
)分子中,每个原子均满足八电子稳定结构,则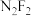 的结构式为
的结构式为(4)C、N、O三种元素都能与H元素形成含A-A(A表示C、N、O元素)键的氢化物。氢化物中A-A键的键能(
 )如下表:
)如下表:
|
| HO-OH |
346 | 247 | 207 |
(5)第三代太阳能电池利用有机金属卤化物碘化铅甲胺(
 )半导体作为吸光材料。
)半导体作为吸光材料。 的晶胞如图所示,其中
的晶胞如图所示,其中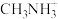 位于顶点(大空心球)位置。已知
位于顶点(大空心球)位置。已知 晶体的晶胞参数为a nm,阿伏加德罗常数的值为
晶体的晶胞参数为a nm,阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为 。(用最简式表达)
。(用最简式表达)
您最近一年使用:0次
名校
8 . 硫化硅分子式为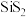 ,遇水会发生水解。下列推测
,遇水会发生水解。下列推测不合理 的是
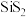 ,遇水会发生水解。下列推测
,遇水会发生水解。下列推测A.与硫化钠作用可生成 |
B.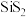 在空气中可以被点燃 在空气中可以被点燃 |
C.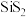 的空间结构名称为V形 的空间结构名称为V形 |
D.水解产物可能为 和 和 |
您最近一年使用:0次
2023-04-21更新
|
363次组卷
|
4卷引用:浙江省9+1联盟2022-2023学年高二下学期期中考试化学试题
浙江省9+1联盟2022-2023学年高二下学期期中考试化学试题(已下线)【2023】【高二下】【期中考】【9+1联盟】【高中化学】【洪翔峰收集】河南省南阳市第一中学校2022-2023学年高二下学期5月月考化学试题(已下线)实验05 盐类水解的应用-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)
22-23高二上·浙江杭州·期中
名校
解题方法
9 . 下列有关描述正确的是
| A.O3为非极性分子 |
| B.NCl3的空间结构为平面三角形 |
C. 的VSEPR模型、空间结构均为平面三角形 的VSEPR模型、空间结构均为平面三角形 |
D. 的VSEPR模型、空间结构相同 的VSEPR模型、空间结构相同 |
您最近一年使用:0次
2022·浙江·模拟预测
解题方法
10 . 硼化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态B原子核外电子有_______ 种不同的空间运动状态。
(2) 主要用作有机合成中的催化剂,也用于制作火箭的高能燃料。
主要用作有机合成中的催化剂,也用于制作火箭的高能燃料。 的空间构型为
的空间构型为_______ 。形成 时,基态B原子价层电子先进行激发,再进行杂化,激发时B原子的价层电子轨道表示式可能为
时,基态B原子价层电子先进行激发,再进行杂化,激发时B原子的价层电子轨道表示式可能为_______ 。(填序号)。
A.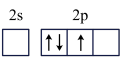 B.
B.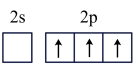 C.
C.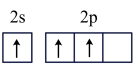 D.
D.
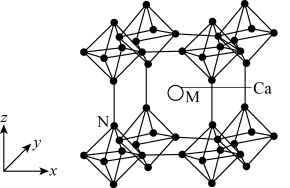
(3)Ca与B组成的金属硼化物结构如图所示,硼原子通过B—B键互相连接成三维骨架形成 正八面体,该结构具有立方晶系的对称性。
正八面体,该结构具有立方晶系的对称性。
①该晶体的化学式为_______ ,晶体中Ca原子的配位数为_______ 。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如M点原子的分数坐标为 ,已知
,已知 八面体中B—B键的键长为rpm,晶胞参数为apm,则N点原子的分数坐标为
八面体中B—B键的键长为rpm,晶胞参数为apm,则N点原子的分数坐标为_______ ,Ca与B原子间的距离d为_______ pm(列出表达式即可)。
(1)基态B原子核外电子有
(2)
 主要用作有机合成中的催化剂,也用于制作火箭的高能燃料。
主要用作有机合成中的催化剂,也用于制作火箭的高能燃料。 的空间构型为
的空间构型为 时,基态B原子价层电子先进行激发,再进行杂化,激发时B原子的价层电子轨道表示式可能为
时,基态B原子价层电子先进行激发,再进行杂化,激发时B原子的价层电子轨道表示式可能为A.
 B.
B. C.
C. D.
D.
(3)Ca与B组成的金属硼化物结构如图所示,硼原子通过B—B键互相连接成三维骨架形成
 正八面体,该结构具有立方晶系的对称性。
正八面体,该结构具有立方晶系的对称性。①该晶体的化学式为
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如M点原子的分数坐标为
 ,已知
,已知 八面体中B—B键的键长为rpm,晶胞参数为apm,则N点原子的分数坐标为
八面体中B—B键的键长为rpm,晶胞参数为apm,则N点原子的分数坐标为
您最近一年使用:0次





