名校
解题方法
1 . 铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
(1)基态Fe3+的电子排布式为_________________ 。
(2)实验室用KSCN溶液、苯酚(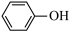 )检验Fe3+。N、O、S的第一电离能由大到小的顺序为
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为______ (用元素符号表示),苯酚中碳原子的杂化轨道类型为_______ 。
(3)FeCl3的熔点为306℃,沸点为315℃。FeCl3的晶体类型是________ 。FeSO4常作补铁剂,SO42-的立体构型是__________ 。
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗暴剂等。1 mol Fe(CO)5分子中含________ molσ键,与CO互为等电子体的离子是__________ (填化学式,写一种)。
(5)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为_____ 。
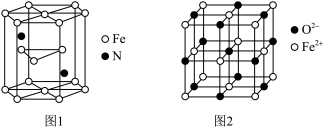
(6)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加 德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____ ;Fe2+与O2-的最短核间距为___________ pm。
(1)基态Fe3+的电子排布式为
(2)实验室用KSCN溶液、苯酚(
 )检验Fe3+。N、O、S的第一电离能由大到小的顺序为
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为(3)FeCl3的熔点为306℃,沸点为315℃。FeCl3的晶体类型是
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗暴剂等。1 mol Fe(CO)5分子中含
(5)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为

(6)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加 德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为
您最近一年使用:0次
2019-12-11更新
|
706次组卷
|
9卷引用:宁夏回族自治区吴忠市青铜峡市高级中学2020届高三上学期第二次月考化学试题
宁夏回族自治区吴忠市青铜峡市高级中学2020届高三上学期第二次月考化学试题【市级联考】广东省揭阳市2019届高三上学期期末学业水平考试理科综合化学试题【全国百强校】河北省武邑中学2019届高三上学期期末考试化学试题【校级联考】甘肃省河西五地2018-2019学年高二第二学期联考化学试题【市级联考】山东省泰安市2019届高三下学期3月第一次模拟考试理科综合化学试题四川省绵阳南山中学2020届高三9月月考理科综合化学试题2020届高考化学二轮复习物质结构与性质专题练习河北省石家庄市第二中学2020届高三下学期教学质量检测模拟考试理综化学试题(已下线)专题6.4 物质结构与性质(选考)(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升
名校
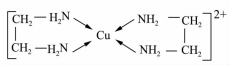
2 . GaN、GaP、GaAs是人工合成的一系列新型半导体材料,其晶体结构均与金刚石相似。铜是重要的过渡元素,能形成多种配合物,如Cu2+与乙二胺(H2N-CH2-CH2-NH2)可形成如图所示配离子。回答下列问题:
(1)基态Ga原子价电子的轨道表达式为________________ ;
(2)熔点:GaN_____ GaP(填“>”或“<”);
(3)第一电离能:As_____ Se(填“>”或“<”);
(4)Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是______ ;
a.配位键 b.极性键 c.离子键 d.非极性键
(5)乙二胺分子中氮原子轨道的杂化类型为________ ,乙二胺和三甲胺[N(CH3)3]均属于胺。但乙二胺比三甲胺的沸点高很多,原因是___________ ;
(6)Cu的某种晶体晶胞为面心立方结构,晶胞边长为acm,铜原子的半径为rcm。该晶体中铜原子的堆积方式为_______ 型(填“A1”、“A2”或“A3”),该晶体密度为____ g/cm3(用含a和NA的代数式表达),该晶体中铜原子的空间利用率为______ (用含a和r的代数式表达)。
(1)基态Ga原子价电子的轨道表达式为
(2)熔点:GaN
(3)第一电离能:As
(4)Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是
a.配位键 b.极性键 c.离子键 d.非极性键
(5)乙二胺分子中氮原子轨道的杂化类型为
(6)Cu的某种晶体晶胞为面心立方结构,晶胞边长为acm,铜原子的半径为rcm。该晶体中铜原子的堆积方式为
您最近一年使用:0次
2017-03-27更新
|
370次组卷
|
4卷引用:宁夏六盘山高级中学2017届高三第四次模拟考试理科综合化学试题
解题方法
3 . 【化学一选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大。A 是原子半径最小的元素;B的最外层电子数是次外层电子数的2倍; D的L能层有两对成对电子;E+的核外有三个能层,且都外于全满状态。试回答下列问题:
(1)基态E原子核外电子的排布式为___________________ 。
(2)B、C、D三种元素的电负性由大到小的顺序是____________ (填元素符号)。A、C、D三种元素形成的常见离子化合物中阳离子的空间构型为_____________ ,阴离子的中心原子轨道采用______________ 杂化。
(3)E(CA3) 离子的颜色是
离子的颜色是___________ ;含有化学键类型是_____________ ;离子中C原子杂化轨道类型是__________________ 。
(4)D、E能形成两种晶体,其晶胞分别如甲、乙两图。晶体乙中,E的配位数为_________ ;在一定条件下,甲和C2A4反应生成乙,同时生成在常温下分别为气体和液体的另外两种常见无污染物质。该化学反应方程式为______________________ 。
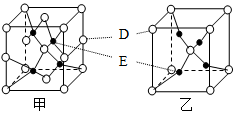
(5)若甲的密度为ρ g/cm3,NA表示阿伏伽德罗常数,则甲晶胞的边长可表示为_________ cm。
(1)基态E原子核外电子的排布式为
(2)B、C、D三种元素的电负性由大到小的顺序是
(3)E(CA3)
 离子的颜色是
离子的颜色是(4)D、E能形成两种晶体,其晶胞分别如甲、乙两图。晶体乙中,E的配位数为

(5)若甲的密度为ρ g/cm3,NA表示阿伏伽德罗常数,则甲晶胞的边长可表示为
您最近一年使用:0次
解题方法
4 . 选修原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子。
(1)Y原子核外共有________ 种不同运动状态的电子,基态T原子有________ 种不同能级的电子。
(2)X、Y、Z的第一电离能由小到大的顺序为________ (用元素符号表示)
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为________ 。
(4)Z与R能形成化合物甲,1mol甲中含________ mol化学键,甲与氢氟酸反应,生成物的分子空间构型分别为________ ,________ 。
(5)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为________ 。
(6)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应的离子方程式为
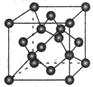
(7)X单质的晶胞如图所示,一个X晶胞中有________ 个X原子;若X晶体的密度为p g/cm3,阿伏加德罗常数的值为NA,则晶体中最近 的两个X原子之间的距离为________ cm(用代数式表示)。
(1)Y原子核外共有
(2)X、Y、Z的第一电离能由小到大的顺序为
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为
(4)Z与R能形成化合物甲,1mol甲中含
(5)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为
| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1539 | 183 |
(6)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应的离子方程式为
(7)X单质的晶胞如图所示,一个X晶胞中有

您最近一年使用:0次
2016-12-09更新
|
188次组卷
|
3卷引用:2016届宁夏六盘山高级中学高三二模理综化学试卷



