解题方法
1 . 铜及其化合物是生活、生产中运用广泛的材料。
(1)铜元素在周期表中的位置是___________ ,基态 原子核外电子占据最高能层的符号是
原子核外电子占据最高能层的符号是___________ 。
(2)合成氨工业常用醋酸二氨合铜(I){ }溶液吸收对氨合成的催化剂有毒害作用的
}溶液吸收对氨合成的催化剂有毒害作用的 。
。
① 中存在的化学键类型有
中存在的化学键类型有___________ 。
② 的沸点比
的沸点比 的沸点
的沸点___________ ,原因是___________ 。 的键角小于
的键角小于 的键角,原因是
的键角,原因是___________ 。
(3)晶胞的两个基本要素。
①原子坐标参数:晶胞内部各微粒的相对位置。 的晶胞结构如图所示,其中原子坐标参数:A
的晶胞结构如图所示,其中原子坐标参数:A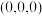 ;B
;B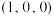 ;C
;C 。则
。则 处微粒的坐标参数为
处微粒的坐标参数为___________ 。
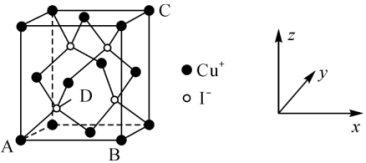
②晶胞参数:描述晶胞的大小和形状。若晶胞的边长为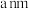 ,则
,则 与
与 的最短距离为
的最短距离为___________  ,设
,设 为阿伏加德罗常数的值,该化合物的密度为
为阿伏加德罗常数的值,该化合物的密度为___________ (用含 、
、 的代数式表示)
的代数式表示) 。
。
(1)铜元素在周期表中的位置是
 原子核外电子占据最高能层的符号是
原子核外电子占据最高能层的符号是(2)合成氨工业常用醋酸二氨合铜(I){
 }溶液吸收对氨合成的催化剂有毒害作用的
}溶液吸收对氨合成的催化剂有毒害作用的 。
。①
 中存在的化学键类型有
中存在的化学键类型有②
 的沸点比
的沸点比 的沸点
的沸点 的键角小于
的键角小于 的键角,原因是
的键角,原因是(3)晶胞的两个基本要素。
①原子坐标参数:晶胞内部各微粒的相对位置。
 的晶胞结构如图所示,其中原子坐标参数:A
的晶胞结构如图所示,其中原子坐标参数:A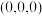 ;B
;B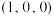 ;C
;C 。则
。则 处微粒的坐标参数为
处微粒的坐标参数为
②晶胞参数:描述晶胞的大小和形状。若晶胞的边长为
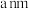 ,则
,则 与
与 的最短距离为
的最短距离为 ,设
,设 为阿伏加德罗常数的值,该化合物的密度为
为阿伏加德罗常数的值,该化合物的密度为 、
、 的代数式表示)
的代数式表示) 。
。
您最近一年使用:0次
解题方法
2 . 《物质结构与性质》
(1)下列粒子的立体构型不是平面三角形的是___________ 。
A.CO32- B.NH3 C.BF3 D.SO3
(2)下列分子中,属于含极性键的非极性分子的是___________ 。
A.CH4 B.H2S C.C60 D.HCl
(3)现有四种离子晶体的晶胞,其离子排列方式如下列图所示,其中化学式不属于Mn型的是______ 。

(4)联合制碱法又称侯氏制碱法,其原理为:第一步NaCl+ NH3 + CO2+H2O=NaHCO3 + NH4Cl,第二步加热NaHCO3使其分解。关于第一步反应所包含的各物质中:
①属于离子化合物的是_________________ (填化学式);
②中心原子是sp杂化的分子是_________________ (填化学式);
③NaCl晶体中Na+的配位数为___________ ;
④写出H2O的任意一种等电子体的化学式___________ 。
(5)周期表前四周期的五种元素a、b、c、d、e,其核电荷数依次增大。a原子的核外电子总数与其周期数相同,b原子的最外层电子中有3个未成对电子,c原子的最外层电子数是其内层电子数的3倍,d与c同主族,e的价电子排布为3d104s1。
①b、c元素的第一电离能大小为:b_______ c(填“>"或“<”)
②d的基态原子的电子排布式为___________ ; a2d的VSKPK模型为___________ 。
③ba3和a2c两种分子键角较大的是___________ ;ba3极易溶于a2c的原因,除了两种分子都是极性
分子外,还因为____________________________ 。
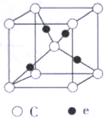
④e和c能形成一种化合物,其晶胞结构如右图所示,若设阿伏伽德罗常数值为NA,晶体的密度为d g/cm3,则晶胞参数a=_______ nm(用含d、NA的代数式表示)。
(1)下列粒子的立体构型不是平面三角形的是
A.CO32- B.NH3 C.BF3 D.SO3
(2)下列分子中,属于含极性键的非极性分子的是
A.CH4 B.H2S C.C60 D.HCl
(3)现有四种离子晶体的晶胞,其离子排列方式如下列图所示,其中化学式不属于Mn型的是

(4)联合制碱法又称侯氏制碱法,其原理为:第一步NaCl+ NH3 + CO2+H2O=NaHCO3 + NH4Cl,第二步加热NaHCO3使其分解。关于第一步反应所包含的各物质中:
①属于离子化合物的是
②中心原子是sp杂化的分子是
③NaCl晶体中Na+的配位数为
④写出H2O的任意一种等电子体的化学式
(5)周期表前四周期的五种元素a、b、c、d、e,其核电荷数依次增大。a原子的核外电子总数与其周期数相同,b原子的最外层电子中有3个未成对电子,c原子的最外层电子数是其内层电子数的3倍,d与c同主族,e的价电子排布为3d104s1。
①b、c元素的第一电离能大小为:b
②d的基态原子的电子排布式为
③ba3和a2c两种分子键角较大的是
分子外,还因为
④e和c能形成一种化合物,其晶胞结构如右图所示,若设阿伏伽德罗常数值为NA,晶体的密度为d g/cm3,则晶胞参数a=

您最近一年使用:0次



