1 . 用价电子对互斥(VSEPR)理论可以预测许多分子或离子的空间结构,有时也能用来推测键角大小,下列判断正确的是
| A.SO2、CS2、HI都是直线形分子 |
| B.BF3键角为120°,SnF2键角大于120° |
| C.COCl2、BF3、SO3都是平面三角形分子 |
| D.PCl3、NH3、PCl5都是三角锥形分子 |
您最近一年使用:0次
名校
2 . 烯烃催化制备醛的反应机理如下,下列说法错误的是
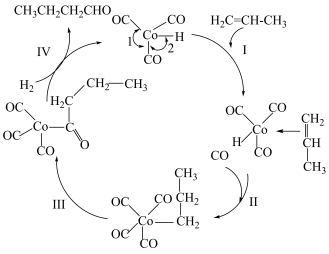

A.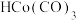 反应前后质量和化学性质没有发生变化 反应前后质量和化学性质没有发生变化 |
| B.步骤Ⅰ中钴的配位数和化合价都发生了变化 |
C.键角: |
D.总反应式为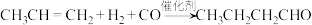 |
您最近一年使用:0次
3 . 下列说法正确的是
A. 分子中的氢键结构: 分子中的氢键结构: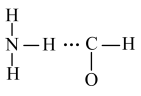 |
B.氢化物沸点: |
C. 的VSEPR模型: 的VSEPR模型: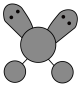 |
D.键角: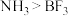 |
您最近一年使用:0次
解题方法
4 . Ⅰ.铊(T1)盐与氰化钾 被列为
被列为 级危险品,常用普鲁士蓝作为解毒剂.
级危险品,常用普鲁士蓝作为解毒剂.
(1)写出铊的价电子排布式:___________ 。
(2)向 溶液中滴加
溶液中滴加 溶液后,经提纯、结晶可得到
溶液后,经提纯、结晶可得到 普鲁士蓝蓝色晶体,实验表明,
普鲁士蓝蓝色晶体,实验表明, 通过配位键构成了晶体的骨架,其局部结构如图1所示,记为Ⅰ型立方结构,将Ⅰ型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2所示,记为Ⅱ型立方结构,下层左后方的小立方体
通过配位键构成了晶体的骨架,其局部结构如图1所示,记为Ⅰ型立方结构,将Ⅰ型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2所示,记为Ⅱ型立方结构,下层左后方的小立方体 未标出)。
未标出)。 )有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因:
)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因:___________ ;
②若 位于Ⅱ型立方结构的棱心和体心上,则
位于Ⅱ型立方结构的棱心和体心上,则 位于Ⅱ型立方结构的
位于Ⅱ型立方结构的___________ 上;若 的摩尔质量为
的摩尔质量为 ,该蓝色晶体密度为
,该蓝色晶体密度为 ,Ⅱ型立方结构的边长为
,Ⅱ型立方结构的边长为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
___________ (用含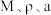 的代数式表示)。
的代数式表示)。
Ⅱ.铂钴合金磁性极强,磁稳定性较高,耐化学腐蚀性好,主要用于航天航空仪表、电子钟表、磁控管等。
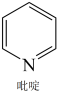
(3)二氯二吡啶合铂是由 和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体(如图所示).科学研究表明,其顺式分子具有抗癌活性.
和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体(如图所示).科学研究表明,其顺式分子具有抗癌活性. 键
键 ,吡啶中
,吡啶中 原子的价层孤电子对占据
原子的价层孤电子对占据___________ 轨道。
②二氯二吡啶合铂分子中存在的微粒间作用力有___________ (填选项字母)。
a.离子键 b.配位键 c.金属键
d.非极性键 e.氢键 f.极性键
③反式二氯二吡啶合铂分子是___________ (填“极性分子”或“非极性分子”)。
(4)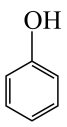 、
、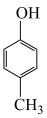 、
、 的酸性随羟基极性的增大而增强,则酸性从强到弱的排序为
的酸性随羟基极性的增大而增强,则酸性从强到弱的排序为___________ 。
 被列为
被列为 级危险品,常用普鲁士蓝作为解毒剂.
级危险品,常用普鲁士蓝作为解毒剂.(1)写出铊的价电子排布式:
(2)向
 溶液中滴加
溶液中滴加 溶液后,经提纯、结晶可得到
溶液后,经提纯、结晶可得到 普鲁士蓝蓝色晶体,实验表明,
普鲁士蓝蓝色晶体,实验表明, 通过配位键构成了晶体的骨架,其局部结构如图1所示,记为Ⅰ型立方结构,将Ⅰ型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2所示,记为Ⅱ型立方结构,下层左后方的小立方体
通过配位键构成了晶体的骨架,其局部结构如图1所示,记为Ⅰ型立方结构,将Ⅰ型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2所示,记为Ⅱ型立方结构,下层左后方的小立方体 未标出)。
未标出)。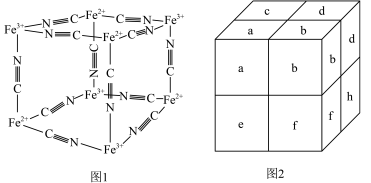
 )有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因:
)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因:②若
 位于Ⅱ型立方结构的棱心和体心上,则
位于Ⅱ型立方结构的棱心和体心上,则 位于Ⅱ型立方结构的
位于Ⅱ型立方结构的 的摩尔质量为
的摩尔质量为 ,该蓝色晶体密度为
,该蓝色晶体密度为 ,Ⅱ型立方结构的边长为
,Ⅱ型立方结构的边长为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
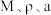 的代数式表示)。
的代数式表示)。Ⅱ.铂钴合金磁性极强,磁稳定性较高,耐化学腐蚀性好,主要用于航天航空仪表、电子钟表、磁控管等。
(3)二氯二吡啶合铂是由
 和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体(如图所示).科学研究表明,其顺式分子具有抗癌活性.
和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体(如图所示).科学研究表明,其顺式分子具有抗癌活性.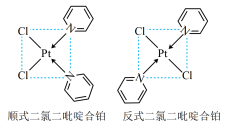
 键
键 ,吡啶中
,吡啶中 原子的价层孤电子对占据
原子的价层孤电子对占据②二氯二吡啶合铂分子中存在的微粒间作用力有
a.离子键 b.配位键 c.金属键
d.非极性键 e.氢键 f.极性键
③反式二氯二吡啶合铂分子是
(4)
 、
、 、
、 的酸性随羟基极性的增大而增强,则酸性从强到弱的排序为
的酸性随羟基极性的增大而增强,则酸性从强到弱的排序为
您最近一年使用:0次
名校
5 . 工业上电解氧化铝时常加入冰晶不,制取冰晶石的反应方程式为: ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A. 的VSEPR模型为V形 的VSEPR模型为V形 |
B. 在水中的电离方程式为: 在水中的电离方程式为: |
C.由铝原子核形成的下列三种微粒:a. b. b. ,再失去一个电子所需最低能量由大到小的顺序是: ,再失去一个电子所需最低能量由大到小的顺序是: |
D. 为直线形结构,分子中存在大 为直线形结构,分子中存在大 键: 键: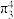 |
您最近一年使用:0次
2024-02-27更新
|
198次组卷
|
2卷引用:山东省青岛第五十八中学2023-2024学年高二上学期期末化学试卷
名校
解题方法
6 . 元素A、D、E、W、X、Y、Z基态原子,原子序数依次增大且分占前四周期,D的各能级电子数相等;E的核外电子有3种空间运动状态。W的价电子排布式为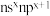 ,X的最高能级的单电子数是A的3倍,Y的最高价氧化物水化物酸性最强,Z与A中的单电子数(不为0)和最外层电子数均相同,但两者族序数不同。请用化学用语回答下列问题:
,X的最高能级的单电子数是A的3倍,Y的最高价氧化物水化物酸性最强,Z与A中的单电子数(不为0)和最外层电子数均相同,但两者族序数不同。请用化学用语回答下列问题:
(1)Z元素在周期表中的位置为:___________ ;位于周期表___________ 区。
(2)D、E、W元素第一电离能由大到小顺序为:___________ ;电负性由大到小顺序为:___________ 。
(3)比较键角:
___________  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(4)实验测得:ZY属于共价化合物,气态ZY分子的相对分子质量为199,该分子中含有配位键,则气态ZY分子的结构式可能为___________ 。
(5)某物质晶胞结构如图所示。
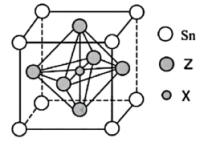
①该物质的化学式可以表示为___________ 。
②该晶胞中距离最近的 与Z原子的核间距为
与Z原子的核间距为 ,则该晶胞的密度为
,则该晶胞的密度为___________  (用含a、
(用含a、 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, )。
)。
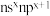 ,X的最高能级的单电子数是A的3倍,Y的最高价氧化物水化物酸性最强,Z与A中的单电子数(不为0)和最外层电子数均相同,但两者族序数不同。请用化学用语回答下列问题:
,X的最高能级的单电子数是A的3倍,Y的最高价氧化物水化物酸性最强,Z与A中的单电子数(不为0)和最外层电子数均相同,但两者族序数不同。请用化学用语回答下列问题:(1)Z元素在周期表中的位置为:
(2)D、E、W元素第一电离能由大到小顺序为:
(3)比较键角:

 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)(4)实验测得:ZY属于共价化合物,气态ZY分子的相对分子质量为199,该分子中含有配位键,则气态ZY分子的结构式可能为
(5)某物质晶胞结构如图所示。

①该物质的化学式可以表示为
②该晶胞中距离最近的
 与Z原子的核间距为
与Z原子的核间距为 ,则该晶胞的密度为
,则该晶胞的密度为 (用含a、
(用含a、 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, )。
)。
您最近一年使用:0次
7 .  可发生水解反应
可发生水解反应 .下列说法错误的是
.下列说法错误的是
 可发生水解反应
可发生水解反应 .下列说法错误的是
.下列说法错误的是A. 、 、 分子中键角较大的是 分子中键角较大的是 | B. 是由极性键构成的极性分子 是由极性键构成的极性分子 |
C.质量数为35的Cl原子可表示为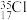 | D.HClO的电子式为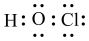 |
您最近一年使用:0次
名校
8 . 含元素R的微粒可发生如下反应: 下列说法错误的是
下列说法错误的是
 下列说法错误的是
下列说法错误的是| A.R元素的最高化合价为+7 | B.RO 的空间结构为三角锥形 的空间结构为三角锥形 |
| C.R2在常温常压下一定是气体 | D.R元素位于周期表中的s区 |
您最近一年使用:0次
名校
9 . 磷化氢(PH3)是一种无色剧毒,有类似大蒜气味的气体,微溶于冷水。下列关于PH3的叙述错误的是
| A.PH3分子中有未成键的电子对 |
| B.PH3是极性分子 |
| C.PH3分子结构为三角锥形 |
| D.PH3中共价键的键长比NH3的短 |
您最近一年使用:0次
解题方法
10 . 三氟化氯(ClF3)是极强助燃剂,能自耦电离:2ClF3 ClF
ClF +ClF
+ClF ,其分子空间结构如图。下列推测合理的是
,其分子空间结构如图。下列推测合理的是
 ClF
ClF +ClF
+ClF ,其分子空间结构如图。下列推测合理的是
,其分子空间结构如图。下列推测合理的是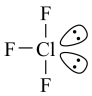
| A.ClF3分子是含有极性键的非极性分子 |
| B.BrF3比ClF3更易发生自耦电离 |
| C.ClF3水解反应的产物为HCl和HFO |
D.ClF 与H2O、ClF 与H2O、ClF 与CCl4的空间结构分别相同 与CCl4的空间结构分别相同 |
您最近一年使用:0次



