名校
1 . 工业上电解氧化铝时常加入冰晶不,制取冰晶石的反应方程式为: ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A. 的VSEPR模型为V形 的VSEPR模型为V形 |
B. 在水中的电离方程式为: 在水中的电离方程式为: |
C.由铝原子核形成的下列三种微粒:a. b. b. ,再失去一个电子所需最低能量由大到小的顺序是: ,再失去一个电子所需最低能量由大到小的顺序是: |
D. 为直线形结构,分子中存在大 为直线形结构,分子中存在大 键: 键: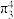 |
您最近一年使用:0次
2024-02-27更新
|
198次组卷
|
2卷引用:山东省东营市利津县高级中学2023-2024学年高二下学期开学考试化学试题
2 . 铁及其配合物在科研、生产中有着重要的应用。回答以下问题:
(1)写出Fe在元素周期表中的位置___________ 。
(2) 能与
能与 形成
形成 ,其中
,其中 电负性从大到小的顺序是
电负性从大到小的顺序是___________ , 离子的空间构型为
离子的空间构型为___________ 。
(3)邻二氮菲(phen, )能与
)能与 形成橙红色的配合物离子,可表示为
形成橙红色的配合物离子,可表示为 ,常用于
,常用于 定量检测。1mol该配合物离子中有
定量检测。1mol该配合物离子中有___________ mol配位键。某研究小组向反应后的溶液中滴加少量稀硫酸,溶液颜色变浅,简要说明原因:___________ 。
(4)配合物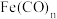 的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应:
的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应: 。
。
①分解反应过程中断裂的化学键只有配位键,形成的化学键是___________ 。
②写出配体CO的结构式___________ ,1mol该配合物中含有的 键数目为
键数目为___________ 。
(1)写出Fe在元素周期表中的位置
(2)
 能与
能与 形成
形成 ,其中
,其中 电负性从大到小的顺序是
电负性从大到小的顺序是 离子的空间构型为
离子的空间构型为(3)邻二氮菲(phen,
 )能与
)能与 形成橙红色的配合物离子,可表示为
形成橙红色的配合物离子,可表示为 ,常用于
,常用于 定量检测。1mol该配合物离子中有
定量检测。1mol该配合物离子中有(4)配合物
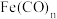 的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应:
的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应: 。
。①分解反应过程中断裂的化学键只有配位键,形成的化学键是
②写出配体CO的结构式
 键数目为
键数目为
您最近一年使用:0次
名校
解题方法
3 . 同一周期主族元素W、Z、X、Y原子序数依次增大,X原子的最外层电子数是W原子的次外层电子数的3倍,由四种元素原子形成的阴离子结构如图,下列说法正确的是
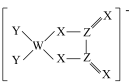
| A.Z位于元素周期表第2周期ⅥA族 | B.以W为中心原子形成的VSEPR模型为平面三角形 |
| C.该阴离子中含有配位键 | D.最高价氧化物对应水化物的酸性:Y>Z>W |
您最近一年使用:0次
2024-02-01更新
|
223次组卷
|
3卷引用:山东省东营市利津县高级中学2023-2024学年高二下学期开学考试化学试题
名校
解题方法
4 . 有五种元素X、Y、Z、Q、T。X元素为主族元素,基态X原子的M电子层上有两个未成对电子且无空轨道;基态Y原子的价层电子排布为 ;基态Z原子的L电子层的p能级上有一个空轨道;基态Q原子的L电子层的p能级上只有一对成对电子;基态T原子的M电子层上p轨道为半充满状态。下列叙述不正确的是
;基态Z原子的L电子层的p能级上有一个空轨道;基态Q原子的L电子层的p能级上只有一对成对电子;基态T原子的M电子层上p轨道为半充满状态。下列叙述不正确的是
 ;基态Z原子的L电子层的p能级上有一个空轨道;基态Q原子的L电子层的p能级上只有一对成对电子;基态T原子的M电子层上p轨道为半充满状态。下列叙述不正确的是
;基态Z原子的L电子层的p能级上有一个空轨道;基态Q原子的L电子层的p能级上只有一对成对电子;基态T原子的M电子层上p轨道为半充满状态。下列叙述不正确的是| A.Y和Q可形成化合物Y2Q3 |
B.最高价氧化物对应水化物的酸性: |
| C.X和Q结合生成的化合物为离子化合物 |
| D. ZQ2是极性键构成的直线形分子 |
您最近一年使用:0次



