解题方法
1 . 下列说法正确的是
A. 和 和 的中心原子的价层电子对数均为4 的中心原子的价层电子对数均为4 |
B. 能与 能与 以配位键结合是因为 以配位键结合是因为 中氮原子有孤电子对 中氮原子有孤电子对 |
C. 的熔点高于 的熔点高于 是因为 是因为 键的键能比 键的键能比 大 大 |
D.氨水中存在 是因为 是因为 是离子化合物 是离子化合物 |
您最近一年使用:0次
名校
解题方法
2 . A、B、C、D为原子序数依次增大的四种短周期元素,A2-和B+具有相同的电子层结构,C、D为同周期元素,C元素原子核外电子总数是最外层电子数的3倍;D元素同周期中原子半径最小的元素。回答下列问题:
(1)四种元素中电负性最大的是_______ (填元素符号),其中C原子的核外电子排布式为_______ 。
(2)A的两种单质互为同素异形体,其中沸点高的是_______ (填分子式),原因是_______ ;A和B的氢化物所属的晶体类型分别为_______ 和_______ 。
(3)C和D可按原子个数比为1∶3形成化合物E,E的空间结构为_______ ,中心原子的杂化轨道类型为_______ 。
(4)化合物D2A的空间结构为_______ ,中心原子的价层电子对数为_______ ;
(5)面心立方ZnS晶胞与金刚石的晶胞结构类似,阴、阳离子各占晶胞所含粒子数的一半。
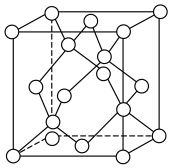
若该ZnS晶胞的晶胞参数为a pm,阿伏加德罗常数的值为NA,则晶体的密度为_______ g·cm-3。
(1)四种元素中电负性最大的是
(2)A的两种单质互为同素异形体,其中沸点高的是
(3)C和D可按原子个数比为1∶3形成化合物E,E的空间结构为
(4)化合物D2A的空间结构为
(5)面心立方ZnS晶胞与金刚石的晶胞结构类似,阴、阳离子各占晶胞所含粒子数的一半。

若该ZnS晶胞的晶胞参数为a pm,阿伏加德罗常数的值为NA,则晶体的密度为
您最近一年使用:0次
3 . 反应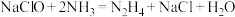 可用于制备火箭和燃料电池的燃料肼(
可用于制备火箭和燃料电池的燃料肼( )。下列说法正确的是
)。下列说法正确的是
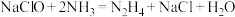 可用于制备火箭和燃料电池的燃料肼(
可用于制备火箭和燃料电池的燃料肼( )。下列说法正确的是
)。下列说法正确的是A. 的电子式为 的电子式为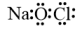 | B. 的中子数为14 的中子数为14 |
C. 的结构式为 的结构式为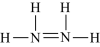 | D. 的VSEPR模型为 的VSEPR模型为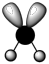 |
您最近一年使用:0次
解题方法
4 . X、Y、Z、W是原子序数依次增大的短周期元素,X的2p轨道有两个未成对电子,Y元素原子半径在同周期中最大,X与Y最外层电子数之和与Z的最外层电子数相等,在地壳的岩层中存在元素W的游离态。下列说法正确的是
A.第一电离能: ,电负性: ,电负性: |
| B.Y、W形成的化合物中只存在离子键 |
| C.X、Z、W的单质形成的晶体类型相同,均为分子晶体 |
| D.X、W形成的一种离子呈平面三角形,则中心原子价层电子对数为3 |
您最近一年使用:0次
解题方法
5 . 氧族元素包括氧、硫、硒等,这些元素的单质及其化合物在工农业生产和科学研究中具有广泛的用途。回答下列问题:
(1)下列属于氧原子激发态的轨道表示式的有___________ (填字母,下同),其中失去最外层上一个电子所需能量最低的是___________ 。
a. b.
b.
c.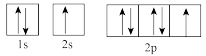 d.
d.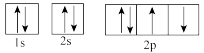
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
① 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的___________ 杂化轨道形成S—S___________ (填“ ”或“
”或“ ”)共价键。
”)共价键。
② 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角___________ (填“=”“>”或“<”) 。
。
③ 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是___________ 。
(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:
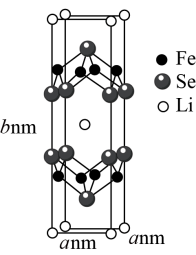
1个晶胞中的Se原子数为___________ 。晶胞的部分参数如图所示,且晶胞棱边夹角均为90°,晶体密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为___________ (列式表示)。
(1)下列属于氧原子激发态的轨道表示式的有
a.
 b.
b.
c.
 d.
d.
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
| 物质 | 熔点/℃ | 沸点/℃ |  制备方法 制备方法 |
 | -90.0 | 71.0 | 加热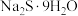 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 |
 | -0.4 | 150.0 |
 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的 ”或“
”或“ ”)共价键。
”)共价键。②
 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角 。
。③
 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:

1个晶胞中的Se原子数为
 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
6 . 化学用语是学习化学的重要工具,以下化学用语表述正确的是
A. 的空间填充模型: 的空间填充模型: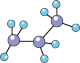 |
| B.HClO分子的VSEPR模型:直线形 |
C.基态 的价电子轨道表示式: 的价电子轨道表示式: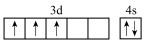 |
D.1,3-丁二烯的键线式: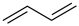 |
您最近一年使用:0次
名校
7 . 下列关于杂化轨道的叙述中,不正确的是( )
| A.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构 |
| B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
| C.NH3和CH4两个分子中中心原子N和C都是通过sp3杂化轨道成键 |
D.ClO 的立体构型为平面三角形 的立体构型为平面三角形 |
您最近一年使用:0次
2023-06-08更新
|
76次组卷
|
2卷引用:广东省梅州市兴宁市齐昌中学2022-2023学年高三上学期第二次质检考试化学试题
名校
8 . 某种电化学的电解液的组成如图所示,X、Y、Z、Q、W为原子序数依次增大的短周期元素,下列说法正确的是


A.电解熔融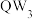 可获得Q的单质 可获得Q的单质 | B.原子半径: |
| C.W的含氧酸均为强酸 | D.QW 的空间构型为正四面体 的空间构型为正四面体 |
您最近一年使用:0次
2023-03-04更新
|
397次组卷
|
4卷引用:江苏省扬州中学2022-2023学年高三上学期11月月考化学试题
2023高三·全国·专题练习
名校
9 . 某种净水剂由原子序数依次增大的R、W、X、Y、Z五种主族元素组成。五种元素分处三个短周期,且包含地壳中含量前三的三种元素。五种元素原子的最外层电子数之和为20。下列说法正确的是
A.简单离子半径: |
B.最简单氢化物的稳定性: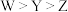 |
| C.R分别与W、Z形成的三原子分子均为V形分子 |
D.常见单质的熔点: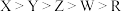 |
您最近一年使用:0次
名校
解题方法
10 . 下列表示不正确的是
A.绿矾的化学式为 | B.氧原子的核外电子轨道表示式: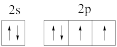 |
C. 为极性分子 为极性分子 | D. 的VSEPR模型: 的VSEPR模型: |
您最近一年使用:0次



