名校
解题方法
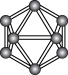
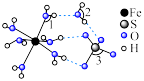
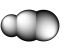
1 . 观察下列模型并结合信息,判断有关说法错误的是
| 晶体硼结构单元(有12个B原子) |  |  分子 分子 | HCN | |
| 结构模型示意图 |
|
|
|
|
A.晶体硼的结构单元中含有30个 键,含20个正三角形 键,含20个正三角形 |
B. 结构中键角1、2、3由大到小的顺序:3>1>2 结构中键角1、2、3由大到小的顺序:3>1>2 |
C.固态硫 中S原子为 中S原子为 杂化 杂化 |
D. 的结构式为 的结构式为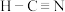 |
您最近一年使用:0次
2024-03-30更新
|
1153次组卷
|
2卷引用:山西省大同市第一中学校2023-2024学年高二下学期3月月考化学试题
2 .  、
、 都是重要的有机反应中间体,下列说法正确的是
都是重要的有机反应中间体,下列说法正确的是
 、
、 都是重要的有机反应中间体,下列说法正确的是
都是重要的有机反应中间体,下列说法正确的是A. 的球棍模型为 的球棍模型为 | B. 中C-H为 中C-H为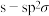 |
C. 中键角为109°28′ 中键角为109°28′ | D. 与 与 形成的化合物中含有离子键 形成的化合物中含有离子键 |
您最近一年使用:0次
3 . 甲醛(HCHO)、过氧乙酸(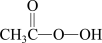 )、次氯酸钙
)、次氯酸钙 均可用于杀菌消毒,下列说法正确的是
均可用于杀菌消毒,下列说法正确的是
| A.甲醛分子的空间结构:三角锥形 |
B.过氧乙酸分子中所有碳原子的杂化类型: 、 、 |
C.基态氯原子的价层电子排布式: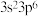 |
| D.基态钙原子占据的最高能级轨道形状:哑铃形 |
您最近一年使用:0次
4 . 近年,我国科学家通过热磷化法制备出了电催化分解水的催化剂Co-Fe-P和Ni-Fe-P等过渡金属磷化物,将推动电解水制氢技术的快速发展。回答下列问题:
(1)铁元素在元素周期表中的位置_______ ,Fe3+的价电子排布式_______ 。
(2)磷的一些卤化物的熔沸点如表所示,试解释PF3、PCl3、PBr3、PI3熔沸点逐渐升高的原因_______
(3)磷酸具有很强的配位能力,PO 的中心原子杂化类型为
的中心原子杂化类型为_______ ,写出与PO 互为等电子体的一种分子
互为等电子体的一种分子_______
(4)钴的配合物种类很多,如[Co(NO2)(NH3)5]Cl2和[Co(NH3)4Cl2]Cl等,[Co(NO2)(NH3)5]2+的配位数是_______ ,其配体中的NH3的分子空间构型为_______ ;等物质的量的[Co(NO2)(NH3)5]Cl2和[Co(NH3)4Cl2]Cl分别与足量的硝酸银溶液反应,两者生成氯化银的质量比为_______ 。
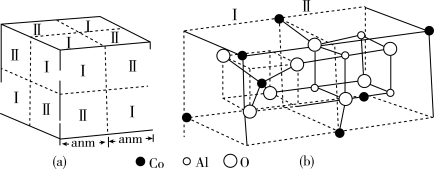
(5)钴蓝晶体结构如图(a)所示,该立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,求晶体的化学式为_______ ,密度为_______ g·cm-3。
(1)铁元素在元素周期表中的位置
(2)磷的一些卤化物的熔沸点如表所示,试解释PF3、PCl3、PBr3、PI3熔沸点逐渐升高的原因
| 卤化磷 | 熔点/K | 沸点/K |
| PF3 | 121.5 | 171.5 |
| PCl3 | 161 | 348.5 |
| PBr3 | 233 | 451.2 |
| PI3 | 334 | 573 |
 的中心原子杂化类型为
的中心原子杂化类型为 互为等电子体的一种分子
互为等电子体的一种分子(4)钴的配合物种类很多,如[Co(NO2)(NH3)5]Cl2和[Co(NH3)4Cl2]Cl等,[Co(NO2)(NH3)5]2+的配位数是
(5)钴蓝晶体结构如图(a)所示,该立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,求晶体的化学式为

您最近一年使用:0次
名校
解题方法
5 . 前四周期的A、B、C、D四种元素在周期表中均与元素X紧密相邻。已知元素X最高价氧化物的化学式为X2O5,B、D同主族且B元素的原子半径是同族元素中最小的,C的最高价氧化物对应的水化物是强酸(本题中出现的 B 、 C 均为字母,不是元素符号 )。
(1)D元素基态原子的外围电子排布式为____________________ 。
(2)A、C、X三种元素原子的第一电离能由大到小的顺序为________________ (用相应的元素符号作答)。
(3)B、X、D氢化物的沸点由高到低的顺序为_______________ (用相应的化学式作答)。
(4)C元素的原子可形成多种离子,试推测下列微粒的立体构型(C为字母,不是碳元素):
(5)元素B的一种氢化物B2H4具有重要的用途。有关B2H4的说法正确的是___ 。
A.B2H4分子间可形成氢键 B.B原子是sp3杂化
C.B2H4分子中含有5个σ键和1个π键 D.B2H4晶体变为液态时破坏共价键
(6)E元素和D元素在同一周期,属于VIII族,价层有三个单电子,E(OH)2为两性氢氧化物,在浓的强碱溶液中可形成E(OH)42-,写出E(OH)2酸式电离的电离方程式_____________________________ 。
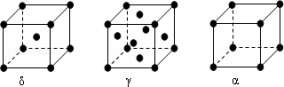
(7)F元素基态原子M层上有5对成对电子,F形成的单质有δ、γ、α三种同素异形体,三种晶胞(如下图所示)中F原子的配位数之比为___________ ,δ、γ、α三种晶胞的边长之比为_____________ 。
(1)D元素基态原子的外围电子排布式为
(2)A、C、X三种元素原子的第一电离能由大到小的顺序为
(3)B、X、D氢化物的沸点由高到低的顺序为
(4)C元素的原子可形成多种离子,试推测下列微粒的立体构型(C为字母,不是碳元素):
| 微粒 | CO32- | CO42- |
| 立体构型名称 |
(5)元素B的一种氢化物B2H4具有重要的用途。有关B2H4的说法正确的是
A.B2H4分子间可形成氢键 B.B原子是sp3杂化
C.B2H4分子中含有5个σ键和1个π键 D.B2H4晶体变为液态时破坏共价键
(6)E元素和D元素在同一周期,属于VIII族,价层有三个单电子,E(OH)2为两性氢氧化物,在浓的强碱溶液中可形成E(OH)42-,写出E(OH)2酸式电离的电离方程式
(7)F元素基态原子M层上有5对成对电子,F形成的单质有δ、γ、α三种同素异形体,三种晶胞(如下图所示)中F原子的配位数之比为

您最近一年使用:0次
2017-05-24更新
|
469次组卷
|
4卷引用:山西省山西大学附属中学2017届高三下学期3月模块诊断理科综合化学试题