解题方法
1 . X、Y、Z、J、Q、W为前四周期元素,原子序数依次增大。元素Y在地壳中含量最高,W的一种常见高价氧化物是红棕色粉末,常用于油漆、涂料、油墨的红色染料,25℃X、Z、J、Q的最高价氧化物对应水化物溶液(浓度均为0.01mol·L-1)的pH与原子序数的关系如图所示。

根据上述信息进行判断,并回答下列问题:
(1)W在周期表中的位置__ 。比较X、Y、Z的简单离子半径大小为__ <____ <__ (用离子符号表示);
(2)元素的非金属性Y__ J(填“>”或“<”)。下列各项中,不能说明这一结论的有__ (填序号)。
A.J的氢化物的水溶液放置在空气中会变浑浊
B.Y与J之间形成的化合物中元素的化合价。
C.Y和J的单质的状态
D.Y和J在周期表中的位置
(3)X、J、Q这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是_____ (填化学式);酸根呈三角锥结构的酸是___ (填化学式)。
(4)Y和Q形成的化合物Q2Y的立体构型为__ ,Q的单质与湿润的Na2CO3反应可制备Q2Y,其化学方程式为___ 。

根据上述信息进行判断,并回答下列问题:
(1)W在周期表中的位置
(2)元素的非金属性Y
A.J的氢化物的水溶液放置在空气中会变浑浊
B.Y与J之间形成的化合物中元素的化合价。
C.Y和J的单质的状态
D.Y和J在周期表中的位置
(3)X、J、Q这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是
(4)Y和Q形成的化合物Q2Y的立体构型为
您最近一年使用:0次
2019-11-28更新
|
306次组卷
|
2卷引用:山东省烟台市2020届高三上学期期中考试化学试题
名校
解题方法
2 . 周期表中的五种元素 A、B、C、D、E、F,A是宇宙中含量最多的元素,D是地壳中含量最多的元素,B 的基态原子价层电子排布为 nsnnpn;C是基态原子含有未成对电子数目最多的第二周期元素;E的基态原子M层填满电子,N层仅有2个电子;F位于第六周期,与Cu 同族,其单质在金属活动性顺序表中排在末位。
(1)写出 E的基态原子的价层电子排布式________________ ;
(2)B、C 形成的BC-常作为配位化合物中的配体,BC-中B原子的杂化方式为_________ ,BC-中含有的σ键与π键的数目之比为____________ ,其等电子体有_________ (填2个);
(3)A、B、C三种元素的电负性由小到大的顺序为______________________________ ;
(4)D3分子的立体构型为____________ ;
(5)E、F 均能与 BC-形成配离子。E 与 BC-形成的是四配位离子,工业上常用 F 和BC-形成的配离子(直线形)与 E 反应来提取 F 单质,写出E置换F的离子方程式_________________________________ 。
(1)写出 E的基态原子的价层电子排布式
(2)B、C 形成的BC-常作为配位化合物中的配体,BC-中B原子的杂化方式为
(3)A、B、C三种元素的电负性由小到大的顺序为
(4)D3分子的立体构型为
(5)E、F 均能与 BC-形成配离子。E 与 BC-形成的是四配位离子,工业上常用 F 和BC-形成的配离子(直线形)与 E 反应来提取 F 单质,写出E置换F的离子方程式
您最近一年使用:0次
解题方法
3 . A、B、C、D、E、F、G是前四周期的七种元素,其原子序数依次增大。A的基态原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D及其同主族元素的氢化物沸点变化趋势如图(D的氢化物沸点最高);F是地壳中含量最高的金属元素;G与F同主族。请回答下列问题:
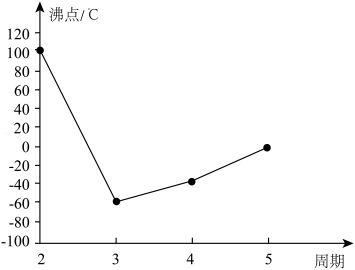
(1)写出F元素基态原子的核外电子排布式:____________ 。
(2)B、C、D三种元素电负性由大到小的顺序是____________ (用元素符号表示)。
(3)有关上述元素的下列说法,正确的是________ (填序号)。
①CA3沸点高于BA4,主要是因为前者相对分子质量较大
②配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于离子晶体
③C的氢化物的中心原子采取sp2杂化
④F单质的熔点高于E单质,是因为F单质的金属键较强
⑤比G的原子序数少1的元素第一电离能高于G
(4)CA3分子的立体构型为________ ,1 mol B2A4分子中含有________ 个σ键;

(1)写出F元素基态原子的核外电子排布式:
(2)B、C、D三种元素电负性由大到小的顺序是
(3)有关上述元素的下列说法,正确的是
①CA3沸点高于BA4,主要是因为前者相对分子质量较大
②配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于离子晶体
③C的氢化物的中心原子采取sp2杂化
④F单质的熔点高于E单质,是因为F单质的金属键较强
⑤比G的原子序数少1的元素第一电离能高于G
(4)CA3分子的立体构型为
您最近一年使用:0次
解题方法
4 . 已知:周期表中前四周期的六种元素A、B、C、D、E、F核电荷数依次增大,其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F2+离子核外各层电子均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序为____ 。(用元素符号表示)
(2)B的氯化物的熔点比D的氯化物的熔点高,理由是____________________ 。
(3)E的最高价氧化物分子的空间构型是__________ ,是____ 分子(填“极性”“非极性”)。
(4)F原子的核外电子排布式是________________ 。
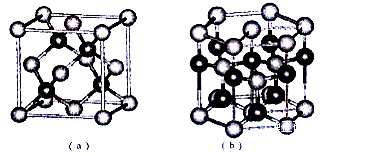
(5)E、F形成某种化合物有如图所示两种晶体结构(深色球表示F原子),其化学式为_________ 。(a)中E原子的配位数为____ 。若在(b)的结构中取出一个平行六面体作为晶胞,则平均一个晶胞中含有____ 个F原子。结构(a)与(b)中晶胞的原子空间利用率相比,(a)____ (b)(填“>”“<”或“=”)。
(1)A、B、C、D的第一电离能由小到大的顺序为
(2)B的氯化物的熔点比D的氯化物的熔点高,理由是
(3)E的最高价氧化物分子的空间构型是
(4)F原子的核外电子排布式是
(5)E、F形成某种化合物有如图所示两种晶体结构(深色球表示F原子),其化学式为

您最近一年使用:0次
2017-10-07更新
|
227次组卷
|
3卷引用:河北省五校联盟2018届高三上学期摸底考试理综化学试题
名校
解题方法
5 . 前四周期元素A、B、C、D、E、F的原子序数依次增大,A是宇宙中含量最丰富的元素;B和C同一主族,且B的L层电子数是K层电子数的2.5倍;D和C同一周期;E元素原子核外电子有17种不同的运动状态,F位于第四周期,其未成对电子数只有一个,且内层都处于全充满状态。请回答下列问题:
(1)B原子的L层轨道表达式_________ ;D元素原子的价电子排布式是___________ 。
(2)由A、B原子形成的分子的结构式为:A-B=B-A,则该分子中σ键和π键的数目之比为_____ , B、C的氢化物中BH3的沸点高于 CH3的沸点,原因是______ ;C、D和E的电负性由大到小的顺序为______ ;C、D和E的第一电离能由大到小的顺序是______ ;C和D最高价含氧酸的酸性由弱到强的顺序为_________ 。CO 中C的杂化方式为
中C的杂化方式为________ ,该离子的“VSEPR”模型为__________ 形。
(3)向FDO4溶液中加入过量稀氨水,得到的深蓝色溶液中阳离子化学式为_________ ,该离子的配位体为____________ 。
(4)D(黑球)和F(白球)形成的某种晶体的晶胞如图所示,已知该晶胞的棱长为516 pm,则该晶胞的密度为___________ g/cm3,(列出计算式即可,不必计算结果,阿伏伽德罗常数值为NA),最近的黑球和白球之间的距离为____________ pm。

(1)B原子的L层轨道表达式
(2)由A、B原子形成的分子的结构式为:A-B=B-A,则该分子中σ键和π键的数目之比为
 中C的杂化方式为
中C的杂化方式为(3)向FDO4溶液中加入过量稀氨水,得到的深蓝色溶液中阳离子化学式为
(4)D(黑球)和F(白球)形成的某种晶体的晶胞如图所示,已知该晶胞的棱长为516 pm,则该晶胞的密度为

您最近一年使用:0次
2017-05-22更新
|
301次组卷
|
3卷引用:新疆生产建设兵团第二中学2016-2017学年高二下学期第四次月考化学试题



