名校
解题方法
1 . 按要求回答下列问题:
(1)A.乙烷 B.乙烯 C.乙炔 D.苯是有机化学中的代表物质,其中:
①既有 键又有
键又有 键的是
键的是_______ (填序号,下同)。
②碳碳键的键长由大到小排序是:_______ 。
③上述分子中所有原子均在同一平面是:_______ 。
(2)含硫元素的微粒有很多,例如 、
、 、
、 、
、 、
、 ,其中
,其中 的分子结构如下图所示,像一顶皇冠,请回答下列问题:
的分子结构如下图所示,像一顶皇冠,请回答下列问题: 中含有的
中含有的 键数目是
键数目是_______ 。
② 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是_______ , 的空间结构是
的空间结构是_______ 。
③ 分子的VSEPR模型是
分子的VSEPR模型是_______ , 是
是_______ (填“极性”或“非极性”)分子。
④沸点:
_______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是_______ 。
(1)A.乙烷 B.乙烯 C.乙炔 D.苯是有机化学中的代表物质,其中:
①既有
 键又有
键又有 键的是
键的是②碳碳键的键长由大到小排序是:
③上述分子中所有原子均在同一平面是:
(2)含硫元素的微粒有很多,例如
 、
、 、
、 、
、 、
、 ,其中
,其中 的分子结构如下图所示,像一顶皇冠,请回答下列问题:
的分子结构如下图所示,像一顶皇冠,请回答下列问题: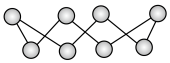
 中含有的
中含有的 键数目是
键数目是②
 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是 的空间结构是
的空间结构是③
 分子的VSEPR模型是
分子的VSEPR模型是 是
是④沸点:

 (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是
您最近一年使用:0次
名校
解题方法
2 . 下列粒子中,与 分子的空间构型相同的是
分子的空间构型相同的是
 分子的空间构型相同的是
分子的空间构型相同的是A. | B. | C. | D. |
您最近一年使用:0次
名校
解题方法
3 . 二氟化氧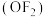 的键角为
的键角为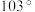 ,是一种无色的剧毒气体,能发生反应:
,是一种无色的剧毒气体,能发生反应: ,下列有关说法正确的是。
,下列有关说法正确的是。
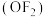 的键角为
的键角为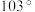 ,是一种无色的剧毒气体,能发生反应:
,是一种无色的剧毒气体,能发生反应: ,下列有关说法正确的是。
,下列有关说法正确的是。A. 难溶于 难溶于 | B. 的键角大于 的键角大于 |
C. 分子中O与F之间存在的是氢键 分子中O与F之间存在的是氢键 | D. 的VSEPR模型名称为正四面体形 的VSEPR模型名称为正四面体形 |
您最近一年使用:0次
4 . 硒( )是人体必需的微量元素,它能有效提高人体免疫机能,抑制癌症和心脑血管等疾病的发病率,下列有关说法错误的是
)是人体必需的微量元素,它能有效提高人体免疫机能,抑制癌症和心脑血管等疾病的发病率,下列有关说法错误的是
 )是人体必需的微量元素,它能有效提高人体免疫机能,抑制癌症和心脑血管等疾病的发病率,下列有关说法错误的是
)是人体必需的微量元素,它能有效提高人体免疫机能,抑制癌症和心脑血管等疾病的发病率,下列有关说法错误的是A.硒的最高价氧化物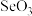 所有原子处于同一平面上 所有原子处于同一平面上 |
| B.基态硒元素原子核外电子所占据的最高能级的电子云轮廓图为哑铃形 |
| C.硒元素位于元素周期表中第Ⅵ族 |
| D.O和Se均为p区非金属元素 |
您最近一年使用:0次
名校
5 .  为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是A.标准状况下,22.4L乙炔中 键数为 键数为 、 、 键数为 键数为 |
B.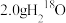 与 与 的混合物中含有的中子数为 的混合物中含有的中子数为 |
C.含 的冰中含有氢键的数目为 的冰中含有氢键的数目为 |
D.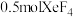 中氙的价层电子对数为 中氙的价层电子对数为 |
您最近一年使用:0次
名校
解题方法
6 . 有机反应过程中,随反应条件不同,成键的碳原子可以形成碳正离子( )、碳负离子(
)、碳负离子( )、甲基(
)、甲基( )等微粒。下列说法不正确的是
)等微粒。下列说法不正确的是
 )、碳负离子(
)、碳负离子( )、甲基(
)、甲基( )等微粒。下列说法不正确的是
)等微粒。下列说法不正确的是A. 中含有7mol电子 中含有7mol电子 |
B. 中所有的原子不都在一个平面内 中所有的原子不都在一个平面内 |
C. 的空间构型为平面三角形 的空间构型为平面三角形 |
D.键角: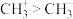 |
您最近一年使用:0次
7 . 现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素。请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有___________ 个方向,C简单离子核外有___________ 种运动状态不同的电子。
(2) 难溶于二硫化碳,简要说明理由
难溶于二硫化碳,简要说明理由___________ 。
(3) 分子的空间构型为
分子的空间构型为___________ , 分子的VSEPR模型名称为
分子的VSEPR模型名称为___________ 。
(4)下列气态分子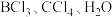 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为___________ 。
| 元素 | 相关信息 |
| A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 原子核外P电子数与s电子数相等 |
| C | 基态原子的价电子排布为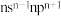 |
| D | 能层数与C相同,且电负性比C大 |
| E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)
 难溶于二硫化碳,简要说明理由
难溶于二硫化碳,简要说明理由(3)
 分子的空间构型为
分子的空间构型为 分子的VSEPR模型名称为
分子的VSEPR模型名称为(4)下列气态分子
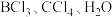 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为
您最近一年使用:0次
名校
解题方法
8 . 我国科学家成功合成了世界上首个五氮阴离子盐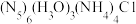 ,其局部结构如下图所示,下列说法中错误的是
,其局部结构如下图所示,下列说法中错误的是
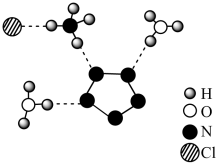
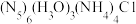 ,其局部结构如下图所示,下列说法中错误的是
,其局部结构如下图所示,下列说法中错误的是
A.该化合物中两种阳离子的中心原子均采取 杂化 杂化 |
| B.该化合物中两种阳离子的空间构型分别为正四面体形和三角锥形 |
C.阴离子 中的 中的 键总数为5个 键总数为5个 |
| D.该化合物中只存在共价键、氢键和配位键三种作用力 |
您最近一年使用:0次
2023-02-27更新
|
253次组卷
|
2卷引用:重庆市渝东九校联盟2021-2022学年高二下学期期中考试化学试题
名校
解题方法
9 . A~H元素在周期表中的位置如图所示,回答下列问题:

(1)G是地壳中含量第5的元素,在地壳中全部以化合态存在,其化合物的焰色反应为砖红色,这与G原子核外电子发生跃迁______ (填“吸收”或“释放”)能量有关。
(2)第一电离能介于C、D之间的第二周期元素有_______ 种。
(3)H被称为“人类的第三金属”,与H同周期且其基态原子的未成对电子数与H原子相同的元素另有_______ 种。
(4)D的某种氢化物(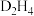 )可用作火箭燃料,燃烧时发生的反应是:
)可用作火箭燃料,燃烧时发生的反应是: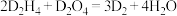 ,若该反应中有
,若该反应中有 电子转移,则形成的
电子转移,则形成的 键有
键有_______  。
。
(5) 是有机合成中常用的还原剂,
是有机合成中常用的还原剂,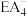 中E元素基态原子的价层电子轨道表示式为
中E元素基态原子的价层电子轨道表示式为______ ;离子半径:
______  (填“
(填“ ”或“
”或“ ”);
”); 中不存在
中不存在______ (填字母)。
A.离子键 B.共价键 C. 键 D.
键 D. 键 E.氢键
键 E.氢键
(6)F元素能形成多种含氧酸及盐,其中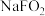 是常用的消毒剂,其酸根离子
是常用的消毒剂,其酸根离子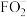 的价层电子对数为
的价层电子对数为______ ,空间构型为______ 。

(1)G是地壳中含量第5的元素,在地壳中全部以化合态存在,其化合物的焰色反应为砖红色,这与G原子核外电子发生跃迁
(2)第一电离能介于C、D之间的第二周期元素有
(3)H被称为“人类的第三金属”,与H同周期且其基态原子的未成对电子数与H原子相同的元素另有
(4)D的某种氢化物(
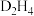 )可用作火箭燃料,燃烧时发生的反应是:
)可用作火箭燃料,燃烧时发生的反应是: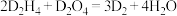 ,若该反应中有
,若该反应中有 电子转移,则形成的
电子转移,则形成的 键有
键有 。
。(5)
 是有机合成中常用的还原剂,
是有机合成中常用的还原剂,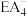 中E元素基态原子的价层电子轨道表示式为
中E元素基态原子的价层电子轨道表示式为
 (填“
(填“ ”或“
”或“ ”);
”); 中不存在
中不存在A.离子键 B.共价键 C.
 键 D.
键 D. 键 E.氢键
键 E.氢键(6)F元素能形成多种含氧酸及盐,其中
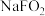 是常用的消毒剂,其酸根离子
是常用的消毒剂,其酸根离子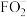 的价层电子对数为
的价层电子对数为
您最近一年使用:0次
名校
解题方法
10 . 价电子对互斥模型( 模型)可有效解释和预测分子的空间构型,下列解释均正确的是
模型)可有效解释和预测分子的空间构型,下列解释均正确的是
 模型)可有效解释和预测分子的空间构型,下列解释均正确的是
模型)可有效解释和预测分子的空间构型,下列解释均正确的是| 选项 | 分子 | 中心原子上价层电子对数 | 杂化轨道类型 | 分子的空间结构 |
| A |  | 4 |  | 平面正三角形 |
| B |  | 4 |  | 正四面体形 |
| C |  | 2 |  | 直线形 |
| D |  | 3 |  | 三角锥形 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



