解题方法
1 . 照相底片定影时,常用定影液硫代硫酸钠( )溶解未曝光的溴化银(
)溶解未曝光的溴化银( ),生成含
),生成含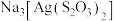 的废定影液再向其中加入
的废定影液再向其中加入 使
使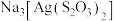 中的银转化为
中的银转化为 ,使定影液再生。将
,使定影液再生。将 在高温下转化为Ag,达到回收银的目的。回答下列问题:
在高温下转化为Ag,达到回收银的目的。回答下列问题:
(1)元素周期表中,铜、银、金位于同一副族相邻周期,则基态银原子的最外层电子排布式为__________________ 。
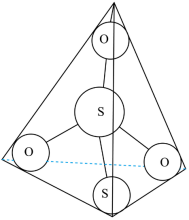
(2) 离子结构如图所示,其中心硫原子的杂化方式为
离子结构如图所示,其中心硫原子的杂化方式为___________ 。基态S原子中,核外电子占据的最高能级的符号是__________ ,占据最高能级电子的电子云轮廓图为________ 形。
(3)写出 溶于
溶于 溶液反应的离子方程式
溶液反应的离子方程式______ 。 中存在的作用力有离子键、共价键、
中存在的作用力有离子键、共价键、__________ 。
(4)在空气中灼烧 生成
生成 和
和 ,
, 分子的空间构型为
分子的空间构型为__________ 。分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数n代表参与形成大
键的原子数n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则
),则 中的大
中的大 键应表示为
键应表示为_________ 。
(5) 的键角小于
的键角小于 的键角,原因是
的键角,原因是_________________ 。
(6)用X射线衍射法可测定阿伏加 德罗常数。由金的X射线衍射图象可知金的晶胞属于面心立方晶胞。若金原子的半径为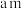 ,金的密度为
,金的密度为 ,摩尔质量为
,摩尔质量为 ,列出计算阿伏加 德罗常数的算式
,列出计算阿伏加 德罗常数的算式_________ (用含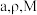 的表达式表示)。
的表达式表示)。
 )溶解未曝光的溴化银(
)溶解未曝光的溴化银( ),生成含
),生成含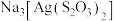 的废定影液再向其中加入
的废定影液再向其中加入 使
使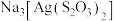 中的银转化为
中的银转化为 ,使定影液再生。将
,使定影液再生。将 在高温下转化为Ag,达到回收银的目的。回答下列问题:
在高温下转化为Ag,达到回收银的目的。回答下列问题:
(1)元素周期表中,铜、银、金位于同一副族相邻周期,则基态银原子的最外层电子排布式为
(2)
 离子结构如图所示,其中心硫原子的杂化方式为
离子结构如图所示,其中心硫原子的杂化方式为(3)写出
 溶于
溶于 溶液反应的离子方程式
溶液反应的离子方程式 中存在的作用力有离子键、共价键、
中存在的作用力有离子键、共价键、(4)在空气中灼烧
 生成
生成 和
和 ,
, 分子的空间构型为
分子的空间构型为 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数n代表参与形成大
键的原子数n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则
),则 中的大
中的大 键应表示为
键应表示为(5)
 的键角小于
的键角小于 的键角,原因是
的键角,原因是(6)用X射线衍射法可测定阿伏加 德罗常数。由金的X射线衍射图象可知金的晶胞属于面心立方晶胞。若金原子的半径为
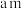 ,金的密度为
,金的密度为 ,摩尔质量为
,摩尔质量为 ,列出计算阿伏加 德罗常数的算式
,列出计算阿伏加 德罗常数的算式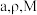 的表达式表示)。
的表达式表示)。
您最近一年使用:0次
名校
解题方法
2 . 据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属-绝缘体的转换。回答下列问题:
(1)锌和镉位于同副族,而锌与铜相邻。现有 4 种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10。失去1个电子需要的能量由大到小排序是______ (填字母)。
A.④②①③ B.④②③① C.①②④③ D.①④③②
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是_______ 。在硫的化合物中,H2S、CS2都是三原子分子,但它们的键角(立体构型)差别很大,用价层电子对互斥理论解释:_________ ;用杂化轨道理论解释:_________ 。
(3)Cd2+与NH3等配体形成配离子。[Cd(NH3)4]2+中2个NH3被2个Cl-替代只得到1种结构,它的立体构型是___________ 。1 mol [Cd(NH3)4]2+含___________ mol σ键。
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为__________ 。
(5)锆晶胞如图所示,1个晶胞含_______ 个Zr原子;这种堆积方式称为__________ 。
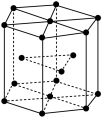
(6)镉晶胞如图所示。已知:NA是阿伏加 德罗常数的值,晶体密度为 d g·cm-3。在该晶胞中两个镉原子最近核间距为______ nm(用含NA、d的代数式表示),镉晶胞中原子空间利用率为________ (用含π的代数式表示)。
(1)锌和镉位于同副族,而锌与铜相邻。现有 4 种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10。失去1个电子需要的能量由大到小排序是
A.④②①③ B.④②③① C.①②④③ D.①④③②
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是
(3)Cd2+与NH3等配体形成配离子。[Cd(NH3)4]2+中2个NH3被2个Cl-替代只得到1种结构,它的立体构型是
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为
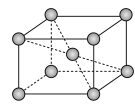
(5)锆晶胞如图所示,1个晶胞含

(6)镉晶胞如图所示。已知:NA是阿伏加 德罗常数的值,晶体密度为 d g·cm-3。在该晶胞中两个镉原子最近核间距为

您最近一年使用:0次
2020-04-23更新
|
370次组卷
|
3卷引用:陕西省安康市宁陕县宁陕中学2020届高三全仿真考试化学试题
名校
解题方法
3 . 铂钴合金是以铂为基含钴二元合金,在高温下,铂与钴可无限互溶,其固体为面心立方晶格。铂钴合金磁性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表、电子钟表、磁控管等。氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过____ 方法区分晶体准晶体和非晶体。
(2)基态F原子的价层电子排布图(轨道表达式)为______ 。
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为______ ,与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是______ (各举一例)。
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。NH4+中中心原子的杂化类型是______ ;氟化铵中存在______ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键
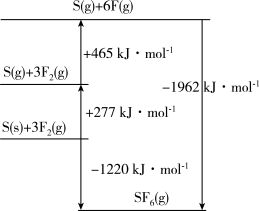
(5)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则F-F键的键能为______ kJ•mol-1,S-F键的键能为______ kJ•mol-1。
(6)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g•cm-3。
①CuF的熔点比CuCl的高,原因是______
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图(b)所示,则CuF的晶胞参数a=______ nm(列出计算式)。

(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态F原子的价层电子排布图(轨道表达式)为
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。NH4+中中心原子的杂化类型是
A.离子键 B.σ键 C.π键 D.氢键
(5)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则F-F键的键能为

(6)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g•cm-3。
①CuF的熔点比CuCl的高,原因是
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图(b)所示,则CuF的晶胞参数a=

您最近一年使用:0次
2019-11-13更新
|
271次组卷
|
4卷引用:陕西省洛南中学2020届高三第十次模拟理综化学试题
解题方法
4 . LED灯是一种环保的光源,在相同照明效果下比传统光源节能80%以上。目前市售LED晶片材质基本以砷化镓、磷化铝镓钢(AlGaInP)、氮化铟镓( InGaN)为主,砷化镓的晶胞结构如图。回答下列问题:
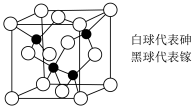
(1)砷的基态原子的电子排布式是___________ 。
(2)磷和砷是同一族的元素,第一电离能:磷___________ (填“>”“<”或“=”,下同)砷,它们形成的氢化物的沸点:PH3___________ AsH3,原因是______________________ 。
(3)AsH3是无色、稍有大蒜味的气体。AsH3中砷原子的杂化轨道方式为___________ ,AsH3的空间结构为___________ 。
(4)砷元素的常见化合价有+3和+5,它们对应的含氧酸有H3AsO3和H3AsO4两种,其中H3AsO4的酸性比H3AsO3的酸性强,从物质结构与性质的关系来看,H3AsO4的酸性比H3AsO3的酸性强的原因是_________________________________ 。
(5)此晶胞中所含的砷原子的个数为___________ ,砷化镓的化学式为___________ 。

(1)砷的基态原子的电子排布式是
(2)磷和砷是同一族的元素,第一电离能:磷
(3)AsH3是无色、稍有大蒜味的气体。AsH3中砷原子的杂化轨道方式为
(4)砷元素的常见化合价有+3和+5,它们对应的含氧酸有H3AsO3和H3AsO4两种,其中H3AsO4的酸性比H3AsO3的酸性强,从物质结构与性质的关系来看,H3AsO4的酸性比H3AsO3的酸性强的原因是
(5)此晶胞中所含的砷原子的个数为
您最近一年使用:0次
5 . 钾、氟及锌的相关化合物用途非常广泛。回答下列问题:
(1)基态锌原子的价电子排布式为___________ ;K、F、Zn的电负性从大到小的顺序为___________ 。
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是_______________ 。
(3)OF2分子的几何构型为___________ ,中心原子的杂化类型为___________ 。
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在___________ ;与O3-互为等电子体的分子为___________ (任 写一种 )。
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。
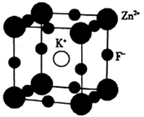
①晶胞中Zn2+的配位数为___________ 个。
②晶胞中紧邻的两个F-间的距离为_______________________ (列出算式即可)nm。
③该晶体的密度为___________ (列出算式即可,用NA表示阿伏伽德罗常数的数值)g·cm-3。
(1)基态锌原子的价电子排布式为
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是
(3)OF2分子的几何构型为
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。

①晶胞中Zn2+的配位数为
②晶胞中紧邻的两个F-间的距离为
③该晶体的密度为
您最近一年使用:0次
2018-01-07更新
|
409次组卷
|
6卷引用:陕西省榆林市2018届高三第二次模拟考试理综化学试题
2010·黑龙江哈尔滨·二模
解题方法
6 . 现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知BA5为离子化合物,写出其电子式______
(2)B基态原子中能量最高的电子,其电子云在空间有______ 个方向,原子轨道呈______ 形
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,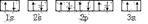
该同学所画的电子排布图违背了______
(4)G位于______ 族______ 区,价电子排布式为______
(5)DE3 中心原子的杂化方式为______ ,用价层电子对互斥理论推测其空间构型为______
(6)检验F元素的方法是______ ,请用原子结构的知识解释产生此现象的原因是______
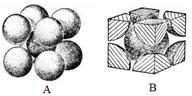
(7)F元素的晶胞如下图所示,若设该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,F原子的摩尔质量为M,则F原子的半径为______ cm
| A元素的核外电子数和电子层数相等,也是原子半径最小的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是:I1=738kJ/mol I2 = 1451 kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,
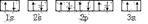
该同学所画的电子排布图违背了
(4)G位于
(5)DE3 中心原子的杂化方式为
(6)检验F元素的方法是
(7)F元素的晶胞如下图所示,若设该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,F原子的摩尔质量为M,则F原子的半径为

您最近一年使用:0次
2010·陕西西安·二模
解题方法
7 . 【化学—物质结构与性质】
下表中实线是元素周期表的部分边界,其中上边界并未用实线标出。
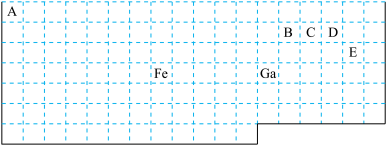
根据信息回答下列问题:
(1)周期表中比Ga质子数少2的基态原子价电子排布式为 。
(2)Fe元素位于周期表的 分区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为__________;已知:原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为 ____和 _____(填化学式),CO的结构式为 。
(3)在CH4、CO及CH3OH中,碳原子采取sp3杂化的分子为 。
(4)根据VSEPR理论预测ED4- 离子的空间构型为______________型。B、C、D及E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的电子式为:__________________________________(写2种) 。
(5)B与D形成的稳定化合物为___________分子(填“极性”“非极性”),其固态为 ________晶体。
下表中实线是元素周期表的部分边界,其中上边界并未用实线标出。

根据信息回答下列问题:
(1)周期表中比Ga质子数少2的基态原子价电子排布式为 。
(2)Fe元素位于周期表的 分区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为__________;已知:原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为 ____和 _____(填化学式),CO的结构式为 。
(3)在CH4、CO及CH3OH中,碳原子采取sp3杂化的分子为 。
(4)根据VSEPR理论预测ED4- 离子的空间构型为______________型。B、C、D及E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的电子式为:__________________________________(写2种) 。
(5)B与D形成的稳定化合物为___________分子(填“极性”“非极性”),其固态为 ________晶体。
您最近一年使用:0次



