名校
解题方法
1 . A、B、C、D为原子序数依次增大的四种元素,A2﹣和B+具有相同的电子构型:C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是___________ (填元素符号),其中C原子的核外电子排布式为 ___________ 。
(2)单质A有两种同素异形体,其中沸点高的是___________ (填分子式),原因是 ___________ ;B的氢化物的电子式为 ___________ 。
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为___________ ,中心原子的杂化轨道类型为 ___________ 。
(4)化合物D2A的立体构型为___________ ,中心原子的价层电子对数为 ___________ 。
(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为
(4)化合物D2A的立体构型为
您最近一年使用:0次
名校
2 . 部分含氯物质的分类与相应化合价的关系如图所示。下列推理错误的是
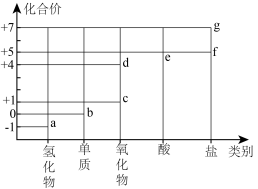

| A.a与e反应可生成b | B.d为酸性氧化物 |
| C.c溶于水可生成HClO | D.f、g中阴离子的VSEPR模型相同 |
您最近一年使用:0次
2023-12-16更新
|
184次组卷
|
4卷引用:吉林省通化市梅河口市第五中学2023-2024学年高三上学期12月月考化学试题
3 . 下列化学用语表述错误的是
A.HClO的电子式: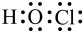 |
B.中子数为10的氧原子: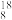 O O |
C.NH3分子的VSEPR模型: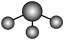 |
D.基态N原子的价层电子排布图: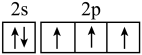 |
您最近一年使用:0次
2023-06-16更新
|
11389次组卷
|
33卷引用:吉林省长春市2024届高三上学期质量监测(一)化学试题
吉林省长春市2024届高三上学期质量监测(一)化学试题2023年高考湖南卷化学真题(已下线)专题02 化学用语(已下线)专题02 化学用语(已下线)专题02 化学用语(已下线)2023年湖南卷高考真题变式题(选择题1-5)(已下线)考点08 微粒间相互作用力(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第18讲原子结构和核外电子排布(已下线)专题02 化学用语的正误判断-2023年高考化学真题题源解密(全国通用)(已下线)专题02 化学用语及其应用-2023年高考化学真题题源解密(新高考专用)甘肃省武威市凉州区2024届高三上学期第一次诊断考试化学试题(已下线)考点17 原子结构和核外电子排布(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)重庆市第七中学校2023-2024学年高三上学期11月月考化学试卷广西玉林市博白县中学2023-2024学年高三上学期开学考试化学试题天津市第四中学2023-2024学年高三上学期第二次月考化学试卷宁夏回族自治区石嘴山市第三中学2023-2024学年高三上学期第四次月考理综试题辽宁省鞍山市普通高中2023-2024学年高三上学期期末联考化学试题黑龙江省肇东市第四中学2023-2024学年高三上学期期末考试化学试题(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)宁夏石嘴山市第三中学2023-2024学年高三上学期第四次月考理科综合试卷广东省深圳市盐田高级中学2023-2024学年高二上学期1月期末化学试题(已下线)选择题6-10(已下线)化学(九省联考考后提升卷,贵州卷)-2024年1月“九省联考”真题完全解读与考后提升湖南省邵东市第三中学2023-2024学年高二上学期1月期末考试化学试卷 (已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)2023-2024学年度第二学期高三化学零模试卷北京市师范大学附属实验中学2024届高三零模化学试题安徽省淮北市第一中学2023-2024学年高二下学期第一次月考化学试题山西省太原师范学院附属中学 师苑中学校2023-2024学年高二下学期准高三第二次月考化学试题北京市大兴区第一中学2023-2024学年高二下学期期中考试化学试题广东省肇庆市加美学校2023-2024学年高二下学期竞赛化学试题四川省达州外国语学校2023-2024学年高二下学期3月月考化学试题黑龙江省齐齐哈尔市第八中学校2023-2024学年高二下学期期中考试化学试卷
真题
名校
4 . 下列化学用语或表述正确的是
| A.BeCl2的空间结构:V形 | B.P4中的共价键类型:非极性键 |
| C.基态Ni原子价电子排布式:3d10 | D.顺—2—丁烯的结构简式: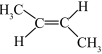 |
您最近一年使用:0次
2023-06-13更新
|
10849次组卷
|
13卷引用:吉林省吉林市第一中学2022-2023学年高一6月月考(线上)化学试题
吉林省吉林市第一中学2022-2023学年高一6月月考(线上)化学试题2023年高考辽宁卷化学真题(已下线)T2-化学用语(已下线)2023年高考化学真题完全解读(辽宁卷)(已下线)专题02 化学用语江西省乐安县第二中学2022-2023学年高二下学期6月期末考试化学试题(已下线)专题02 化学用语(已下线)专题02 化学用语(已下线)考点08 微粒间相互作用力(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题02 化学用语的正误判断-2023年高考化学真题题源解密(全国通用)(已下线)专题02 化学用语及其应用-2023年高考化学真题题源解密(新高考专用)(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)测试辽宁化学 请勿下载
名校
5 . CsCl是一种分析试剂,制备方法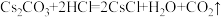 。下列说法正确的是
。下列说法正确的是
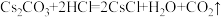 。下列说法正确的是
。下列说法正确的是A.CsCl的电子式: | B.基态 的核外电子排布式: 的核外电子排布式: |
C. 的空间构型:三角锥形 的空间构型:三角锥形 | D.中子数为18的Cl原子: |
您最近一年使用:0次
2023-05-27更新
|
522次组卷
|
4卷引用:吉林省长春市农安县2023-2024学年高三上学期零模调研化学试题
名校
解题方法
6 . 下列化学用语表达错误的是
A.中子数为20的氯原子: |
B. 的价层电子对互斥模型: 的价层电子对互斥模型: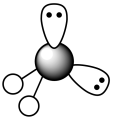 |
C.基态C原子的价层电子轨道表示式: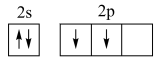 |
D.邻羟基苯甲醛分子内氢键示意图: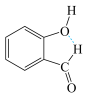 |
您最近一年使用:0次
2023-03-08更新
|
561次组卷
|
4卷引用:吉林省长春市第二实验中学2023-2024学年高三上学期9月月考化学试题
名校
解题方法
7 . 鲍林提出杂化轨道理论能解释分子的空间结构,下列关于粒子的描述正确的是
| 选项 | 粒子 | 空间结构 | 解释 |
| A | SO3 | 正三角形 | S原子采取sp3杂化 |
| B | BF3 | 正三角形 | B原子采取sp2杂化 |
| C | C2H4 | 平面三角形 | C原子采取sp2杂化 |
| D |  | 四面体形 | Cl原子采取sp3杂化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 氮元素及其化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)基态氮原子的核外共有_________ 种不同运动状态的电子,氮元素的第一电离能在同周期中从大到小排第_________ 位。
(2)已知NH3分子的键角约为107°,而PH3分子的键角约为94°,试用价层电子对互斥理论解释NH3的键角比PH3的键角大的原因:______________
(3)乙二胺(H2N—CH2—CH2—NH2)分子中氮原子轨道的杂化类型为_________ ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高很多,原因是___________ 。
(1)基态氮原子的核外共有
(2)已知NH3分子的键角约为107°,而PH3分子的键角约为94°,试用价层电子对互斥理论解释NH3的键角比PH3的键角大的原因:
(3)乙二胺(H2N—CH2—CH2—NH2)分子中氮原子轨道的杂化类型为
您最近一年使用:0次
名校
解题方法
9 . 下列说法不正确的是
A.键角: | B.沸点: |
C. 的空间结构为平面三角形 的空间结构为平面三角形 | D. 是极性分子 是极性分子 |
您最近一年使用:0次
2022-12-29更新
|
448次组卷
|
2卷引用:吉林省长春市第二实验中学2022-2023学年高二下学期4月月考化学试题
名校
10 . 主族元素X、Y、Z、Q、M的原子序数依次增大且均不大于20,元素Z和Q同族。元素M的化合物M+[Q-X≡Y]-为实验室中常用于检验Fe3+试剂,下列说法中错误的是
| A.Q与M的简单离子半径,前者大于后者 |
| B.YH3与XH4键角,前者小于后者 |
| C.1molFe(QXY)3中σ键为9mol |
| D.Y、Z两元素基态原子核外电子的空间运动状态不同 |
您最近一年使用:0次
2022-10-22更新
|
157次组卷
|
2卷引用:吉林省长春市第二实验中学2022-2023学年高二下学期4月月考化学试题



