名校
解题方法
1 . 已知HNO3、H2SO4的结构如图所示,下列说法不正确的是
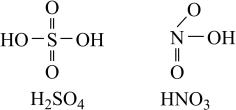
| A.HNO3、H2SO4分子中N、S的杂化轨道类型分别为sp2、sp3 |
B.NO 、SO 、SO 的空间结构分别为平面三角形、正四面体形 的空间结构分别为平面三角形、正四面体形 |
| C.HNO3、H2SO4都能与水分子形成分子间氢键 |
D.等物质的量的NO 、SO 、SO 中含σ键的个数之比为2∶3 中含σ键的个数之比为2∶3 |
您最近一年使用:0次
名校
2 . 2023年10月26日,神舟17号载人飞船成功发射,“人造太阳”、墨子“传信”、超算“发威”、中国空间站、C919投运,使中国“赶上世界”的强国梦实现了历史性跨越。下列叙述错误的是
| A.火箭用液氢为燃料生成水,水分子的空间结构为V形 |
| B.墨子“传信”和超算“天河一号”中使用的芯片的主要材料均为硅 |
| C.臭氧是替代氯气的净水剂,和氯气一样,为非极性分子 |
D.“人造太阳”核聚变反应堆的 中子数为2 中子数为2 |
您最近一年使用:0次
名校
3 . 下列有关二氧化碳的描述错误的是
| A.含有非极性键 | B.是直线形分子 |
| C.属于非极性分子 | D.结构式为 |
您最近一年使用:0次
名校
4 . 下列说法正确的是
A.HCl和 分子中均含有 分子中均含有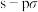 键 键 |
B. 和 和 的VSEPR模型和空间结构均一致 的VSEPR模型和空间结构均一致 |
C. 和 和 都是含有极性键的非极性分子 都是含有极性键的非极性分子 |
D.酸性: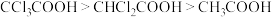 |
您最近一年使用:0次
名校
5 . 根据原子结构,分子结构与性质的相关知识,回答下列问题:
(1) 分子的VSEPR模型为
分子的VSEPR模型为___________ ; 分子的立体构型为
分子的立体构型为___________ 。
(2) 为
为___________ 杂化,与其互为等电子体的微粒有___________ (任写一种)。
(3)硫代硫酸盐可用作浸金试剂。硫代硫酸根( )可看作是
)可看作是 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。
①基态O原子的核外电子中,两种自旋状态的电子数之比为___________ 。 的空间结构是
的空间结构是___________ 。
②浸金时, 作为配体可提供孤电子对与
作为配体可提供孤电子对与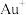 形成
形成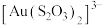 。分别判断
。分别判断 中的中心S原子和端基S原子能否做配位原子并说明理由:
中的中心S原子和端基S原子能否做配位原子并说明理由:___________ 。
(1)
 分子的VSEPR模型为
分子的VSEPR模型为 分子的立体构型为
分子的立体构型为(2)
 为
为(3)硫代硫酸盐可用作浸金试剂。硫代硫酸根(
 )可看作是
)可看作是 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。①基态O原子的核外电子中,两种自旋状态的电子数之比为
 的空间结构是
的空间结构是②浸金时,
 作为配体可提供孤电子对与
作为配体可提供孤电子对与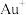 形成
形成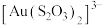 。分别判断
。分别判断 中的中心S原子和端基S原子能否做配位原子并说明理由:
中的中心S原子和端基S原子能否做配位原子并说明理由:
您最近一年使用:0次
名校
6 . X、Y、Z、M和Q五种主族元素,原子序数依次增大,X原子半径最小,短周期中M电负性最小,Z与Y、Q相邻,基态Z原子的s能级与p能级的电子数相等,下列说法不正确 的是
A.沸点: |
B.M与Z可形成化合物 、 、 |
C.化学键中离子键成分的百分数: |
D. 与 与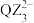 离子空间结构均为三角锥形 离子空间结构均为三角锥形 |
您最近一年使用:0次
名校
解题方法
7 . 下列表示不正确 的是
A.HCl的形成过程: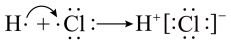 |
B. 的VSEPR模型: 的VSEPR模型: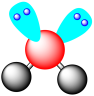 |
C. 的空间结构: 的空间结构: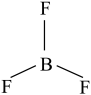 (平面三角形) (平面三角形) |
D.硅的基态原子轨道表示式: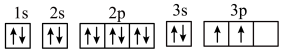 |
您最近一年使用:0次
名校
解题方法
8 . 下列化学用语表述错误的是
A.基态铬原子的简化电子排布式为 ,在元素周期表中位于 ,在元素周期表中位于 区 区 |
| B.基态氧原子的核外电子的运动状态有8种 |
C. 的VSEPR模型: 的VSEPR模型: |
D.用电子式表示 的形成过程: 的形成过程: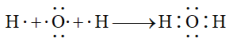 |
您最近一年使用:0次
名校
解题方法
9 . 关于① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,下列说法中正确的是
,下列说法中正确的是
 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,下列说法中正确的是
,下列说法中正确的是| A.④分子空间构型为三角锥形,该分子为极性分子 |
| B.②③⑤的VSEPR模型为平面三角形 |
| C.③与⑥中心原子杂化类型相同,两者都是极性分子 |
| D.①中所有原子都满足最外层8电子稳定结构 |
您最近一年使用:0次
名校
10 . 我国科学家成功合成世界上首个五氮阴离子盐: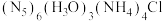 ,其部分结构如图(虚线代表氢键)。下列有关说法错误的是
,其部分结构如图(虚线代表氢键)。下列有关说法错误的是
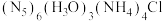 ,其部分结构如图(虚线代表氢键)。下列有关说法错误的是
,其部分结构如图(虚线代表氢键)。下列有关说法错误的是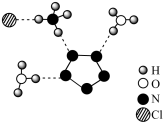
| A.该盐中存在的主要微粒间作用是:离子键、共价键、氢键 |
| B.结合该盐结构可知,氢键只有H…O、H…N、H…Cl三种存在形式 |
C.已知 具有类似苯环结构,则每个N杂化类型均为 具有类似苯环结构,则每个N杂化类型均为 ,离子内存在一个大 ,离子内存在一个大 键 键 |
| D.该盐中两种阳离子的中心原子轨道杂化类型相同,但空间结构不同 |
您最近一年使用:0次



