名校
1 . 苯、甲苯,乙苯、二甲苯等均是重要的芳香族化合物。回答下列问题:
(1)苯的实验式为___________ 。
(2)1mol苯与3molH2发生加成反应,碳的杂化类型由___________ ,转化为___________ 。
(3)甲苯的一氯代物有___________ 种,由甲苯制备2,4,6-三硝基甲苯(TNT)的化学方程式为___________ 。
(4)向对二甲苯中加入足量酸性高锰酸钾溶液,生成的有机物中的官能团名称___________ 。
(5)如图是某同学设计的制取少量溴苯(熔点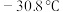 ,沸点
,沸点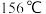 )的装置。实验时,打开K,向圆底烧瓶中滴加苯和溴的混合液,发现a中有微沸现象,b中的液体逐渐变为浅红色,c中有少量气泡产生,反应结束后,对a中的液体进行后续处理即可获得溴苯。
)的装置。实验时,打开K,向圆底烧瓶中滴加苯和溴的混合液,发现a中有微沸现象,b中的液体逐渐变为浅红色,c中有少量气泡产生,反应结束后,对a中的液体进行后续处理即可获得溴苯。___________ 。
②该实验___________ (填“放热”或“吸热”)。
③c中看到的现象证明___________ 。
④得到粗溴苯后,用如下操作进行精制:
①水洗 ②蒸馏 ③用干燥剂干燥 ④10%NaOH溶液洗
正确的操作顺序是___________ (填序号)。
A.①②③④② B.②④②③① C.④①③①② D.①④①③②
⑤进行蒸馏操作中,仪器选择及安装(夹持及加热装置已省略)均正确的是___________ (填字母)。
(1)苯的实验式为
(2)1mol苯与3molH2发生加成反应,碳的杂化类型由
(3)甲苯的一氯代物有
(4)向对二甲苯中加入足量酸性高锰酸钾溶液,生成的有机物中的官能团名称
(5)如图是某同学设计的制取少量溴苯(熔点
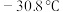 ,沸点
,沸点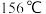 )的装置。实验时,打开K,向圆底烧瓶中滴加苯和溴的混合液,发现a中有微沸现象,b中的液体逐渐变为浅红色,c中有少量气泡产生,反应结束后,对a中的液体进行后续处理即可获得溴苯。
)的装置。实验时,打开K,向圆底烧瓶中滴加苯和溴的混合液,发现a中有微沸现象,b中的液体逐渐变为浅红色,c中有少量气泡产生,反应结束后,对a中的液体进行后续处理即可获得溴苯。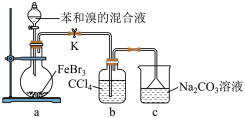
②该实验
③c中看到的现象证明
④得到粗溴苯后,用如下操作进行精制:
①水洗 ②蒸馏 ③用干燥剂干燥 ④10%NaOH溶液洗
正确的操作顺序是
A.①②③④② B.②④②③① C.④①③①② D.①④①③②
⑤进行蒸馏操作中,仪器选择及安装(夹持及加热装置已省略)均正确的是
您最近一年使用:0次
2024-05-21更新
|
207次组卷
|
2卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
2 . 金属锂有“白色石油”之称,是新时代重要的资源,“盐湖提锂”越来越受到重视。
(1) 与
与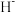 具有相同的电子构型,
具有相同的电子构型,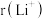 小于
小于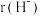 ,原因是
,原因是_______ 。 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 离子的空间结构是
离子的空间结构是_______ ,其中心原子的杂化轨道类型为_______ 。

(2) 晶胞如图所示,已知晶胞参数为
晶胞如图所示,已知晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为_______  (列出计算式)。
(列出计算式)。
(3)某兴趣小组取盐湖水进行浓缩和初步除杂后,得到浓缩卤水(含有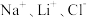 和少量
和少量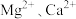 ),并设计了以下列过程通过制备碳酸锂来提取锂。
),并设计了以下列过程通过制备碳酸锂来提取锂。

 时相关物质的参数如下:①
时相关物质的参数如下:① 的溶解度:
的溶解度:
②:

回答下列问题:
①“沉淀1”为_______ 。
②向“滤液1”中加入适量固体 发生反应:
发生反应: 。通过计算解释
。通过计算解释 可用于转化的原因:
可用于转化的原因:_______ 。
③为提高 ,的析出量和纯度,“操作A”依次为
,的析出量和纯度,“操作A”依次为_______ 、_______ 、洗涤。
④有同学建议用“侯氏制碱法”的原理制备 。查阅资料后,发现文献对常温下的
。查阅资料后,发现文献对常温下的 有不同的描述:i.是白色固体:ii.尚未从溶液中分离出来。为探究
有不同的描述:i.是白色固体:ii.尚未从溶液中分离出来。为探究 的性质,将饱和
的性质,将饱和 溶液与饱和
溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
_______ (填“稳定”或“不稳定”),有关反应的离子方程式为_______ 。
(1)
 与
与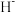 具有相同的电子构型,
具有相同的电子构型,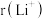 小于
小于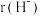 ,原因是
,原因是 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 离子的空间结构是
离子的空间结构是
(2)
 晶胞如图所示,已知晶胞参数为
晶胞如图所示,已知晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为 (列出计算式)。
(列出计算式)。(3)某兴趣小组取盐湖水进行浓缩和初步除杂后,得到浓缩卤水(含有
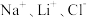 和少量
和少量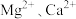 ),并设计了以下列过程通过制备碳酸锂来提取锂。
),并设计了以下列过程通过制备碳酸锂来提取锂。
 时相关物质的参数如下:①
时相关物质的参数如下:① 的溶解度:
的溶解度:
②:

| 化合物 |  |
 | 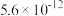 |
 |  |
 |  |
 |  |
①“沉淀1”为
②向“滤液1”中加入适量固体
 发生反应:
发生反应: 。通过计算解释
。通过计算解释 可用于转化的原因:
可用于转化的原因:③为提高
 ,的析出量和纯度,“操作A”依次为
,的析出量和纯度,“操作A”依次为④有同学建议用“侯氏制碱法”的原理制备
 。查阅资料后,发现文献对常温下的
。查阅资料后,发现文献对常温下的 有不同的描述:i.是白色固体:ii.尚未从溶液中分离出来。为探究
有不同的描述:i.是白色固体:ii.尚未从溶液中分离出来。为探究 的性质,将饱和
的性质,将饱和 溶液与饱和
溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
您最近一年使用:0次
名校
解题方法
3 . 工业上以锌矿(主要成分为 ,还含有
,还含有 、
、 、
、 、
、 、
、 等杂质)为主要原料制备皓矾
等杂质)为主要原料制备皓矾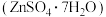 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题:

(1)“浸取”之前,需要对锌矿进行粉碎处理,其目的是___________________ 。
(2)“浸取”时,需要加入氧化剂 溶液,写出氯化铁溶液与硫化锌反应的离子方程式:
溶液,写出氯化铁溶液与硫化锌反应的离子方程式:_________ ,“浸取”时,溶液为酸性介质条件下,可能造成的影响是_____________ 。
(3) 中氧原子采取的杂化方式为
中氧原子采取的杂化方式为______________________ 。
(4)加入 反应完成后,加入硫酸钠溶液,可使溶液中的铁元素形成黄钠铁矾沉淀
反应完成后,加入硫酸钠溶液,可使溶液中的铁元素形成黄钠铁矾沉淀 ,写出生成黄钠铁矾的化学方程式:
,写出生成黄钠铁矾的化学方程式:________________________________ 。
(5)为了检验“滤液3”中铁元素是否除尽,可分别取滤液3于试管中,加入KSCN溶液和 溶液进行检验,若检验出有
溶液进行检验,若检验出有 ,则可观察到加入
,则可观察到加入 的试管中的现象为
的试管中的现象为_____________ ,解释产生此现象的原因:__________________________________________________ (用离子方程式表示)。
(6)“滤液4”经“一系列操作”可得产品皓矾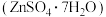 ,具体操作为
,具体操作为__________ 、___________ 、过滤、洗涤、干燥。
(7)工艺中产生的废液中含有 ,排放前需处理。向废液中加入由
,排放前需处理。向废液中加入由 和
和 组成的缓冲溶液调节
组成的缓冲溶液调节 ,通入
,通入 发生反应:
发生反应: .处理后的废液中部分微粒浓度如下:
.处理后的废液中部分微粒浓度如下:
则处理后的废液中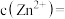
__________  。[已知:
。[已知: ,
, ,
, ,
, ]
]
 ,还含有
,还含有 、
、 、
、 、
、 、
、 等杂质)为主要原料制备皓矾
等杂质)为主要原料制备皓矾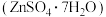 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题:
(1)“浸取”之前,需要对锌矿进行粉碎处理,其目的是
(2)“浸取”时,需要加入氧化剂
 溶液,写出氯化铁溶液与硫化锌反应的离子方程式:
溶液,写出氯化铁溶液与硫化锌反应的离子方程式:(3)
 中氧原子采取的杂化方式为
中氧原子采取的杂化方式为(4)加入
 反应完成后,加入硫酸钠溶液,可使溶液中的铁元素形成黄钠铁矾沉淀
反应完成后,加入硫酸钠溶液,可使溶液中的铁元素形成黄钠铁矾沉淀 ,写出生成黄钠铁矾的化学方程式:
,写出生成黄钠铁矾的化学方程式:(5)为了检验“滤液3”中铁元素是否除尽,可分别取滤液3于试管中,加入KSCN溶液和
 溶液进行检验,若检验出有
溶液进行检验,若检验出有 ,则可观察到加入
,则可观察到加入 的试管中的现象为
的试管中的现象为(6)“滤液4”经“一系列操作”可得产品皓矾
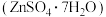 ,具体操作为
,具体操作为(7)工艺中产生的废液中含有
 ,排放前需处理。向废液中加入由
,排放前需处理。向废液中加入由 和
和 组成的缓冲溶液调节
组成的缓冲溶液调节 ,通入
,通入 发生反应:
发生反应: .处理后的废液中部分微粒浓度如下:
.处理后的废液中部分微粒浓度如下:微粒 |
|
|
|
浓度 |
|
|
|
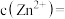
 。[已知:
。[已知: ,
, ,
, ,
, ]
]
您最近一年使用:0次
2022-11-25更新
|
239次组卷
|
4卷引用:山西省部分学校2022-2023学年高三上学期联考化学试题