名校
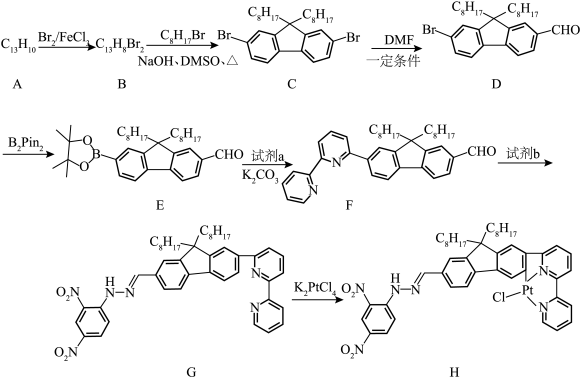
1 . 二联吡啶铂(Ⅱ)配合物(H)在传感器中有重要应用,一种合成路线如图。回答下列问题: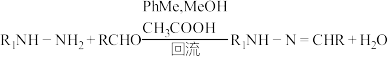
(1)有机物 的官能团的名称为
的官能团的名称为__________ 。
(2)写出 的反应方程式:
的反应方程式:______________ ,该反应的反应类型为__________ 。
(3)试剂 的结构简式为
的结构简式为__________ 。
(4)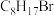 的同分异构体有多种,其中含有两个甲基的结构有
的同分异构体有多种,其中含有两个甲基的结构有__________ 种。
(5)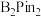 的结构为
的结构为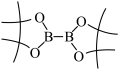 ,可由频哪醇(
,可由频哪醇(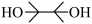 )和四(二甲氨基)二硼合成制得,频哪醇在浓硫酸作用下,加热,可制得分子式为
)和四(二甲氨基)二硼合成制得,频哪醇在浓硫酸作用下,加热,可制得分子式为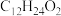 的物质,写出其结构:
的物质,写出其结构:__________ 。
(6)请从物质结构角度分析有机物 能与
能与 反应的原因:
反应的原因:______________ 。
(7)下列关于有机物 的说法错误的是__________(填标号)。
的说法错误的是__________(填标号)。
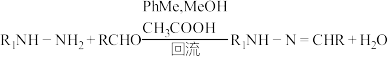
(1)有机物
 的官能团的名称为
的官能团的名称为(2)写出
 的反应方程式:
的反应方程式:(3)试剂
 的结构简式为
的结构简式为(4)
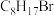 的同分异构体有多种,其中含有两个甲基的结构有
的同分异构体有多种,其中含有两个甲基的结构有(5)
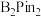 的结构为
的结构为 ,可由频哪醇(
,可由频哪醇( )和四(二甲氨基)二硼合成制得,频哪醇在浓硫酸作用下,加热,可制得分子式为
)和四(二甲氨基)二硼合成制得,频哪醇在浓硫酸作用下,加热,可制得分子式为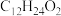 的物质,写出其结构:
的物质,写出其结构:(6)请从物质结构角度分析有机物
 能与
能与 反应的原因:
反应的原因:(7)下列关于有机物
 的说法错误的是__________(填标号)。
的说法错误的是__________(填标号)。A. 的配位数为4 的配位数为4 | B.含有手性碳原子 |
C. 原子的杂化方式为 原子的杂化方式为 | D.存在由 轨道“头碰头”形成的 轨道“头碰头”形成的 键 键 |
您最近一年使用:0次
2024-05-12更新
|
102次组卷
|
2卷引用:2024届山西省晋城市高三下学期第三次模拟考试理科综合试题-高中化学
2 . 丹皮酚(G)可用于缓解骨关节炎引起的疼痛,过敏性鼻炎以及感冒。一种合成丹皮酚及其衍生物H的合成路线如下:
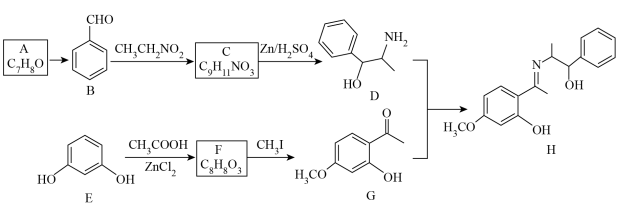
回答下列问题:
(1)E的化学名称为_______ 。
(2)A生成B的反应类型为_______ 。
(3)C的结构简式为_______ 。
(4)D中官能团的名称为_______ 。
(5)H中氮原子的杂化轨道类型为_______ ,手性碳个数为_______ 。
(6)E转变为F的化学方程式为_______ 。
(7)在G的同分异构体中,同时满足下列条件的共有_______ 种(不考虑立体异构);
①与 溶液反应放出
溶液反应放出 ;②与
;②与 溶液显色;③苯环上有两个取代基。其中核磁共振氢谱显示为6组峰,且峰面积比为
溶液显色;③苯环上有两个取代基。其中核磁共振氢谱显示为6组峰,且峰面积比为 的同分异构体的结构简式为
的同分异构体的结构简式为_______ 。

回答下列问题:
(1)E的化学名称为
(2)A生成B的反应类型为
(3)C的结构简式为
(4)D中官能团的名称为
(5)H中氮原子的杂化轨道类型为
(6)E转变为F的化学方程式为
(7)在G的同分异构体中,同时满足下列条件的共有
①与
 溶液反应放出
溶液反应放出 ;②与
;②与 溶液显色;③苯环上有两个取代基。其中核磁共振氢谱显示为6组峰,且峰面积比为
溶液显色;③苯环上有两个取代基。其中核磁共振氢谱显示为6组峰,且峰面积比为 的同分异构体的结构简式为
的同分异构体的结构简式为
您最近一年使用:0次
名校
3 . 化合物Q是一种药物的中间体,可利用如下合成路线制备化合物Q;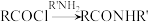
(1)有机物A的化学名称为__________ ;有机物C中官能团的名称为__________ 。
(2)反应①中加入 的作用是
的作用是____________________ ;合成路线中设计反应①和⑤目的是____________________ 。反应⑦的化学方程式为______________________________ 。下列关于反应③的说法,错误的是__________ (填标号)。
A.反应前后N原子的杂化方式未发生变化
B.反应类型为还原反应,当生成1molB时转移6mol电子
C.可以利用酸性 溶液鉴别物质A和B
溶液鉴别物质A和B
(3)有机物D的同分异构体中,同时含有苯环和硝基的共__________ 种(考虑立体异构);其中核磁共振氢谱显示含3组吸收峰,且吸收峰面积比为6:2:1的同分异构体的结构简式为__________ 。
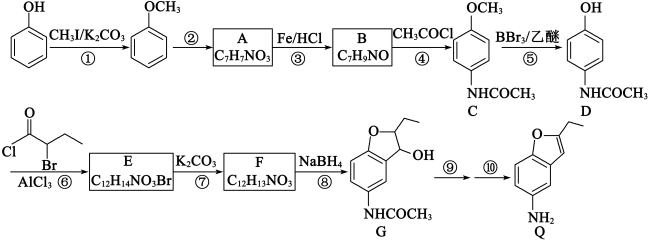
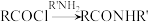
Ⅱ.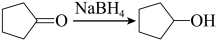
(1)有机物A的化学名称为
(2)反应①中加入
 的作用是
的作用是A.反应前后N原子的杂化方式未发生变化
B.反应类型为还原反应,当生成1molB时转移6mol电子
C.可以利用酸性
 溶液鉴别物质A和B
溶液鉴别物质A和B(3)有机物D的同分异构体中,同时含有苯环和硝基的共
您最近一年使用:0次
2024-03-29更新
|
487次组卷
|
3卷引用:2024届山西省朔州市怀仁市第一中学校高三下学期四模理科综合试题-高中化学
解题方法
4 . 新能源汽车在实现可持续发展的环境目标、减少空气的污染问题及应对气候的逐渐恶化中起到了至关重要的作用。锂离子电池使用寿命在5~8年,研究回收废旧正极材料中Li、Ni、Co、Mn等资源可以促进锂离子电池产业的良性发展。下图是一种三元锂电池正极材料的回收工艺。

回答下列问题:
(1)浸取时 中钴元素转化为
中钴元素转化为 ,有机酸用醋酸时反应的离子方程式为
,有机酸用醋酸时反应的离子方程式为___________ 。
(2)浸取时有机酸用苹果酸 比醋酸浸取效果好,苹果酸分子中C原子的杂化类型为
比醋酸浸取效果好,苹果酸分子中C原子的杂化类型为___________ 。
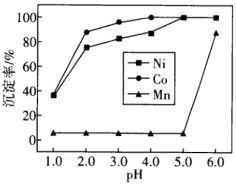
(3) 时溶液中
时溶液中
___________ ;随pH增大, 和
和 的沉淀率增大的原因为
的沉淀率增大的原因为___________ 。
(4)沉锂时生成 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(5)还可以通过电渗析法分离金属离子。硫酸、双氧水浸取后,分三次电渗析可分离成功。下图所示为第一次电渗析分离 的工艺,离子交换膜B为
的工艺,离子交换膜B为___________ (填“阴”或“阳”)离子交换膜。第二次用同样方法分离 ,第三次直接对剩余溶液电渗析分离,且需要将C改为一价阳离子交换膜。由上述分离过程可推测,
,第三次直接对剩余溶液电渗析分离,且需要将C改为一价阳离子交换膜。由上述分离过程可推测, 、
、 、
、 中与
中与 反应最难的为
反应最难的为___________ , 在
在___________ 膜(填“AB”、“BC”或“CD”)之间获得。


已知:①正极材料主要成分可以表示为 (M:Ni、Co、Mn)。
(M:Ni、Co、Mn)。
②浸取液中金属离子生成MS沉淀情况与pH的关系如下图。
③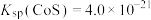 、
、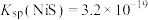 、
、 。
。
回答下列问题:
(1)浸取时
 中钴元素转化为
中钴元素转化为 ,有机酸用醋酸时反应的离子方程式为
,有机酸用醋酸时反应的离子方程式为(2)浸取时有机酸用苹果酸
 比醋酸浸取效果好,苹果酸分子中C原子的杂化类型为
比醋酸浸取效果好,苹果酸分子中C原子的杂化类型为(3)
 时溶液中
时溶液中
 和
和 的沉淀率增大的原因为
的沉淀率增大的原因为(4)沉锂时生成
 ,反应的离子方程式为
,反应的离子方程式为(5)还可以通过电渗析法分离金属离子。硫酸、双氧水浸取后,分三次电渗析可分离成功。下图所示为第一次电渗析分离
 的工艺,离子交换膜B为
的工艺,离子交换膜B为 ,第三次直接对剩余溶液电渗析分离,且需要将C改为一价阳离子交换膜。由上述分离过程可推测,
,第三次直接对剩余溶液电渗析分离,且需要将C改为一价阳离子交换膜。由上述分离过程可推测, 、
、 、
、 中与
中与 反应最难的为
反应最难的为 在
在
您最近一年使用:0次
解题方法
5 . 我国科学家研究发现,常温常压下,铁基离子液体 在工业尾气中
在工业尾气中 、
、 等的脱除方面具有良好的性能。
等的脱除方面具有良好的性能。 结构如图所示。
结构如图所示。

(1) 中C原子的杂化轨道类型有
中C原子的杂化轨道类型有___________ 。在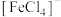 中,配体为
中,配体为___________ ,配位数为___________ 。
(2)在一定条件下 还可以转化为较稳定的
还可以转化为较稳定的
 中σ键与π键的个数比为
中σ键与π键的个数比为___________ , 的电子式为
的电子式为___________ 。
(3) 与
与 反应生成具有特征蓝色的物质X,这是实验室中检验
反应生成具有特征蓝色的物质X,这是实验室中检验 的常用方法。
的常用方法。
①科学家通过最常用的___________ 实验测定了物质X的晶体结构,其晶胞如图b所示(未表示 ),图a表示晶胞的
),图a表示晶胞的 结构(未表示K+)。
结构(未表示K+)。

②物质X的化学式为___________ 。
③若A处粒子的坐标参数为(0,0,0),B处粒子为(1,1,1),则C处粒子的坐标为___________ 。
④已知物质X的摩尔质量为 ,晶胞中
,晶胞中 与
与 的最小距离为dnm,阿伏加德罗常数为
的最小距离为dnm,阿伏加德罗常数为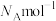 。则该晶胞中两个
。则该晶胞中两个 之间的最短距离为
之间的最短距离为___________ nm,晶体的密度为___________  。
。
 在工业尾气中
在工业尾气中 、
、 等的脱除方面具有良好的性能。
等的脱除方面具有良好的性能。 结构如图所示。
结构如图所示。
(1)
 中C原子的杂化轨道类型有
中C原子的杂化轨道类型有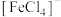 中,配体为
中,配体为(2)在一定条件下
 还可以转化为较稳定的
还可以转化为较稳定的
 中σ键与π键的个数比为
中σ键与π键的个数比为 的电子式为
的电子式为(3)
 与
与 反应生成具有特征蓝色的物质X,这是实验室中检验
反应生成具有特征蓝色的物质X,这是实验室中检验 的常用方法。
的常用方法。①科学家通过最常用的
 ),图a表示晶胞的
),图a表示晶胞的 结构(未表示K+)。
结构(未表示K+)。
②物质X的化学式为
③若A处粒子的坐标参数为(0,0,0),B处粒子为(1,1,1),则C处粒子的坐标为
④已知物质X的摩尔质量为
 ,晶胞中
,晶胞中 与
与 的最小距离为dnm,阿伏加德罗常数为
的最小距离为dnm,阿伏加德罗常数为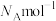 。则该晶胞中两个
。则该晶胞中两个 之间的最短距离为
之间的最短距离为 。
。
您最近一年使用:0次
名校
6 . 某芳香烃A是一种重要的有机化工原料。以它为初始原料经过如下转化可以合成扁桃酸、医药中间体G等多种物质。

已知:①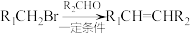
② 为间位定位基团
为间位定位基团
(1)扁桃酸分子中碳原子的杂化类型___________ 。
(2)C→D的化学方程式是___________ 。
(3) 的化学名称是
的化学名称是___________ 。
(4)写出由单体G通过加聚反应所得产物的结构简式___________ 。
(5)G有多种同分异构体,同时满足下列条件的同分异构体有___________ 种(不考虑立体异构)。
①属于芳香族化合物,且分子中含有的环只有苯环
②能发生银镜反应和水解反应
(6)已知 ,某兴趣小组用A为原料合成阿司匹林的前体水杨酸
,某兴趣小组用A为原料合成阿司匹林的前体水杨酸 ,请设计合成路线:
,请设计合成路线:___________ 。

已知:①
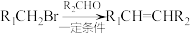
②
 为间位定位基团
为间位定位基团(1)扁桃酸分子中碳原子的杂化类型
(2)C→D的化学方程式是
(3)
 的化学名称是
的化学名称是(4)写出由单体G通过加聚反应所得产物的结构简式
(5)G有多种同分异构体,同时满足下列条件的同分异构体有
①属于芳香族化合物,且分子中含有的环只有苯环
②能发生银镜反应和水解反应
(6)已知
 ,某兴趣小组用A为原料合成阿司匹林的前体水杨酸
,某兴趣小组用A为原料合成阿司匹林的前体水杨酸 ,请设计合成路线:
,请设计合成路线:
您最近一年使用:0次
名校
解题方法
7 . 金属镍广泛应用于制造记忆合金、储氢合金以及用作加氢反应的催化剂,是重要的战略物资,但资源匮乏。从某废镍渣(含 、NiO、FeO、
、NiO、FeO、 )中回收金属镍并转化为
)中回收金属镍并转化为 的流程如图所示:
的流程如图所示:
(1)“滤液A”中主要溶质的化学式为________ 。
(2)“焙烧”后金属元素以硫酸盐的形式存在,写出NiO与 反应的化学方程式:
反应的化学方程式:_______ 。
(3)使用95℃热水“溶解”后过滤,所得“滤渣”的主要成分的化学式是______ 。
(4)①“萃取”时发生反应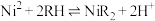 (RH为萃取剂),一定条件下,萃取平衡时,
(RH为萃取剂),一定条件下,萃取平衡时, ,则
,则 的苯取率为
的苯取率为_______ 。
②反萃取获得 ,溶液的实验操作是
,溶液的实验操作是______ 。
(5) 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料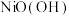 ,该反应的离子方程式为
,该反应的离子方程式为_________ 。
(6)镍能形成多种不同的化合物。图a是镍的一种配合物结构,图b是镍的一种氧化物的结构,下列说法不正确的是_________(填字母)。
 、NiO、FeO、
、NiO、FeO、 )中回收金属镍并转化为
)中回收金属镍并转化为 的流程如图所示:
的流程如图所示:
(1)“滤液A”中主要溶质的化学式为
(2)“焙烧”后金属元素以硫酸盐的形式存在,写出NiO与
 反应的化学方程式:
反应的化学方程式:(3)使用95℃热水“溶解”后过滤,所得“滤渣”的主要成分的化学式是
(4)①“萃取”时发生反应
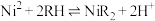 (RH为萃取剂),一定条件下,萃取平衡时,
(RH为萃取剂),一定条件下,萃取平衡时, ,则
,则 的苯取率为
的苯取率为②反萃取获得
 ,溶液的实验操作是
,溶液的实验操作是(5)
 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料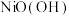 ,该反应的离子方程式为
,该反应的离子方程式为(6)镍能形成多种不同的化合物。图a是镍的一种配合物结构,图b是镍的一种氧化物的结构,下列说法不正确的是_________(填字母)。
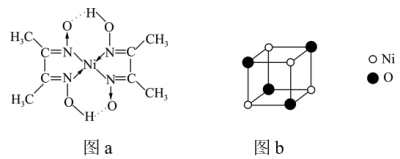
A.图a中,电负性 |
| B.图a分子中存在的化学键有共价键、配位键、氢键 |
| C.图b是氧化镍(NiO)的一个晶胞 |
D.氧化镍中 、 、 的配位数都是6 的配位数都是6 |
您最近一年使用:0次
2024-01-05更新
|
228次组卷
|
4卷引用:山西省运城市新绛县第二中学2023-2024学年高三上学期1月月考理综试题
名校
解题方法
8 . 完成下列问题。
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、 (PAN)等二次污染物。
(PAN)等二次污染物。
①PAN中除H外其余三种元素的第一电离能由大到小的顺序为___________ 。1molPAN中含有的σ键数目为___________ 。
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中中心离子的配位数为_________ ,中心离子的外围电子排布图___________ 。
③相同压强下,HCOOH的沸点比CH3OCH3___________ (填高或低),其原因是___________ 。
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
①(NH4)2SO4晶体中各种微粒间的作用力不涉及___________ (填序号)。
a.离子键 b.共价键 c.配位键 d.范德华力 e.氢键
②NH4NO3中阳离子的中心原子轨道采用___________ 杂化,阴离子的空间构型为___________ 。
(3)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则 =
=___________ (填数字)。已知:该晶胞边长为bpm,NA代表阿伏伽德罗常数,则该晶体的密度为___________ g/cm3(写出计算式即可)。

(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、
 (PAN)等二次污染物。
(PAN)等二次污染物。①PAN中除H外其余三种元素的第一电离能由大到小的顺序为
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中中心离子的配位数为
③相同压强下,HCOOH的沸点比CH3OCH3
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
①(NH4)2SO4晶体中各种微粒间的作用力不涉及
a.离子键 b.共价键 c.配位键 d.范德华力 e.氢键
②NH4NO3中阳离子的中心原子轨道采用
(3)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则
 =
=
您最近一年使用:0次
2023-11-21更新
|
123次组卷
|
2卷引用:山西运城新康国际中学2023-2024学年高三上学期一轮复习检测化学试卷
名校
解题方法
9 . 我国科学家发明了高选择性的二氧化碳加氢合成甲醇( )的催化剂,其组成为
)的催化剂,其组成为 固溶体。四方体
固溶体。四方体 晶胞如图所示,回答下列问题:
晶胞如图所示,回答下列问题:
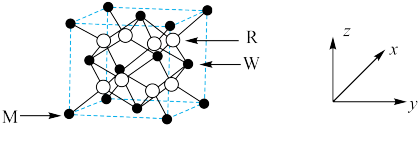
(1)图示晶胞中R代表___________ (填“O”或“ ”)原子,判断的理由为
”)原子,判断的理由为___________ 。
(2)关于 分子:
分子:
①该分子中氧原子采取的杂化类型为___________ 。
②该分子中的碳原子的价层电子对数为___________ 。
③有机物大多难溶于水,而甲醇可以与水互溶,其原因为___________ 。
(3)原子坐标参数表示晶胞内部各原子的相对位置,在如上图所示的晶胞中:
①若M原子的坐标参数为 ,W原子的坐标参数为
,W原子的坐标参数为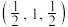 ,则R原子的坐标参数为
,则R原子的坐标参数为___________ 。
② 晶胞在z轴方向的投影图为
晶胞在z轴方向的投影图为___________ (填标号)。
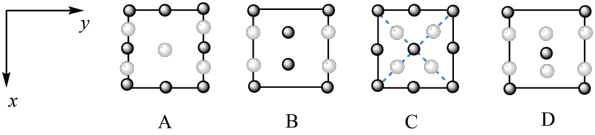
(4)查阅资料可知: 的熔点为2700℃,沸点为4300℃且熔融状态下可导电。
的熔点为2700℃,沸点为4300℃且熔融状态下可导电。
① 属于
属于___________ (填“分子”、“原子”或“离子”)晶体。
②假设 的密度为
的密度为
 ,摩尔质量为M
,摩尔质量为M ,
, 表示阿伏加德罗常数的值,则晶胞中
表示阿伏加德罗常数的值,则晶胞中 原子和O原子的最短距离为
原子和O原子的最短距离为___________  (列式表示即可)。
(列式表示即可)。
 )的催化剂,其组成为
)的催化剂,其组成为 固溶体。四方体
固溶体。四方体 晶胞如图所示,回答下列问题:
晶胞如图所示,回答下列问题:
(1)图示晶胞中R代表
 ”)原子,判断的理由为
”)原子,判断的理由为(2)关于
 分子:
分子:①该分子中氧原子采取的杂化类型为
②该分子中的碳原子的价层电子对数为
③有机物大多难溶于水,而甲醇可以与水互溶,其原因为
(3)原子坐标参数表示晶胞内部各原子的相对位置,在如上图所示的晶胞中:
①若M原子的坐标参数为
 ,W原子的坐标参数为
,W原子的坐标参数为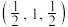 ,则R原子的坐标参数为
,则R原子的坐标参数为②
 晶胞在z轴方向的投影图为
晶胞在z轴方向的投影图为
(4)查阅资料可知:
 的熔点为2700℃,沸点为4300℃且熔融状态下可导电。
的熔点为2700℃,沸点为4300℃且熔融状态下可导电。①
 属于
属于②假设
 的密度为
的密度为
 ,摩尔质量为M
,摩尔质量为M ,
, 表示阿伏加德罗常数的值,则晶胞中
表示阿伏加德罗常数的值,则晶胞中 原子和O原子的最短距离为
原子和O原子的最短距离为 (列式表示即可)。
(列式表示即可)。
您最近一年使用:0次
名校
解题方法
10 . 碳是一种很常见的元素,它能形成多种物质。
(1)碳与铁可以形成合金。基态碳原子的价电子排布图为___________ ;基态铁原子核外共有___________ 种不同空间运动状态的电子。
(2)碳与其他元素一起能形成多种酸或酸根。
① 的空间结构是
的空间结构是___________ 。
②类卤素 分子中σ键与π键的数目比
分子中σ键与π键的数目比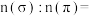
___________ , 对应的酸有两种,理论上硫氰酸(
对应的酸有两种,理论上硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸(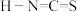 )的沸点,其原因是
)的沸点,其原因是___________ 。
(3)碳也可以形成多种有机化合物。吡咯( )结构中N原子的杂化轨道类型为
)结构中N原子的杂化轨道类型为___________ ;分子中的大π键可以用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则吡咯中的大π键应表示为
),则吡咯中的大π键应表示为___________ 。
(1)碳与铁可以形成合金。基态碳原子的价电子排布图为
(2)碳与其他元素一起能形成多种酸或酸根。
①
 的空间结构是
的空间结构是②类卤素
 分子中σ键与π键的数目比
分子中σ键与π键的数目比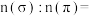
 对应的酸有两种,理论上硫氰酸(
对应的酸有两种,理论上硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸(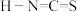 )的沸点,其原因是
)的沸点,其原因是(3)碳也可以形成多种有机化合物。吡咯(
 )结构中N原子的杂化轨道类型为
)结构中N原子的杂化轨道类型为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则吡咯中的大π键应表示为
),则吡咯中的大π键应表示为
您最近一年使用:0次
2023-09-03更新
|
189次组卷
|
2卷引用:山西省大同市第一中学校2023-2024学年高二下学期3月月考化学试题



