名校
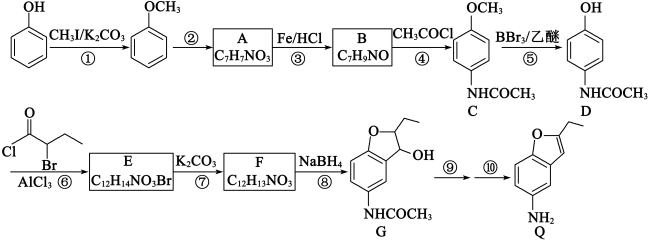
1 . 化合物Q是一种药物的中间体,可利用如下合成路线制备化合物Q;
(1)有机物A的化学名称为__________ ;有机物C中官能团的名称为__________ 。
(2)反应①中加入 的作用是
的作用是____________________ ;合成路线中设计反应①和⑤目的是____________________ 。反应⑦的化学方程式为______________________________ 。下列关于反应③的说法,错误的是__________ (填标号)。
A.反应前后N原子的杂化方式未发生变化
B.反应类型为还原反应,当生成1molB时转移6mol电子
C.可以利用酸性 溶液鉴别物质A和B
溶液鉴别物质A和B
(3)有机物D的同分异构体中,同时含有苯环和硝基的共__________ 种(考虑立体异构);其中核磁共振氢谱显示含3组吸收峰,且吸收峰面积比为6:2:1的同分异构体的结构简式为__________ 。
Ⅱ.
(1)有机物A的化学名称为
(2)反应①中加入
 的作用是
的作用是A.反应前后N原子的杂化方式未发生变化
B.反应类型为还原反应,当生成1molB时转移6mol电子
C.可以利用酸性
 溶液鉴别物质A和B
溶液鉴别物质A和B(3)有机物D的同分异构体中,同时含有苯环和硝基的共
您最近一年使用:0次
2024-03-29更新
|
550次组卷
|
3卷引用:2024届山西省朔州市怀仁市第一中学校高三下学期四模理科综合试题-高中化学
名校
解题方法
2 . 中科院大连化学物理研究所科学家用Ni-BaH3/Al2O3、Ni-LiH等作催化剂,实现了在常压、100~300℃的条件下合成氨,这一成果发表在《Nature Energy》杂志上。
(1)基态 的核外电子排布式为
的核外电子排布式为___________ ,若该离子核外电子空间运动状态有15种,则该离子处于___________ (填“基”或“激发”)态。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中 的空间构型为
的空间构型为___________ 。
②甘氨酸中C原子的杂化方式为___________ ,晶体类型是___________ ,其熔、沸点远高于相对分子质量几乎相等的丙酸(熔点为-21℃,沸点为141℃)的主要原因:一是甘氨酸能形成内盐;二是___________ 。
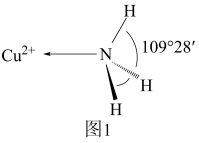
(3)NH3分子中的键角为107°,但在 中NH3分子的键角如图1所示,导致这种变化的原因是
中NH3分子的键角如图1所示,导致这种变化的原因是___________ 。
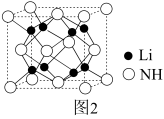
(4)亚氨基锂(Li2NH)是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图2所示,若晶胞参数为dpm,密度为ρg/cm3,则阿伏加德罗常数
___________  (列出表达式)。
(列出表达式)。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中
 的空间构型为
的空间构型为②甘氨酸中C原子的杂化方式为
(3)NH3分子中的键角为107°,但在
 中NH3分子的键角如图1所示,导致这种变化的原因是
中NH3分子的键角如图1所示,导致这种变化的原因是
(4)亚氨基锂(Li2NH)是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图2所示,若晶胞参数为dpm,密度为ρg/cm3,则阿伏加德罗常数

 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
2023-07-07更新
|
84次组卷
|
3卷引用:山西省怀仁市第一中学校2022-2023学年高二下学期期末考试理综化学试题
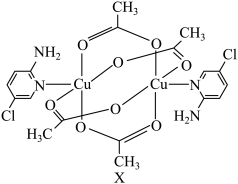
3 . 氨基吡啶与铜等金属离子所形成的配合物具备良好的磁学性质,某氨基吡啶衍生物铜配合物X的结构简式如图所示。
(1)基态氯原子的价层电子排布图为______ ;下列不同状态的氮原子中,能量最高的是______ (填字母)。
A. B.
B.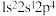 C.
C.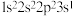 D.
D.
(2)C、N、O元素原子的电负性由大到小的顺序为______ 。
(3)X中 的配位数是
的配位数是______ ;铜元素有不同价态氧化物,高温下稳定性
______ CuO(填“大于”或“小于”),从离子的电子层结构角度分析,主要原因是______ 。
(4)X中N原子的杂化方式为______ 。
(5)下列关于X的说法中不正确的是______(填字母)。

(1)基态氯原子的价层电子排布图为
A.
 B.
B.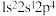 C.
C.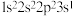 D.
D.
(2)C、N、O元素原子的电负性由大到小的顺序为
(3)X中
 的配位数是
的配位数是
(4)X中N原子的杂化方式为
(5)下列关于X的说法中不正确的是______(填字母)。
A.存在大π键 |
| B.存在氢键、配位键等化学键 |
| C.碳、氧原子间形成的σ键和π键个数比为2∶1 |
| D.铜属于d区元素 |
您最近一年使用:0次
2023-07-06更新
|
80次组卷
|
2卷引用:山西省怀仁市第十一中学校2022-2023学年高二下学期7月期末化学试题
名校
解题方法
4 . 半导体晶体是半导体工业的主要基础原料,第一代半导体代表材料是锗(Ge)单晶和硅单晶(Si),他们的出现实现了超大规模集成电路,第二代砷化镓(GaAs)等化合物半导体制成的激光器成为光通信系统中的关键器件,氮化硼(BN)、碳化硅(SiC)、金刚石等属于第三代半导体材料,又被称为高温半导体材料。
(1) 的价电子排布式为
的价电子排布式为___________ 。
(2)石墨型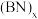 转变为金刚石型
转变为金刚石型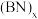 时,
时, 原子的杂化轨道类型由
原子的杂化轨道类型由___________ 变为___________ 。金刚石型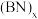 的硬度比金刚石大,推测其原因是
的硬度比金刚石大,推测其原因是___________ 。
(3)磷酸和亚磷酸 是磷元素的两种含氧酸。亚磷酸与
是磷元素的两种含氧酸。亚磷酸与 反应只生成
反应只生成 和
和 两种盐,则
两种盐,则 的结构式为
的结构式为___________ ,其为___________ 元酸
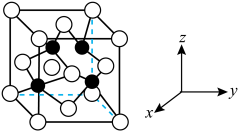
(4)下图为Ga和N形成的某种晶体的晶胞,该晶体也为高温半导体材料。其中黑色的球为Ga,白色球为N,该晶体的化学式为___________ 。若晶胞密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则两个最近的Ga之间的距离为
,则两个最近的Ga之间的距离为___________ 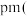 列出计算表达式
列出计算表达式 。
。
(1)
 的价电子排布式为
的价电子排布式为(2)石墨型
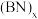 转变为金刚石型
转变为金刚石型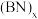 时,
时, 原子的杂化轨道类型由
原子的杂化轨道类型由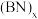 的硬度比金刚石大,推测其原因是
的硬度比金刚石大,推测其原因是(3)磷酸和亚磷酸
 是磷元素的两种含氧酸。亚磷酸与
是磷元素的两种含氧酸。亚磷酸与 反应只生成
反应只生成 和
和 两种盐,则
两种盐,则 的结构式为
的结构式为(4)下图为Ga和N形成的某种晶体的晶胞,该晶体也为高温半导体材料。其中黑色的球为Ga,白色球为N,该晶体的化学式为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则两个最近的Ga之间的距离为
,则两个最近的Ga之间的距离为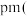 列出计算表达式
列出计算表达式 。
。
您最近一年使用:0次
2023-07-06更新
|
50次组卷
|
2卷引用:山西省应县第一中学校2022-2023学年高二下学期7月期末考试化学试题
名校
解题方法
5 . 过渡金属钛(Ti)性能优越,是继铁、铝之后应用广泛的“第三金属”,被誉为“未来钢铁”、“战略金属”。回答下列问题:
(1)下列Ti 原子电子排布式表示的状态中,电离最外层一个电子所需能量最大的是_______ (填标号)。
(2)TiCl4是氧化法制取钛的中间产物,TiCl4分子结构与TiCl4相同,二者常温下都是无色液体,则TiCl4分子的空间结构为_______ 。TiCl4的稳定性比CCl4差,极易水解,原因是_______ (从原子半径、键长和键能的角度分析)。
(3)六氟合钛酸钾(K2TiF6)可用作钛酸和金属钛的制造。六氟合钛酸钾中存在[TiF6]2-,该晶体中不存在的化学键是 _______ (填标号)。
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:

①有机物甲中标“*”的碳原子的杂化方式为_______ ,1mol甲分子中含有_______ mol σ键。
②有机物乙中,C、N、O三种元素的第一电离能由大到小的顺序是_______ 。
③有机物乙的沸点高于有机物甲,其主要原因是_______ 。
(5)嫦娥三号卫星上的PIC元件(热敏电阻)的主要成分——钡钛矿的晶胞结构如图所示。
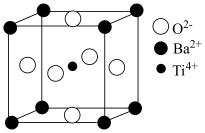
①晶体中一个Ba2+周围距离最近的O2-数目为_______ 。
②已知该晶体的密度为_______ ρg·cm-3,阿伏加德罗常数的值为NA,则该晶体中Ba2+与Ti4+之间的最短距离为 _______ pm (列出计算式)。
(1)下列Ti 原子电子排布式表示的状态中,电离最外层一个电子所需能量最大的是_______ (填标号)。
| A.[Ar]3d²4s¹4p¹ | B.[Ar]3d²4s² |
| C.[Ar]3d³4s²4p¹ | D.[Ar]3d¹4s¹4p² |
(2)TiCl4是氧化法制取钛的中间产物,TiCl4分子结构与TiCl4相同,二者常温下都是无色液体,则TiCl4分子的空间结构为
(3)六氟合钛酸钾(K2TiF6)可用作钛酸和金属钛的制造。六氟合钛酸钾中存在[TiF6]2-,该晶体中不存在的化学键是 _______ (填标号)。
| A.离子键 | B.极性键 | C.非极性键 | D.配位键 |
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:

①有机物甲中标“*”的碳原子的杂化方式为
②有机物乙中,C、N、O三种元素的第一电离能由大到小的顺序是
③有机物乙的沸点高于有机物甲,其主要原因是
(5)嫦娥三号卫星上的PIC元件(热敏电阻)的主要成分——钡钛矿的晶胞结构如图所示。

①晶体中一个Ba2+周围距离最近的O2-数目为
②已知该晶体的密度为
您最近一年使用:0次
2023-05-24更新
|
148次组卷
|
2卷引用:山西省怀仁市第一中学校2023-2024学年高三上学期第三次月考理综化学试题
名校
解题方法
6 .  可用于红外光谱分析以及显像管生产等。以某矿渣(主要成分为
可用于红外光谱分析以及显像管生产等。以某矿渣(主要成分为 ,含有少量CuO、
,含有少量CuO、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如下:
的工艺流程如下:

已知:①Sb属于第ⅤA元素,主要化合价为+3、+5价;
②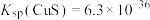 ,
, ;
;
③ 微溶于水,
微溶于水, 难溶于水,它们均为两性氧化物。SbOCl难溶于水;
难溶于水,它们均为两性氧化物。SbOCl难溶于水;
④次磷酸( )为一元中强酸,具有强还原性;
)为一元中强酸,具有强还原性;
⑤“电解”过程中(用惰性电极作电极),被氧化的Sb元素与被还原的Sb元素的质量之比为3∶2。
回答下列问题:
(1)基态As原子的核外电子排布式为___________ 。
(2)“滤渣I”的主要成分是SbOCl,为了提高锑的利用率,将滤渣I用氨水浸取使其转化为 ,转化过程中发生反应的化学方程式为
,转化过程中发生反应的化学方程式为___________ 。
(3)已知“沉淀”阶段溶液中, mol⋅L-1。若当“沉淀”后溶液中
mol⋅L-1。若当“沉淀”后溶液中 mol⋅L-1时,请通过计算说明该阶段是否有
mol⋅L-1时,请通过计算说明该阶段是否有 沉淀生成?
沉淀生成?___________ (简要写出计算过程,不考虑溶液体积的变化)。
(4)“除砷”时,已知 的氧化产物为
的氧化产物为 。
。
① 的化学名称为
的化学名称为___________ 。 的结构简式为
的结构简式为___________ 。
② 中磷原子的杂化轨道类型为
中磷原子的杂化轨道类型为___________ 。“除砷”过程中发生反应的离子方程式为___________ 。
(5)工业上向“电解后溶液”中加入单质Sb的目的是___________ 。
 可用于红外光谱分析以及显像管生产等。以某矿渣(主要成分为
可用于红外光谱分析以及显像管生产等。以某矿渣(主要成分为 ,含有少量CuO、
,含有少量CuO、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如下:
的工艺流程如下:
已知:①Sb属于第ⅤA元素,主要化合价为+3、+5价;
②
 ,
, ;
;③
 微溶于水,
微溶于水, 难溶于水,它们均为两性氧化物。SbOCl难溶于水;
难溶于水,它们均为两性氧化物。SbOCl难溶于水;④次磷酸(
 )为一元中强酸,具有强还原性;
)为一元中强酸,具有强还原性;⑤“电解”过程中(用惰性电极作电极),被氧化的Sb元素与被还原的Sb元素的质量之比为3∶2。
回答下列问题:
(1)基态As原子的核外电子排布式为
(2)“滤渣I”的主要成分是SbOCl,为了提高锑的利用率,将滤渣I用氨水浸取使其转化为
 ,转化过程中发生反应的化学方程式为
,转化过程中发生反应的化学方程式为(3)已知“沉淀”阶段溶液中,
 mol⋅L-1。若当“沉淀”后溶液中
mol⋅L-1。若当“沉淀”后溶液中 mol⋅L-1时,请通过计算说明该阶段是否有
mol⋅L-1时,请通过计算说明该阶段是否有 沉淀生成?
沉淀生成?(4)“除砷”时,已知
 的氧化产物为
的氧化产物为 。
。①
 的化学名称为
的化学名称为 的结构简式为
的结构简式为②
 中磷原子的杂化轨道类型为
中磷原子的杂化轨道类型为(5)工业上向“电解后溶液”中加入单质Sb的目的是
您最近一年使用:0次
2023-05-12更新
|
378次组卷
|
3卷引用:山西省怀仁市第一中学校2023-2024学年高三上学期开学摸底考试理综化学试题
山西省怀仁市第一中学校2023-2024学年高三上学期开学摸底考试理综化学试题辽宁省农村重点高中协作校2023届高三第三次模拟考试化学试题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)
解题方法
7 . 碳和硅是自然界中大量存在的元素,硅及其化合物是工业上最重要的材料。粗硅的制备有二种方法:
方法一:SiO2+2C Si+2CO↑ 方法二: SiO2+2Mg
Si+2CO↑ 方法二: SiO2+2Mg Si+2MgO (可能用到的相对原子质量: B-11 P-31)
Si+2MgO (可能用到的相对原子质量: B-11 P-31)
(1)基态硅原子中存在_______ 对自旋相反的电子,基态Mg 的最外层电子所占据的能级的电子云能廓图是_______ 。
(2)上述反应中所有元素第一电离能最小的元素是_______ (填元素符号)。
(3)试比较C (金刚石),晶体Si,CO 三种物质的熔沸点从高到低的顺序_______ ,试解释原因:_______ 。
(4)CO 在配合物中可作为配体,在Cr(CO)6配合物中配原子是_______ (填元素符号)1mol该配合物中含有π键的数目_______ 。
(5)SiO2晶胞(图2) 可理解成将金刚石晶胞(图1) 中的C原子置换成Si原子,然后在Si-Si之间插入O原子而形成。

①推测SiO2晶胞中Si采用_______ 杂化,O-Si-O的键角_______ 。
②SiO2晶跑中,含有Si原子_______ 个和O原子_______ 个。
方法一:SiO2+2C
 Si+2CO↑ 方法二: SiO2+2Mg
Si+2CO↑ 方法二: SiO2+2Mg Si+2MgO (可能用到的相对原子质量: B-11 P-31)
Si+2MgO (可能用到的相对原子质量: B-11 P-31)(1)基态硅原子中存在
(2)上述反应中所有元素第一电离能最小的元素是
(3)试比较C (金刚石),晶体Si,CO 三种物质的熔沸点从高到低的顺序
(4)CO 在配合物中可作为配体,在Cr(CO)6配合物中配原子是
(5)SiO2晶胞(图2) 可理解成将金刚石晶胞(图1) 中的C原子置换成Si原子,然后在Si-Si之间插入O原子而形成。

①推测SiO2晶胞中Si采用
②SiO2晶跑中,含有Si原子
您最近一年使用:0次
8 . 氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到 和BN,如图所示:
和BN,如图所示:
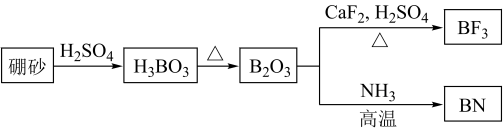
请回答下列问题:
(1) 的电子式为
的电子式为___________ 。
(2)由 制备
制备 的化学方程式是
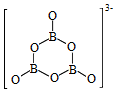
的化学方程式是___________ , 的结构式为
的结构式为___________ 。
(3)根据对角线规则,B的一些化学性质与元素___________ 的相似。 分子中,
分子中,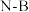 化学键称为
化学键称为___________ 键,其电子对由___________ 提供。氨硼烷在催化剂作用下水解释放氢气: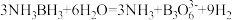 ,
, 的结构如图所示:在该反应中,B原子的杂化轨道类型由
的结构如图所示:在该反应中,B原子的杂化轨道类型由___________ 变为___________ 。与 互为等电子体的阳离子
互为等电子体的阳离子___________ (写一种即可)。
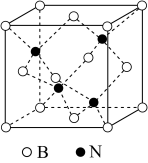
(4)氮化硼晶体有多种结构,如立方氮化硼和六方氮化硼等。立方氮化硼结构与金刚石相似(如图),晶胞边长为apm,立方氮化硼的密度是 。设阿伏加德罗常数值为
。设阿伏加德罗常数值为 。则a=
。则a=___________ (用 、
、 表示)。
表示)。
 和BN,如图所示:
和BN,如图所示:
请回答下列问题:
(1)
 的电子式为
的电子式为(2)由
 制备
制备 的化学方程式是
的化学方程式是 的结构式为
的结构式为(3)根据对角线规则,B的一些化学性质与元素
 分子中,
分子中, 化学键称为
化学键称为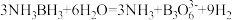 ,
, 的结构如图所示:在该反应中,B原子的杂化轨道类型由
的结构如图所示:在该反应中,B原子的杂化轨道类型由 互为等电子体的阳离子
互为等电子体的阳离子
(4)氮化硼晶体有多种结构,如立方氮化硼和六方氮化硼等。立方氮化硼结构与金刚石相似(如图),晶胞边长为apm,立方氮化硼的密度是
 。设阿伏加德罗常数值为
。设阿伏加德罗常数值为 。则a=
。则a= 、
、 表示)。
表示)。
您最近一年使用:0次
9 . ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含ⅤA族元素的化合物在医药生产中有许多重要用途。请回答下列问题:
(1)基态氮原子的价电子排布图是___ ;基态砷原子的电子排布式为___ 。
(2)砷与同周期第ⅦA族的溴的第一电离能相比,较大的是___ 。
(3)AsH3是无色稍有大蒜味的气体。AsH3的沸点高于PH3,其主要原因是___ 。
(4)Na3AsO4可作杀虫剂。AsO 的立体构型为
的立体构型为___ ,与其互为等电子体的一种分子为___ 。
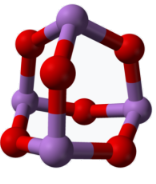
(5)某砷的氧化物俗称“砒霜”,其分子结构如图所示。该化合物的分子式为___ ,砷原子采取___ 杂化。
(6)GaAs是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与___ 个Ga相连。
(1)基态氮原子的价电子排布图是
(2)砷与同周期第ⅦA族的溴的第一电离能相比,较大的是
(3)AsH3是无色稍有大蒜味的气体。AsH3的沸点高于PH3,其主要原因是
(4)Na3AsO4可作杀虫剂。AsO
 的立体构型为
的立体构型为(5)某砷的氧化物俗称“砒霜”,其分子结构如图所示。该化合物的分子式为

(6)GaAs是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与
您最近一年使用:0次
解题方法
10 . 氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯商品名称为“特氟龙”,可做不粘锅涂层。它是一种准晶体,该晶体是一种无平移周期序、但有严格准周期位置序的独特晶体。可通过____________ 方法区分晶体、准晶体和非晶体。
(2)锑(Sb)与砷处于同一主族且相邻,基态锑原子价电子排布式为____________ 。[H2F]+[SbF6]-(氟酸锑)是一种超强酸,存在[H2F]+,写出一种与[H2F]+互为等电子体的阴离子是____________ 。
(3)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序____________ (填元素符号)。
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为____________ 。
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在____________ (填序号):
A.离子键 B. σ键 C.π键D.范德华力 E.配位键
(4)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃。
①CuF比CuCl熔点高的原因是____________ ;
②CuF的晶胞结构如图。F-填充在Cu+围成的____________ 空隙中,空隙填充率为____________ %。

(1)聚四氟乙烯商品名称为“特氟龙”,可做不粘锅涂层。它是一种准晶体,该晶体是一种无平移周期序、但有严格准周期位置序的独特晶体。可通过
(2)锑(Sb)与砷处于同一主族且相邻,基态锑原子价电子排布式为
(3)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在
A.离子键 B. σ键 C.π键D.范德华力 E.配位键
(4)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃。
①CuF比CuCl熔点高的原因是
②CuF的晶胞结构如图。F-填充在Cu+围成的

您最近一年使用:0次



