解题方法
1 . 我国科学家研究发现,常温常压下,铁基离子液体 在工业尾气中
在工业尾气中 、
、 等的脱除方面具有良好的性能。
等的脱除方面具有良好的性能。 结构如图所示。
结构如图所示。 中C原子的杂化轨道类型有
中C原子的杂化轨道类型有___________ 。在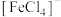 中,配体为
中,配体为___________ ,配位数为___________ 。
(2)在一定条件下 还可以转化为较稳定的
还可以转化为较稳定的
 中σ键与π键的个数比为
中σ键与π键的个数比为___________ , 的电子式为
的电子式为___________ 。
(3) 与
与 反应生成具有特征蓝色的物质X,这是实验室中检验
反应生成具有特征蓝色的物质X,这是实验室中检验 的常用方法。
的常用方法。
①科学家通过最常用的___________ 实验测定了物质X的晶体结构,其晶胞如图b所示(未表示 ),图a表示晶胞的
),图a表示晶胞的 结构(未表示K+)。
结构(未表示K+)。___________ 。
③若A处粒子的坐标参数为(0,0,0),B处粒子为(1,1,1),则C处粒子的坐标为___________ 。
④已知物质X的摩尔质量为 ,晶胞中
,晶胞中 与
与 的最小距离为dnm,阿伏加德罗常数为
的最小距离为dnm,阿伏加德罗常数为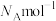 。则该晶胞中两个
。则该晶胞中两个 之间的最短距离为
之间的最短距离为___________ nm,晶体的密度为___________  。
。
 在工业尾气中
在工业尾气中 、
、 等的脱除方面具有良好的性能。
等的脱除方面具有良好的性能。 结构如图所示。
结构如图所示。
 中C原子的杂化轨道类型有
中C原子的杂化轨道类型有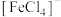 中,配体为
中,配体为(2)在一定条件下
 还可以转化为较稳定的
还可以转化为较稳定的
 中σ键与π键的个数比为
中σ键与π键的个数比为 的电子式为
的电子式为(3)
 与
与 反应生成具有特征蓝色的物质X,这是实验室中检验
反应生成具有特征蓝色的物质X,这是实验室中检验 的常用方法。
的常用方法。①科学家通过最常用的
 ),图a表示晶胞的
),图a表示晶胞的 结构(未表示K+)。
结构(未表示K+)。
③若A处粒子的坐标参数为(0,0,0),B处粒子为(1,1,1),则C处粒子的坐标为
④已知物质X的摩尔质量为
 ,晶胞中
,晶胞中 与
与 的最小距离为dnm,阿伏加德罗常数为
的最小距离为dnm,阿伏加德罗常数为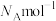 。则该晶胞中两个
。则该晶胞中两个 之间的最短距离为
之间的最短距离为 。
。
您最近一年使用:0次
名校
解题方法
2 . 碳是一种很常见的元素,它能形成多种物质。
(1)碳与铁可以形成合金。基态碳原子的价电子排布图为___________ ;基态铁原子核外共有___________ 种不同空间运动状态的电子。
(2)碳与其他元素一起能形成多种酸或酸根。
① 的空间结构是
的空间结构是___________ 。
②类卤素 分子中σ键与π键的数目比
分子中σ键与π键的数目比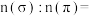
___________ , 对应的酸有两种,理论上硫氰酸(
对应的酸有两种,理论上硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸(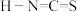 )的沸点,其原因是
)的沸点,其原因是___________ 。
(3)碳也可以形成多种有机化合物。吡咯( )结构中N原子的杂化轨道类型为
)结构中N原子的杂化轨道类型为___________ ;分子中的大π键可以用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则吡咯中的大π键应表示为
),则吡咯中的大π键应表示为___________ 。
(1)碳与铁可以形成合金。基态碳原子的价电子排布图为
(2)碳与其他元素一起能形成多种酸或酸根。
①
 的空间结构是
的空间结构是②类卤素
 分子中σ键与π键的数目比
分子中σ键与π键的数目比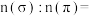
 对应的酸有两种,理论上硫氰酸(
对应的酸有两种,理论上硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸(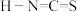 )的沸点,其原因是
)的沸点,其原因是(3)碳也可以形成多种有机化合物。吡咯(
 )结构中N原子的杂化轨道类型为
)结构中N原子的杂化轨道类型为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则吡咯中的大π键应表示为
),则吡咯中的大π键应表示为
您最近一年使用:0次
2023-09-03更新
|
194次组卷
|
2卷引用:山西省大同市第一中学校2023-2024学年高二下学期3月月考化学试题
名校
解题方法
3 . Fe、Cu为过渡金属元素,它们在工业生产中都有重要的应用。回答下列问题:
(1)将乙醇蒸气通过赤热的氧化铜粉末,会发生反应: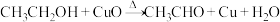
①有同学书写基态碳原子的核外电子排布图为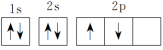 ,这样的书写不正确,违背了
,这样的书写不正确,违背了___________ 。
②乙醛和乙醇的相对分子质量相差2,但是,乙醇的沸点高于乙醛,其主要原因是___________ 。
(2)Fe、 都能被硝酸氧化。
都能被硝酸氧化。 中氮原子轨道的杂化类型为
中氮原子轨道的杂化类型为___________ 。
(3)研究发现,阳离子的颜色与未成对电子数有关。例如: 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是___________ 。
(1)将乙醇蒸气通过赤热的氧化铜粉末,会发生反应:
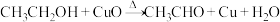
①有同学书写基态碳原子的核外电子排布图为
 ,这样的书写不正确,违背了
,这样的书写不正确,违背了②乙醛和乙醇的相对分子质量相差2,但是,乙醇的沸点高于乙醛,其主要原因是
(2)Fe、
 都能被硝酸氧化。
都能被硝酸氧化。 中氮原子轨道的杂化类型为
中氮原子轨道的杂化类型为(3)研究发现,阳离子的颜色与未成对电子数有关。例如:
 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是
您最近一年使用:0次
解题方法
4 . 汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。很多含巯基(-SH)的有机化合物是重金属元素求的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物II。

(1)汞的原子序数为80,与Zn属于同族元素,Hg价电子排布式为_______ ,位于元素周期表_______ 区。
(2)C、O、S分别形成的简单氢化物的沸点由高到低顺序为_______ ,理由_______ 。
(3)预测化合物I溶解性为_______ (填“难溶于水”或“易溶于水”);1mol化合物I中采取sp3杂化的原子数目是_______ 。
(4)理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分锗原子被Hg和Sb取代后形成。

①图b为Ce晶胞中部分锗原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是_______ 。
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为_______ ;X晶体的化学式为:_______ ;设X的相对分子质量为 ,则X晶体的密度为
,则X晶体的密度为_______ g·cm-3(列出计算式)。

(1)汞的原子序数为80,与Zn属于同族元素,Hg价电子排布式为
(2)C、O、S分别形成的简单氢化物的沸点由高到低顺序为
(3)预测化合物I溶解性为
(4)理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分锗原子被Hg和Sb取代后形成。

①图b为Ce晶胞中部分锗原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为
 ,则X晶体的密度为
,则X晶体的密度为
您最近一年使用:0次
名校
5 . 太阳能的开发利用在新能源研究中占据重要地位。单晶硅太阳能电池片在加工时,一般掺杂微量的铜、硼、镓、硒、钛等。请回答下列问题:
(1)镓与硒相比,电负性更大的是___________ (写元素符号)。
(2)基态 的核外电子排布式为
的核外电子排布式为___________ ;已知高温下 比CuO更稳定,试从铜原子核外电子结构角度解释其原因:
比CuO更稳定,试从铜原子核外电子结构角度解释其原因:___________ 。
(3)与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的有___________ (填元素符号)。
(4)在第二周期元素中,第一电离能介于B和N两元素之间的有___________ (写元素符号)。
(5)纳米 是一种应用广泛的催化剂,纳米
是一种应用广泛的催化剂,纳米 催化的一个实例如图所示。甲中所含的化学键种类有
催化的一个实例如图所示。甲中所含的化学键种类有___________ (填字母)。
a.氢键 b.离子键 c.极性键 d.非极性键

(1)镓与硒相比,电负性更大的是
(2)基态
 的核外电子排布式为
的核外电子排布式为 比CuO更稳定,试从铜原子核外电子结构角度解释其原因:
比CuO更稳定,试从铜原子核外电子结构角度解释其原因:(3)与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的有
(4)在第二周期元素中,第一电离能介于B和N两元素之间的有
(5)纳米
 是一种应用广泛的催化剂,纳米
是一种应用广泛的催化剂,纳米 催化的一个实例如图所示。甲中所含的化学键种类有
催化的一个实例如图所示。甲中所含的化学键种类有a.氢键 b.离子键 c.极性键 d.非极性键

您最近一年使用:0次
名校
解题方法
6 . 一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图。 的价电子排布式为
的价电子排布式为_______ ;一水合甘氨酸锌中所涉及的非金属元素电负性由大到小的顺序是_______ 。
(2)甘氨酸(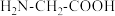 )中N的杂化轨道类型为
)中N的杂化轨道类型为_______ ;甘氨酸易溶于水,试从结构角度解释_______ 。
(3)一水合甘氨酸锌中 的配位数为
的配位数为_______ 。 填入
填入 组成
组成_______ 空隙中;
②由①能否判断出 、
、 相切?
相切?_______ (填“能”或“否”);
③已知晶体密度为 ,
, 半径为a pm,若要使
半径为a pm,若要使 、
、 相切,则
相切,则 半径为
半径为_______ pm(写计算表达式)。
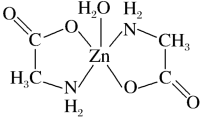
 的价电子排布式为
的价电子排布式为(2)甘氨酸(
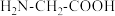 )中N的杂化轨道类型为
)中N的杂化轨道类型为(3)一水合甘氨酸锌中
 的配位数为
的配位数为(4) 是
是 的另一种配合物,IMI的结构为
的另一种配合物,IMI的结构为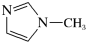 ,常温下IMI的某种衍生物与甘氨酸形成的离子化合物
,常温下IMI的某种衍生物与甘氨酸形成的离子化合物 为液态而非固态。原因是
为液态而非固态。原因是
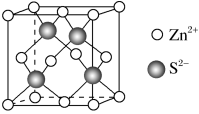
 填入
填入 组成
组成②由①能否判断出
 、
、 相切?
相切?③已知晶体密度为
 ,
, 半径为a pm,若要使
半径为a pm,若要使 、
、 相切,则
相切,则 半径为
半径为
您最近一年使用:0次
2021-01-03更新
|
379次组卷
|
6卷引用:山西省大同市第一中学2020届高三3月月考理综化学试题
名校
解题方法
7 . GaN是制造5G芯片的材料,氮化镓铝和氮化铝LED可发出紫外光。回答下列问题:
(1)基态As原子核外电子排布式为[Ar]________ ,下列状态的铝中,电离最外层的一个电子所需能量最小的是_____________ (填标号)。
A. B.
B. 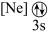 C.[Ne] D.
C.[Ne] D. 
(2)8—羟基喹啉铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与 (8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为
(8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为_______ ; 所含元素中电负性最大的是
所含元素中电负性最大的是___ (填元素符号),C、N、O的杂化方式依次为 _____ 、_________ 和____________ 。
(3)已知下列化合物的熔点:
①表中卤化物的熔点产生差异的原因是____________ 。
②熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6,二聚体Al2Cl6的结构式为_______ ;其中Al的配位数为_________ 。
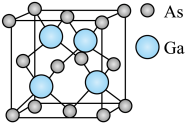
(4)GaAs的晶胞结构如图所示,紧邻的As原子之间的距离为x,紧邻的As、Ga原子之间的距离为y,则 =
=________ 。
(1)基态As原子核外电子排布式为[Ar]
A.
 B.
B. 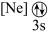 C.[Ne] D.
C.[Ne] D. 
(2)8—羟基喹啉铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与
 (8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为
(8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为 所含元素中电负性最大的是
所含元素中电负性最大的是(3)已知下列化合物的熔点:
| 化合物 | AlF3 | GaF3 | AlCl3 |
| 熔点/℃ | 1040 | 1000 | 194 |
①表中卤化物的熔点产生差异的原因是
②熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6,二聚体Al2Cl6的结构式为
(4)GaAs的晶胞结构如图所示,紧邻的As原子之间的距离为x,紧邻的As、Ga原子之间的距离为y,则
 =
=
您最近一年使用:0次
2020-02-22更新
|
130次组卷
|
3卷引用:山西省同煤一中联盟校2020届高三2月网上联考理综化学试题
山西省同煤一中联盟校2020届高三2月网上联考理综化学试题广东省湛江一中等五校2020届高三10月联考理综化学试题(已下线)考点14 物质结构与性质(选考)-2020年高考化学命题预测与模拟试题分类精编
名校
解题方法
8 . A、B、C、D、E是原子序数依次增大的五种常见元素,其中A是原子半径最小的元素,B元素的一种核素可用于考古断代,D元素的s轨道和p轨道上的电子数相等且有2个未成对电子;E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满。请用元素符号或化学式回答下列问题:
(1)A、B、C、D四种元素中,电负性最大的是___ ,第一电离能最大的是___ 。
(2)化合物CA3的沸点比化合物BA4的高,其主要原因是____ 。
(3)A、B形成的化合物M与氢氰酸(HCN)反应可得丙烯腈(H2C=CH—C≡N),则M的结构式为___ ,丙烯腈分子中碳原子轨道杂化类型是____ 。
(4)由C元素形成的一种离子与BD2互为等电子体,该离子的结构式为____ 。
(5)基态E原子的核外电子排布式为____ ,如图是D、E形成的某种化合物的晶胞结构示意图,该晶体的化学式为____ 。

(6)向E的硫酸盐溶液中通入过量的CA3,可生成[E(CA3)4]2+,1mol[E(CA3)4]2+中含有σ键的数目约为___ 。
(1)A、B、C、D四种元素中,电负性最大的是
(2)化合物CA3的沸点比化合物BA4的高,其主要原因是
(3)A、B形成的化合物M与氢氰酸(HCN)反应可得丙烯腈(H2C=CH—C≡N),则M的结构式为
(4)由C元素形成的一种离子与BD2互为等电子体,该离子的结构式为
(5)基态E原子的核外电子排布式为

(6)向E的硫酸盐溶液中通入过量的CA3,可生成[E(CA3)4]2+,1mol[E(CA3)4]2+中含有σ键的数目约为
您最近一年使用:0次
名校
解题方法
9 . 现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期。B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子,E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子。请回答下列问题:
(1)请写出D基态的价层电子排布图:_____ 。
(2)下列说法正确的是_____ 。
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点SiO2>CO2
B.电负性顺序:C<N<O<F
C.N2与CO为等电子体,结构相似,化学性质相似
D.稳定性:H2O>H2S,原因是水分子间存在氢键
(3)某化合物与F(Ⅰ)(Ⅰ表示化合价为+1)结合形成如图所示的离子,该离子中碳原子的杂化方式是______ 。

(4)已知(BC)2是直线性分子,并有对称性,且分子中每个原子最外层都达到8电子稳定结构,则(BC)2中σ键和π键的个数比为______ 。
(5)C元素最高价含氧酸与硫酸酸性强度相近,原因是______ 。
(6)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的O2-围成的正四面体空隙和3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,正四面体空隙数与O2-数之比为_____ ,有_____ %的正八面体空隙没有填充阳离子。Fe3O4晶胞中有8个图示结构单元,晶体密度为5.18g/cm3,则该晶胞参数a=______ pm。(写出计算表达式)

(1)请写出D基态的价层电子排布图:
(2)下列说法正确的是
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点SiO2>CO2
B.电负性顺序:C<N<O<F
C.N2与CO为等电子体,结构相似,化学性质相似
D.稳定性:H2O>H2S,原因是水分子间存在氢键
(3)某化合物与F(Ⅰ)(Ⅰ表示化合价为+1)结合形成如图所示的离子,该离子中碳原子的杂化方式是

(4)已知(BC)2是直线性分子,并有对称性,且分子中每个原子最外层都达到8电子稳定结构,则(BC)2中σ键和π键的个数比为
(5)C元素最高价含氧酸与硫酸酸性强度相近,原因是
(6)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的O2-围成的正四面体空隙和3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,正四面体空隙数与O2-数之比为

您最近一年使用:0次
2020-02-09更新
|
319次组卷
|
3卷引用:山西省大同市2020届高三第一次联合考试(市直)化学试题
山西省大同市2020届高三第一次联合考试(市直)化学试题【全国百强校】安徽省六安市第一中学2020届高三下学期自测卷(三)线下考试化学试题(已下线)考点14 物质结构与性质(选考)-2020年高考化学命题预测与模拟试题分类精编
10 . [化学——选修3:物质结构与性质]铬元素在地壳中含量占第21位,是一种重要的金属。回答下列问题:
(1)基态铬原子的价电子排布式为_________________ ,根据价层电子判断铬元素中最高价态为___________ 价。铬元素的第二电离能________ 锰元素的第二电离能(填“>”“<”填“=”)。
(2)无水氯化亚铬(CrCl2)的制备方法为在500℃时用含HCl的H2气流还原CrCl3,该过程涉及到的反应原理为____________________________________________ (用化学方程式表示)。
已知:氯化亚铬的熔点为820~824℃,则其晶体类型为___________ 晶体。二价铬还能与乙酸根形成配合物,在乙酸根中碳原子的杂化形式为___________
(3)已知CrO5中铬元素为最高价态,画出其结构式:______________________
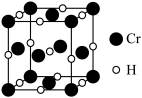
(4)Cr元素与H元素形成化合物的晶胞结构如图所示,则该化合物的化学式为___________ 。已知:该晶胞的边长为437.6 pm,NA表示阿伏加 德罗常数的值,则晶体的密度为____ g/cm3(列出计算式即可)。
(1)基态铬原子的价电子排布式为
(2)无水氯化亚铬(CrCl2)的制备方法为在500℃时用含HCl的H2气流还原CrCl3,该过程涉及到的反应原理为
已知:氯化亚铬的熔点为820~824℃,则其晶体类型为
(3)已知CrO5中铬元素为最高价态,画出其结构式:

(4)Cr元素与H元素形成化合物的晶胞结构如图所示,则该化合物的化学式为
您最近一年使用:0次
2019-11-03更新
|
534次组卷
|
6卷引用:山西省大同市第一中学2020届高三2月月考理综化学试题
山西省大同市第一中学2020届高三2月月考理综化学试题四川省天府名校2020届高三上学期第一轮联合质量测评化学试题2020届高三《新题速递·化学》12月第01期(考点12-15)(已下线)考点14 物质结构与性质(选考)-2020年高考化学命题预测与模拟试题分类精编广西名校高三2019-2020学年第一学期第一次大联考-化学西南四省名校2020届高三第一次大联考理综化学试题



