名校
1 .  是一种重要的化工产品,实验室可利用
是一种重要的化工产品,实验室可利用 制取该配合物:
制取该配合物: 。已知
。已知 的空间结构如图,其中1~6处的小圆圈表示
的空间结构如图,其中1~6处的小圆圈表示 分子,各相邻的
分子,各相邻的 分子间的距离相等,中心离子
分子间的距离相等,中心离子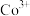 位于八面体的中心,
位于八面体的中心, 分子到中心离子的距离相等(图中虚线长度相等),下列说法正确的是
分子到中心离子的距离相等(图中虚线长度相等),下列说法正确的是
 是一种重要的化工产品,实验室可利用
是一种重要的化工产品,实验室可利用 制取该配合物:
制取该配合物: 。已知
。已知 的空间结构如图,其中1~6处的小圆圈表示
的空间结构如图,其中1~6处的小圆圈表示 分子,各相邻的
分子,各相邻的 分子间的距离相等,中心离子
分子间的距离相等,中心离子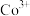 位于八面体的中心,
位于八面体的中心, 分子到中心离子的距离相等(图中虚线长度相等),下列说法正确的是
分子到中心离子的距离相等(图中虚线长度相等),下列说法正确的是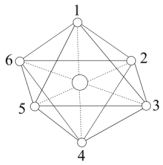
A. 为非极性分子 为非极性分子 |
B. 中键角 中键角 小于 小于 中键角 中键角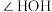 |
C.1 mol  含有 含有 键的数目为18 键的数目为18 |
D.若 中两个 中两个 被 被 替代,得到的 替代,得到的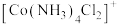 有2种结构 有2种结构 |
您最近一年使用:0次
名校
解题方法
2 . 设阿伏加德罗常数的值为 ,下列叙述正确的是
,下列叙述正确的是
 ,下列叙述正确的是
,下列叙述正确的是A. 与 与 分别熔化,克服的粒子间作用力相同 分别熔化,克服的粒子间作用力相同 |
B.标准状况下,22.4L苯分子中含有 个 个 键 键 |
C.吡啶(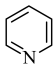 )中有与苯类似的大 )中有与苯类似的大 键, 键, 原子的孤电子对占据 原子的孤电子对占据 杂化轨道 杂化轨道 |
D.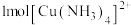 中 中 键的数目为 键的数目为 |
您最近一年使用:0次
解题方法
3 . 化学学科核心素养中提出了宏观辨识与微观探析,要求能从不同层次认识物质的多样性,能从微粒水平认识物质的组成、结构等。下列叙述的化学用语或图示表达正确的是
A. 中阴离子的电子式: 中阴离子的电子式: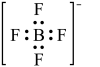 |
B. 的空间填充模型: 的空间填充模型: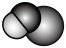 |
C.四水合铜离子 的结构: 的结构: |
D.石墨烯中C原子的杂化: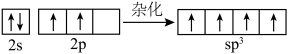 |
您最近一年使用:0次
4 . Fe氧簇MOF催化 与
与 反应的机理如图所示。下列说法正确的是
反应的机理如图所示。下列说法正确的是
 与
与 反应的机理如图所示。下列说法正确的是
反应的机理如图所示。下列说法正确的是
A.根据 分子的结构推测其电子式为 分子的结构推测其电子式为 |
B.总反应方程式为 |
| C.该反应中极性键和非极性键均有断裂和形成 |
| D.该反应中Fe元素的化合价和配位数未发生变化 |
您最近一年使用:0次
5 . 25℃,金属阳离子 与
与 逐步结合的平衡常数如下:
逐步结合的平衡常数如下:
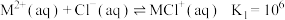


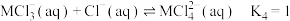
下列说法正确的是[已知:平均配位数
 与
与 逐步结合的平衡常数如下:
逐步结合的平衡常数如下: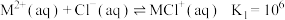


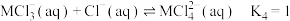
下列说法正确的是[已知:平均配位数

A.溶液中 数目越多, 数目越多,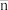 越大 越大 |
B.当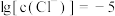 时, 时, 与 与 间不能形成配位键 间不能形成配位键 |
C.已知 ,可推知 ,可推知 的金属活动性强于 的金属活动性强于 |
D.当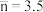 时,溶液中 时,溶液中 略大于 略大于 |
您最近一年使用:0次
名校
6 . 现有两种化学式相同但颜色不同的配合物,它们的化学式均为: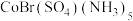 ,配合物A为红色加入
,配合物A为红色加入 生黄色沉淀,但加入
生黄色沉淀,但加入 不产生沉淀,紫色配合物B加入
不产生沉淀,紫色配合物B加入 不产生沉淀,但加入
不产生沉淀,但加入 产生白色沉淀。关于两种配合物说法错误的是:
产生白色沉淀。关于两种配合物说法错误的是:
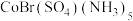 ,配合物A为红色加入
,配合物A为红色加入 生黄色沉淀,但加入
生黄色沉淀,但加入 不产生沉淀,紫色配合物B加入
不产生沉淀,紫色配合物B加入 不产生沉淀,但加入
不产生沉淀,但加入 产生白色沉淀。关于两种配合物说法错误的是:
产生白色沉淀。关于两种配合物说法错误的是:A.红色配合物化学式为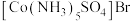 紫色配合物化学式为 紫色配合物化学式为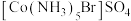 |
| B.两种配合物的中心原子配位数都是6 |
| C.两种配合物中心离子价态均为+3 |
D.两种配合物中心离子均为 杂化 杂化 |
您最近一年使用:0次
名校
7 . 下列实验操作、现象和结论均正确的是
选项 | 操作 | 现象 | 结论 |
A | 向 | 析出深蓝色固体 |
|
B | 向滴有KSCN的 | 溶液褪色 |
|
C | 用毛皮摩擦过的带电橡胶靠近 | 液流方向改变 |
|
D | 向滴有酚酞的NaOH溶液通入 | 溶液褪色 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 设 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是
 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是A.22.4L 中含有C﹣H的数目为 中含有C﹣H的数目为 |
B.1mol 中σ键的个数为 中σ键的个数为 |
C.0.1mol/LNaCl的溶液中 数为 数为 |
D.16g 所含有的电子数为 所含有的电子数为 |
您最近一年使用:0次
9 . 某种新型储氢材料的晶胞如图,八面体中心为金属离子铁,顶点均为 配体;四面体中心为硼原子,顶点均为氢原子。下列说法正确的是(已知:元素电负性
配体;四面体中心为硼原子,顶点均为氢原子。下列说法正确的是(已知:元素电负性 )
)
 配体;四面体中心为硼原子,顶点均为氢原子。下列说法正确的是(已知:元素电负性
配体;四面体中心为硼原子,顶点均为氢原子。下列说法正确的是(已知:元素电负性 )
)
A.该储氢材料的化学式为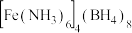 |
B. 金属离子中的未成对电子数为 金属离子中的未成对电子数为 |
| C.晶胞中金属离子的配位数是8 |
| D.基态硼原子的核外电子有5种空间运动状态 |
您最近一年使用:0次
10 . 实验室在如图所示装置中制取 ,将
,将 通入
通入 溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得
溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得 晶体。已知:
晶体。已知: 呈蓝色。下列说法
呈蓝色。下列说法不正确 的是
 ,将
,将 通入
通入 溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得
溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得 晶体。已知:
晶体。已知: 呈蓝色。下列说法
呈蓝色。下列说法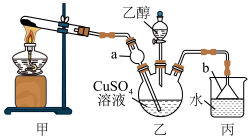
A.在装置甲试管中加入 和 和 固体加热制取 固体加热制取 |
B.装置乙中的 和装置丙中的 和装置丙中的 均可防止倒吸 均可防止倒吸 |
C. 晶体在乙醇中的溶解度小于在水中的溶解度 晶体在乙醇中的溶解度小于在水中的溶解度 |
D.与 相比, 相比, 更易与 更易与 形成配位键 形成配位键 |
您最近一年使用:0次

 溶液中加入乙醇
溶液中加入乙醇 溶液通入
溶液通入
 液流
液流


