名校
解题方法
1 . 乙胺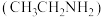 和乙醇
和乙醇 都是重要的有机试剂。下列说法错误的是
都是重要的有机试剂。下列说法错误的是
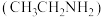 和乙醇
和乙醇 都是重要的有机试剂。下列说法错误的是
都是重要的有机试剂。下列说法错误的是| A.两种分子均易溶于水,且乙胺水溶液呈碱性 | B.上述物质所含元素中C的第一电离能最小 |
| C.两种分子均可通过缩聚反应生成高分子化合物 | D.两种分子中,最多可共平面的原子数目相同 |
您最近一年使用:0次
7日内更新
|
46次组卷
|
2卷引用:河南省部分示范性高中2023-2024学年高二下学期5月联考 化学试题
名校
解题方法
2 . 物质结构决定性质。下列对物质结构与性质的描述错误的是
选项 | 结构 | 性质 |
A | 石墨中每个碳原子上均有1个未参与杂化的 电子,它们所在的原子轨道相互平行且相互重叠 电子,它们所在的原子轨道相互平行且相互重叠 | 石墨具有导电性 |
B |  中的共价键为非极性共价键 中的共价键为非极性共价键 |  为非极性分子 为非极性分子 |
C |  中π电子云重叠程度小于σ电子云 中π电子云重叠程度小于σ电子云 |  易发生加成反应 易发生加成反应 |
D | 邻羟基苯甲醛存在分子内氢键,对羟基苯甲醛存在分子间氢键 | 邻羟基苯甲醛的沸点低于对羟基苯甲醛 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
41次组卷
|
2卷引用:河南省部分示范性高中2023-2024学年高二下学期5月联考 化学试题
3 . 下列事实对应的解释正确的是
| 选项 | 事实 | 解释 |
| A | 向 溶液中加入足量盐酸,产生气泡 溶液中加入足量盐酸,产生气泡 | 非金属性: |
| B | 明矾可用于净水 | 明矾中 水解生成 水解生成 胶体, 胶体, 具有两性 具有两性 |
| C | 硫难溶于水、易溶于二硫化碳 | 硫属于非极性分子,二硫化碳是非极性溶剂,水是极性溶剂 |
| D | 稳定性: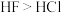 |  分子间存在氢键,而 分子间存在氢键,而 分子间不存在氢键 分子间不存在氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列有关物质结构与性质的说法错误的是
| A.简单氢化物分子间形成的氢键越多,物质的熔、沸点越高 |
| B.超分子具有分子识别和自组装的重要特征 |
C.通过X射线衍射实验可区分晶体 和非晶体 和非晶体 |
| D.离子晶体中阴、阳离子有配位数说明离子键有饱和性 |
您最近一年使用:0次
2024-05-12更新
|
93次组卷
|
2卷引用:河南省漯河市高级中学2023-2024学年高三下学期5月月考化学试题
5 . 可燃冰( ,结构模型如图所示)又称为天然气水合物,是天然气与水在高压低温条件下形成的类冰状结晶物质。
,结构模型如图所示)又称为天然气水合物,是天然气与水在高压低温条件下形成的类冰状结晶物质。
 ,结构模型如图所示)又称为天然气水合物,是天然气与水在高压低温条件下形成的类冰状结晶物质。
,结构模型如图所示)又称为天然气水合物,是天然气与水在高压低温条件下形成的类冰状结晶物质。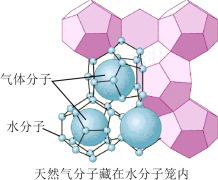
A.键能: | B.键角: |
| C.可燃冰中甲烷分子与水分子间形成了氢键 | D.基态碳原子和氧原子的未成对电子数相同 |
您最近一年使用:0次
名校
6 . 已知 、
、 分别在850℃、300℃能大量分解,对此事实解释合理的是
分别在850℃、300℃能大量分解,对此事实解释合理的是
 、
、 分别在850℃、300℃能大量分解,对此事实解释合理的是
分别在850℃、300℃能大量分解,对此事实解释合理的是A. 能形成氢键而 能形成氢键而 不能 不能 | B.As—H键的键能小于N—H键的键能 |
C. 是极性分子而 是极性分子而 是非极性分子 是非极性分子 | D. 极易溶于水而 极易溶于水而 不能 不能 |
您最近一年使用:0次
7 . 工业合成氨( )是人类科学技术的一项重大突破,对社会发展做出了巨大贡献。
)是人类科学技术的一项重大突破,对社会发展做出了巨大贡献。
(1)基态氮原子的价层电子排布图为______ 。
(2) 在水中的溶解度是常见气体中最大的。
在水中的溶解度是常见气体中最大的。
①下列因素与 的水溶性没有关系的是
的水溶性没有关系的是______ (填字母,下同)。
a. 和
和 都是极性分子
都是极性分子
b. 在水中易形成氢键
在水中易形成氢键
c. 溶于水建立了以下平衡:
溶于水建立了以下平衡:
d. 是一种易液化的气体
是一种易液化的气体
② 溶于水时,大部分
溶于水时,大部分 与
与 通过氢键结合形成
通过氢键结合形成 。根据氨水的性质推知
。根据氨水的性质推知 的结构式为
的结构式为______ 。
a. b.
b.
c. d.
d.
(3)肼的性质与氨气相似,易溶于水,可发生两步电离过程,第一步电离过程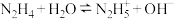 ,试写出第二步电离过程
,试写出第二步电离过程______ 。常温下,某浓度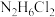 溶液的pH为4,则该溶液中水电离出的
溶液的pH为4,则该溶液中水电离出的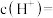
______ 。
(4)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的微粒用*标注。

该反应历程中最大活化能对应骤的化学方程式为______ 。合成氨反应: 的
的
______ kJ/mol(用图中字母表示)
(5)合成氨反应中,正反应速率 ,逆反应速率
,逆反应速率 ,
, 、
、 为速率常数。正反应和逆反应的速率常数与温度的关系如图所示:
为速率常数。正反应和逆反应的速率常数与温度的关系如图所示:

①表示逆反应的速率常数与温度变化关系的曲线为______ (填“c”或“d”),理由为______ 。
②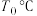 时,
时,
______
(6)用氨气研发燃料电池装置(如图所示),电池反应为 ,使用1mol/L的KOH溶液作电解质溶液,请写出通入a气体一极的电极反应式
,使用1mol/L的KOH溶液作电解质溶液,请写出通入a气体一极的电极反应式______ 。

 )是人类科学技术的一项重大突破,对社会发展做出了巨大贡献。
)是人类科学技术的一项重大突破,对社会发展做出了巨大贡献。(1)基态氮原子的价层电子排布图为
(2)
 在水中的溶解度是常见气体中最大的。
在水中的溶解度是常见气体中最大的。①下列因素与
 的水溶性没有关系的是
的水溶性没有关系的是a.
 和
和 都是极性分子
都是极性分子 b.
 在水中易形成氢键
在水中易形成氢键c.
 溶于水建立了以下平衡:
溶于水建立了以下平衡:
d.
 是一种易液化的气体
是一种易液化的气体②
 溶于水时,大部分
溶于水时,大部分 与
与 通过氢键结合形成
通过氢键结合形成 。根据氨水的性质推知
。根据氨水的性质推知 的结构式为
的结构式为a.
 b.
b.
c.
 d.
d.
(3)肼的性质与氨气相似,易溶于水,可发生两步电离过程,第一步电离过程
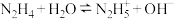 ,试写出第二步电离过程
,试写出第二步电离过程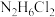 溶液的pH为4,则该溶液中水电离出的
溶液的pH为4,则该溶液中水电离出的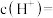
(4)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的微粒用*标注。

该反应历程中最大活化能对应骤的化学方程式为
 的
的
(5)合成氨反应中,正反应速率
 ,逆反应速率
,逆反应速率 ,
, 、
、 为速率常数。正反应和逆反应的速率常数与温度的关系如图所示:
为速率常数。正反应和逆反应的速率常数与温度的关系如图所示:
①表示逆反应的速率常数与温度变化关系的曲线为
②
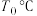 时,
时,
(6)用氨气研发燃料电池装置(如图所示),电池反应为
 ,使用1mol/L的KOH溶液作电解质溶液,请写出通入a气体一极的电极反应式
,使用1mol/L的KOH溶液作电解质溶液,请写出通入a气体一极的电极反应式
您最近一年使用:0次
解题方法
8 . 回答下列问题:
(1)在下列表格中填写各物质的中心原子杂化轨道类型和空间构型:
(2)一定压强下,将HF和HCl混合气体降温时,首先液化的物质是__________ 。
(1)在下列表格中填写各物质的中心原子杂化轨道类型和空间构型:
|
|
|
|
| |
杂化方式 | |||||
空间构型 |
您最近一年使用:0次
2024-04-08更新
|
68次组卷
|
2卷引用:河南省南阳市六校联考2023-2024学年高二下学期3月月考化学试卷
9 . 下列有关物质熔沸点的叙述错误的是
A.因为碳氢键键能小于碳氧键,所以 熔点低于 熔点低于 |
B. 的沸点高于 的沸点高于 |
C.F、Cl、O三种元素的简单氢化物沸点由高到低的顺序为 |
D.对羟基苯甲醛(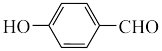 )的熔沸点高于邻羟基苯甲醛( )的熔沸点高于邻羟基苯甲醛(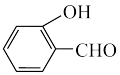 ) ) |
您最近一年使用:0次
2024-04-08更新
|
80次组卷
|
2卷引用:河南省南阳市六校联考2023-2024学年高二下学期3月月考化学试卷
名校
10 . 短周期主族元素X、Y、Z、W、M的原子半径依次增大,与元素有关的信息如表所示:
回答下列问题:
(1) 的一种核素含有8个中子,其核素符号为
的一种核素含有8个中子,其核素符号为___________ ,写出其简单氢化物的一种用途:___________ 。
(2)由 与
与 组成的化合物含有的化学键类型为
组成的化合物含有的化学键类型为___________ 。
(3)上述元素对应的简单离子中半径最大的为___________ (填离子符号)。
(4) 单质与
单质与 的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为
的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为___________ 。
(5) 与
与 形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程
形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程___________ 。
(6) 的简单氢化物的沸点比
的简单氢化物的沸点比 的简单氢化物的沸点高,从结构角度分析其原因为
的简单氢化物的沸点高,从结构角度分析其原因为___________ 。
(7)下列关于 及
及 同主族元素的说法错误的是___________。
同主族元素的说法错误的是___________。
| 元素 | 相关信息 |
 | 简单氢化物的水溶液可以刻蚀玻璃 |
 | 最外层电子数比次外层多3 |
 | 最高正价和最低负价的代数和为4 |
 | 地壳中含量最高的金属元素 |
 | 最高价氧化物对应水化物属于强碱 |
(1)
 的一种核素含有8个中子,其核素符号为
的一种核素含有8个中子,其核素符号为(2)由
 与
与 组成的化合物含有的化学键类型为
组成的化合物含有的化学键类型为(3)上述元素对应的简单离子中半径最大的为
(4)
 单质与
单质与 的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为
的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为(5)
 与
与 形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程
形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程(6)
 的简单氢化物的沸点比
的简单氢化物的沸点比 的简单氢化物的沸点高,从结构角度分析其原因为
的简单氢化物的沸点高,从结构角度分析其原因为(7)下列关于
 及
及 同主族元素的说法错误的是___________。
同主族元素的说法错误的是___________。A.将 的单质通入其同族元素与钠形成的钠盐溶液中,可置换出同族元素的单质 的单质通入其同族元素与钠形成的钠盐溶液中,可置换出同族元素的单质 |
| B.随着原子序数递增,该主族元素对应单质的沸点逐渐升高 |
C.该主族元素中最高价氧化物对应水化物酸性最强的元素为 |
D. 的简单氢化物可与强碱溶液反应 的简单氢化物可与强碱溶液反应 |
您最近一年使用:0次