名校
1 . 磷和砷的相关化合物在化工、医药、材料等领域有着广泛应用。回答下列问题:
(1)红磷是巨型共价分子,无定形结构,下列方法能证明红磷是非晶体的是___________。
(2)第一电离能介于Al、P之间的第三周期元素有___________ 种。
(3)如图所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是___________ 。

(4)黑磷是新型二维半导体材料,具有片层结构(如图所示),P在元素周期表分区中属于___________ 区,层与层之间的相互作用力为___________ 。

(5)N、P、As、Sb均是第ⅤA族的元素,As原子的逐级电离能数据如下:
第五电离能与第六电离能相差较大的原因:___________ 。
(1)红磷是巨型共价分子,无定形结构,下列方法能证明红磷是非晶体的是___________。
| A.质谱法 | B.原子发射光谱法 |
| C.核磁共振谱法 | D.X射线衍射法 |
(3)如图所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(4)黑磷是新型二维半导体材料,具有片层结构(如图所示),P在元素周期表分区中属于

(5)N、P、As、Sb均是第ⅤA族的元素,As原子的逐级电离能数据如下:
| 第一电离能 | 第二电离能 | 第三电离能 | 第四电离能 | 第五电离能 | 第六电离能 |
| 947.0 | 1 798 | 2 735 | 4 837 | 6 043 | 12 310 |
第五电离能与第六电离能相差较大的原因:
您最近一年使用:0次
2 . 化学处处呈现美。下列有关说法正确的是
A. 分子呈现完美对称,为V形结构 分子呈现完美对称,为V形结构 |
| B.NaCl焰色试验为黄色,与氯原子的电子跃迁有关 |
| C.冰雪融化时需要破坏氢键和范德华力 |
| D.镁条燃烧发出耀眼的白光,只将化学能转化为光能 |
您最近一年使用:0次
名校
3 . 磷酸奥司他韦(分子式为 )在治疗流感方面发挥重要作用,其分子结构如图所示,下列有关磷酸奥司他韦的说法错误是
)在治疗流感方面发挥重要作用,其分子结构如图所示,下列有关磷酸奥司他韦的说法错误是
 )在治疗流感方面发挥重要作用,其分子结构如图所示,下列有关磷酸奥司他韦的说法错误是
)在治疗流感方面发挥重要作用,其分子结构如图所示,下列有关磷酸奥司他韦的说法错误是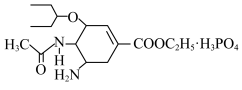
A.能与3mol  反应 反应 | B.能与强酸、强碱反应 |
| C.可形成分子内氢键、分子间氢键 | D.能发生氧化、还原、取代、加成反应 |
您最近一年使用:0次
2024-04-28更新
|
649次组卷
|
2卷引用:广东省汕头市2024届高三二模考试化学试
解题方法
4 . W、X、Y、Z是原子序数依次增大的主族元素,在前三周期均有分布,基态X原子有四种不同空间运动状态的电子;Y为地壳中含量最多的元素,其简单离子与Z的简单离子具有相同电子数;工业上常通过电解Z的氧化物制取其单质,下列说法不正确的是
A.元素电负性: | B.简单氢化物的沸点: |
C.原子半径: | D.Z同周期且第一电离能小于Z的元素有2种 |
您最近一年使用:0次
5 . 短周期元素甲、乙、丙、丁、戊在元素周期表中的相对位置如图所示,已知戊的非金属性最强且其基态原子 轨道只有一个未成对电子。下列说法错误的是
轨道只有一个未成对电子。下列说法错误的是
 轨道只有一个未成对电子。下列说法错误的是
轨道只有一个未成对电子。下列说法错误的是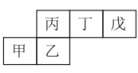
| A.简单离子半径:丙>丁>戊 | B.简单氢化物的沸点:乙<丙 |
| C.简单氢化物的键角:甲>乙 | D.第一电离能:甲<乙<丙<丁<戊 |
您最近一年使用:0次
2024-02-24更新
|
521次组卷
|
2卷引用:广东省2024届高三下学期2月份大联考 化学试题
6 . 尿素的结构可表示为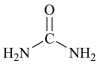 ,下列有关说法正确的是
,下列有关说法正确的是
 ,下列有关说法正确的是
,下列有关说法正确的是A. 分子中含有 分子中含有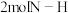 键 键 |
B.根据结构推测,尿素易溶于水,其熔、沸点低于丙酮(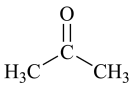 ) ) |
C.组成尿素的四种元素的电负性由大到小的顺序是 |
D. 与 与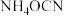 (氰酸铵)互为同分异构体 (氰酸铵)互为同分异构体 |
您最近一年使用:0次
名校
解题方法
7 . 硫、硒、碲的化合物在农药、石油工业、矿物开采、萃取及有机合成等领域的应用广泛。回答下列问题:
(1)基态Se原子的价层电子排布式为___________ 。
(2)下列有关氧族元素单质及其化合物的性质说法正确的是___________。
(3)类卤素 分子结构式为
分子结构式为___________ ,1mol 中含有π键的数目为
中含有π键的数目为___________ ,HSCN结构有两种,已知硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸( ),其原因是
),其原因是___________ 。
(4)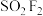 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是___________ 。
___________  (填“>”或“<”或“=”),其原因是
(填“>”或“<”或“=”),其原因是___________ 。
(1)基态Se原子的价层电子排布式为
(2)下列有关氧族元素单质及其化合物的性质说法正确的是___________。
A.氧族元素气态氢化物的稳定性按 、 、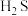 、 、 、 、 的顺序依次减弱 的顺序依次减弱 |
| B.其氢化物中的键长按O―H、S―H、Se―H、Te―H的顺序依次减小 |
C.其阴离子的还原性按 、 、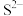 、 、 、 、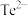 的顺序依次增强 的顺序依次增强 |
D.其最高价氧化物的水化物酸性按 、 、 、 、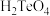 顺序依次增强 顺序依次增强 |
(3)类卤素
 分子结构式为
分子结构式为 中含有π键的数目为
中含有π键的数目为 )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸( ),其原因是
),其原因是(4)
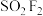 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是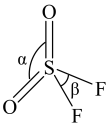

 (填“>”或“<”或“=”),其原因是
(填“>”或“<”或“=”),其原因是
您最近一年使用:0次
名校
8 . 下列有关物质结构与性质的说法错误的是
A. 易溶于 易溶于 ,可从 ,可从 和 和 都是非极性分子的角度解释 都是非极性分子的角度解释 |
B.熔融 能导电,是由于熔融状态下产生了自由移动的 能导电,是由于熔融状态下产生了自由移动的 和 和 |
C. 溶于氨水,是由于 溶于氨水,是由于 与 与 反应生成了可溶性配合物 反应生成了可溶性配合物 |
| D.对羟基苯甲酸存在分子内氢键,是其沸点比邻羟基苯甲酸高的主要原因 |
您最近一年使用:0次
2024-04-16更新
|
66次组卷
|
2卷引用:广东省深圳市光明区高级中学2023-2024学年高三下学期5月模拟考试化学试题
解题方法
9 . 下列说法中正确的是
A.硫难溶于水,微溶于酒精,易溶于 ,说明分子极性: ,说明分子极性: |
| B.非极性分子中只有非极性键,极性分子中只有极性键。 |
| C.邻羟基苯甲醛能形成分子内氢键,而对羟基苯甲醛能形成分子间氢键,所以前者的熔点高于后者 |
| D.乙醇分子和水分子间只存在范德华力 |
您最近一年使用:0次
名校
解题方法
10 . 下列说法中正确的有
①金属晶体的导电性、导热性均与自由电子有关
②水结成冰密度减小与水分子之间能形成氢键有关
③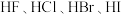 的热稳定性和还原性依次减弱
的热稳定性和还原性依次减弱
④共价键的强弱决定分子晶体熔、沸点的高低
⑤ 的热稳定性依次减弱,熔沸点依次升高
的热稳定性依次减弱,熔沸点依次升高
⑥硬度由大到小:金刚石>碳化硅 晶体硅
晶体硅
①金属晶体的导电性、导热性均与自由电子有关
②水结成冰密度减小与水分子之间能形成氢键有关
③
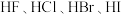 的热稳定性和还原性依次减弱
的热稳定性和还原性依次减弱④共价键的强弱决定分子晶体熔、沸点的高低
⑤
 的热稳定性依次减弱,熔沸点依次升高
的热稳定性依次减弱,熔沸点依次升高⑥硬度由大到小:金刚石>碳化硅
 晶体硅
晶体硅| A.②③④⑥ | B.①②③⑥ | C.①②④⑤ | D.①②⑤⑥ |
您最近一年使用:0次
2024-02-29更新
|
1200次组卷
|
4卷引用:广东省梅州市大埔县虎山中学2023-2024学年高二下学期4月期中考试化学试题



