1 . 氢、氮、氯、铜是元素周期表中前四周期元素。回答下列问题:
(1)铜在元素周期表中的位置__ ,写出NH3的电子式__ 。
(2)氯与硫相比,非金属性较强的是__ (用元素符号表示),下列事实能证明这一结论的是__ 。(填序号)。
a.常温下氯的单质呈气态,硫的单质呈固态
b.稳定性:HCl>H2S
c.酸性:HClO4>H2SO4
d.氯的电负性大于硫的电负性
(3)含氮化合物(CH3)3N与盐酸反应,离子方程式为:(CH3)3N+H+=[(CH3)3NH]+,该反应过程中新生成的化学键为___ (填序号)。
a.离子键 b.配位键 c.氢键 d.非极性共价键
若化合物(CH3)3N能溶于水,其可能的原因是___ 。
(4)Cu与H元素形成某种晶体的结构如图所示,则该晶体的化学式为__ ,若该晶体的密度为ρ g•cm-3,阿伏加 德罗常数的值为NA,则该晶胞的棱长为__ nm(用含ρ和NA的式子表示,已知1nm=10-7cm)。

(1)铜在元素周期表中的位置
(2)氯与硫相比,非金属性较强的是
a.常温下氯的单质呈气态,硫的单质呈固态
b.稳定性:HCl>H2S
c.酸性:HClO4>H2SO4
d.氯的电负性大于硫的电负性
(3)含氮化合物(CH3)3N与盐酸反应,离子方程式为:(CH3)3N+H+=[(CH3)3NH]+,该反应过程中新生成的化学键为
a.离子键 b.配位键 c.氢键 d.非极性共价键
若化合物(CH3)3N能溶于水,其可能的原因是
(4)Cu与H元素形成某种晶体的结构如图所示,则该晶体的化学式为

您最近一年使用:0次
2 . 化学处处呈现美。下列说法不正确的是
| A.雪花是天空中的水汽经凝华而来的一种晶体,其六角形形状与氢键的方向性有关 |
B. 与18-冠-6的空腔大小相近,形成稳定的超分子结构( 与18-冠-6的空腔大小相近,形成稳定的超分子结构(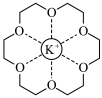 ),这体现出超分子的自组装特征 ),这体现出超分子的自组装特征 |
| C.缺角的NaCl晶体在饱和NaCl溶液中变为完美立方体块,体现晶体的自范性 |
| D.绚烂烟花的产生是电子由较高能量的激发态跃迁到较低能量的激发态乃至基态时,能量以光的形式释放引起的 |
您最近一年使用:0次
名校
3 . 下列关于物质熔、沸点高低说法错误的是
| A.熔点:金刚石>碳化硅>晶体硅>冰>干冰 |
| B.分子晶体中共价键的键能越大,其熔、沸点越高 |
| C.H2S、H2Se、H2Te的熔、沸点依次升高 |
| D.MgO比NaCl熔点高 |
您最近一年使用:0次
名校
解题方法
4 . 如图为冰晶体的结构模型,大球代表O原子,小球代表H原子,下列有关说法正确的是
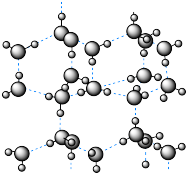
| A.冰晶体中每个水分子与另外四个水分子形成四面体 |
| B.冰晶体具有共价键三维骨架结构,是共价晶体 |
C.水分子间通过 形成冰晶体 形成冰晶体 |
| D.冰晶体融化时,水分子间的空隙增大 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法不正确 的是
A. 中 中 键角比 键角比 中的小 中的小 |
B.接近水的沸点的水蒸气的相对分子质量测定值比按化学式 计算出来的大,是由于氢键的影响 计算出来的大,是由于氢键的影响 |
C.用湿润的蓝色石蕊试纸可鉴别 和HCl 和HCl |
D.非极性分子往往具有高度对称性,如 、 、 、 、 、 、 这样的分子 这样的分子 |
您最近一年使用:0次
名校
6 . 下列说法不正确 的是
| A.通过X射线衍射可测定青蒿素晶体的结构 |
| B.利用盐析的方法可将蛋白质从溶液中分离 |
| C.邻羟基苯甲醛在水中的溶解度高于对羟基苯甲醛在水中的溶解度 |
| D.可用新制氢氧化铜悬浊液鉴别苯、乙醇、乙醛、甲酸和醋酸溶液 |
您最近一年使用:0次
名校
7 . 下列说法不正确的是
A.乳酸[ ]分子中存在一个手性碳原子 ]分子中存在一个手性碳原子 |
B.热稳定性: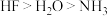 |
C.沸点: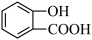 < < |
| D.强度:氢键>化学键>范德华力 |
您最近一年使用:0次
名校
解题方法
8 . 甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确 的是
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A.原子半径:丁>戊>乙 |
| B.乙的简单氢化物的沸点一定高于戊的简单氢化物的沸点 |
| C.甲的简单氢化物遇氯化氢一定有白烟产生 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近一年使用:0次
解题方法
9 . 下列说法不正确 的是
| A.键角:H2O<NH3 | B.键长:Cl-Cl<Br-Br |
| C.酸性:CH3COOH<CH2ClCOOH | D.沸点:对羟基苯甲醛<邻羟基苯甲醛 |
您最近一年使用:0次
2023·山东济南·一模
名校
解题方法
10 . 呋喃(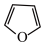 )和四氢呋喃(
)和四氢呋喃(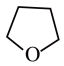 )常用作有机溶剂,呋喃中含
)常用作有机溶剂,呋喃中含 大
大 键。下列说法错误的是
键。下列说法错误的是
 )和四氢呋喃(
)和四氢呋喃( )常用作有机溶剂,呋喃中含
)常用作有机溶剂,呋喃中含 大
大 键。下列说法错误的是
键。下列说法错误的是A.呋喃与 的加成产物有三种 的加成产物有三种 |
| B.呋喃在乙醇中溶解度小于苯中的 |
C.呋喃与四氢呋喃中含 键数目比为9∶13 键数目比为9∶13 |
D. 键角:呋喃>四氢呋喃 键角:呋喃>四氢呋喃 |
您最近一年使用:0次



