1 . 回答下列问题:
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(COCl2):2CHCl3+O2→2HCl+2COCl2,光气(COCl2)分子的立体构型是_______ 形。
(2)某有机物的结构简式为 。该有机物分子是
。该有机物分子是_______ (填“极性”或“非极性”)分子,该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序为_______ 。
(3)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为_______ ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高很多,原因_______
(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为N2H4+HNO2=2H2O+HN3.HN3的酸性和醋酸相近,可微弱电离出H+和N 。
。
①叠氮酸根能与许多金属离子等形成配合物,如[Co(N3)(NH3)5]SO4,根据价层电子对互斥理论判断SO 的空间构型为
的空间构型为_______ 。
②下列有关说法正确的是_______ (填序号)。
A.HN3中含有5个σ键
B.HN3中的三个氮原子均采用sp2杂化
C.HN3、HNO2、H2O、N2H4都是极性分子
D.肼(N2H4)的沸点高达113.5℃,说明肼分子间可形成氢键
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(COCl2):2CHCl3+O2→2HCl+2COCl2,光气(COCl2)分子的立体构型是
(2)某有机物的结构简式为
 。该有机物分子是
。该有机物分子是(3)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为
(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为N2H4+HNO2=2H2O+HN3.HN3的酸性和醋酸相近,可微弱电离出H+和N
 。
。①叠氮酸根能与许多金属离子等形成配合物,如[Co(N3)(NH3)5]SO4,根据价层电子对互斥理论判断SO
 的空间构型为
的空间构型为②下列有关说法正确的是
A.HN3中含有5个σ键
B.HN3中的三个氮原子均采用sp2杂化
C.HN3、HNO2、H2O、N2H4都是极性分子
D.肼(N2H4)的沸点高达113.5℃,说明肼分子间可形成氢键
您最近一年使用:0次
解题方法
2 . 下列关于晶体的说法中,正确的是
| A.冰融化时,分子中H—O键发生断裂 |
| B.共价晶体中,共价键的键能越大,熔点越高 |
| C.分子晶体中,共价键的键能越大,该晶体的熔、沸点一定越高 |
| D.分子晶体中,分子间作用力越大,对应的物质越稳定 |
您最近一年使用:0次
名校
解题方法
3 . 下列说法不正确的是
A.乳酸分子(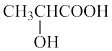 )是手性分子 )是手性分子 |
| B.水蒸气、液态水和冰中均存在氢键 |
C.硫难溶于水,微溶于酒精,易溶于 ,说明分子极性: ,说明分子极性: |
D.酸性: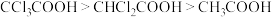 是因为Cl原子电负性大,使得羟基O-H键极性增强,易电离出 是因为Cl原子电负性大,使得羟基O-H键极性增强,易电离出 |
您最近一年使用:0次
名校
解题方法
4 . 下列说法中不正确的是
| A.价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数 |
| B.三氟乙酸的酸性大于三氯乙酸是由于键的极性不同导致电离出氢离子能力不同 |
| C.对羟基苯甲醛不可能形成分子内氢键,只能在分子间形成氢键 |
| D.氯气易溶于氢氧化钠溶液是因为“相似相溶”规律导致的 |
您最近一年使用:0次
2023-03-06更新
|
289次组卷
|
3卷引用:新疆生产建设兵团第三师图木舒克市第一中学2022-2023学年高二下学期3月第一次月考化学试卷
名校
解题方法
5 . 下列说法错误的是
| A.两个原子之间如含有π键,则一定含有1个σ键 |
B. 中含有非极性键,但属于极性分子 中含有非极性键,但属于极性分子 |
C. 、 、 、 、 、 、 的沸点逐渐升高 的沸点逐渐升高 |
| D.气体单质分子中不一定有σ键和π键 |
您最近一年使用:0次
2023-05-07更新
|
74次组卷
|
3卷引用:新疆且末县第一中学2022-2023学年高二下学期6月期末考试化学试题
名校
解题方法
6 . 关于 、
、 、
、 三种物质的说法中正确的是
三种物质的说法中正确的是
 、
、 、
、 三种物质的说法中正确的是
三种物质的说法中正确的是
A. 在水中的溶解度很小,是由于其属于极性分子 在水中的溶解度很小,是由于其属于极性分子 |
B. 和 和 均易溶于水,原因之一是它们都是极性分子 均易溶于水,原因之一是它们都是极性分子 |
C. 和 和 的分子结构相似,均为非极性分子 的分子结构相似,均为非极性分子 |
D. 在水中溶解度很大只是由于 在水中溶解度很大只是由于 分子有极性 分子有极性 |
您最近一年使用:0次
2023-05-02更新
|
90次组卷
|
2卷引用:新疆维吾尔自治区皮山县高级中学2022-2023学年高二下学期4月期中化学试题
名校
解题方法
7 . 下图是元素周期表的一部分,五种元素属于前四周期主族元素,其中只有M为金属元素。下列说法不正确的是
| X | ||
| M | N | Y |
| Z |
| A.Y的最高价氧化物对应水化物的酸性比Z的强 |
| B.M元素与Z元素原子序数差为20 |
| C.X的简单气态氢化物的沸点比Y的低 |
| D.N原子的简单氢化物含有四对共用电子对 |
您最近一年使用:0次
2023-01-26更新
|
292次组卷
|
2卷引用:新疆维吾尔自治区乌苏市第一中学2022-2023学年高一上学期1月月考化学试题
名校
解题方法
8 . 下列有关微粒间作用力的说法不正确的是
| A.碘晶体升华只破坏了分子间的作用力 |
| B.氯化钠熔化或氯化氢溶于水都要破坏化学键 |
C. 分子之间可以形成氢键,导致熔沸点 分子之间可以形成氢键,导致熔沸点 |
D. 属于离子化合物,含有离子键、极性共价键和非极性共价键 属于离子化合物,含有离子键、极性共价键和非极性共价键 |
您最近一年使用:0次
2023-05-04更新
|
189次组卷
|
2卷引用:新疆且末县第一中学2022-2023学年高二下学期6月期末考试化学试题
名校
解题方法
9 . 关于分子的性质,下列说法不正确 的是
| A.H-Cl的键能比H-I的键能大,故HCl分子比HI分子稳定 |
| B.三氯乙酸酸性大于一氯乙酸,是因为Cl3C-的极性大于ClH2C- |
| C.乙醇在水中的溶解度小于丁醇(CH3CH2CH2CH2OH),可以用相似相溶解释 |
| D.分子晶体的熔点通常比共价晶体的熔点低得多 |
您最近一年使用:0次
2023-03-18更新
|
426次组卷
|
4卷引用: 新疆生产建设兵团第二师八一中学2022-2023学年高二下学期期中考试化学试题
10 . 下列说法中正确的是
A.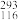 Lv的相对原子质量为293 Lv的相对原子质量为293 |
| B.H2O的稳定性大于H2S,是因为水分子间存在氢键 |
| C.质子数相同,电子数也相同的两种微粒,不可能是一种分子和一种离子 |
| D.元素的非金属性越强,其气态氢化物水溶液的酸性越强 |
您最近一年使用:0次



