名校
解题方法
1 . 下列物质的性质或数据与氢键无关的是
| A.氨气很容易液化 |
B.邻羟基苯甲酸(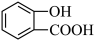 )的熔点为 )的熔点为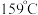 ,对羟基苯甲酸( ,对羟基苯甲酸(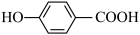 )的熔点为 )的熔点为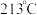 |
| C.乙醚微溶于水,而乙醇可与水以任意比互溶 |
D. 分解时吸收的热量比 分解时吸收的热量比 分解时吸收的热量多 分解时吸收的热量多 |
您最近半年使用:0次
2 . 短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法正确的是
元素 最高价 氧化物的水化物 | X | Y | Z | W |
| 分子式 | 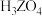 | |||
 溶液对应的pH(25℃) 溶液对应的pH(25℃) | 1.00 | 13.00 | 1.57 | 0.70 |
| A.元素电负性:Z<W | B.简单离子半径:W<Y |
| C.含氧酸酸性强弱:Z<W | D.简单氢化物的沸点:X<Z |
您最近半年使用:0次
名校
解题方法
3 . 下列物质性质排序错误的是
A.酸性: | B.沸点: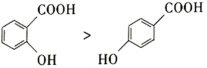 |
C.熔点: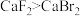 | D.稳定性: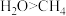 |
您最近半年使用:0次
2024-04-19更新
|
267次组卷
|
2卷引用:天津市滨海新区塘沽一中2023-2024学年高二下学期第一次月考化学试卷
名校
解题方法
4 . 请回答下列问题:
(1)第VIII族元素Fe、Co、Ni性质相似,称为铁系元素,主要用于制造合金。基态Ni原子有_____ 种运动状态的电子,核外能量最高的电子位于_____ 能级;Ni属于_____ 区(填“s”或“p”或“d”或“f”)。
(2)Fe3+与酚类物质的显色反应常用于离子检验,已知Fe3+遇邻苯二酚(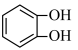 )和对苯二酚(
)和对苯二酚(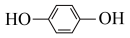 )均显绿色。邻苯二酚的熔、沸点比对苯二酚
)均显绿色。邻苯二酚的熔、沸点比对苯二酚______ (填“高”或“低”),原因是_______ 。
(3)结合VSEPR理论模型及杂化轨道理论分析以下问题:
①Bi(NO3)3中阴离子的立体构型为_______ ,N原子的杂化方式为_____ 。
②NaN3中 的空间结构为
的空间结构为_______ ,其中心原子的杂化类型为______ 。分析微粒空间结构的方法______ 。
(4)60g SiO2中含有的Si−O键数目为____ (用NA表示);1 mol冰中含有___ mol氢键。
(1)第VIII族元素Fe、Co、Ni性质相似,称为铁系元素,主要用于制造合金。基态Ni原子有
(2)Fe3+与酚类物质的显色反应常用于离子检验,已知Fe3+遇邻苯二酚(
 )和对苯二酚(
)和对苯二酚( )均显绿色。邻苯二酚的熔、沸点比对苯二酚
)均显绿色。邻苯二酚的熔、沸点比对苯二酚(3)结合VSEPR理论模型及杂化轨道理论分析以下问题:
①Bi(NO3)3中阴离子的立体构型为
②NaN3中
 的空间结构为
的空间结构为(4)60g SiO2中含有的Si−O键数目为
您最近半年使用:0次
名校
5 . 下列关于物质熔、沸点高低说法错误的是
| A.熔点:金刚石>碳化硅>晶体硅>冰>干冰 |
| B.分子晶体中共价键的键能越大,其熔、沸点越高 |
| C.H2S、H2Se、H2Te的熔、沸点依次升高 |
| D.MgO比NaCl熔点高 |
您最近半年使用:0次
名校
6 . 下列说法正确的是
| A.Na2O2和 NaOH 所含化学键类型完全相同 |
| B.NH3比 PH3稳定是因为NH3分子间存在氢键 |
| C.气体单质中,一定有σ键,可能有π键 |
| D.H2O2 是含极性键和非极性键的极性分子 |
您最近半年使用:0次
名校
解题方法
7 . 下列叙述中正确的是
| A.NH3、CO、CO2都是极性分子 |
| B.CH4、CCl4都是含有极性键的非极性分子 |
| C.HF、HCl、HBr、HI的稳定性依次增强 |
| D.HF、HCl、HBr、HI的熔沸点逐渐升高 |
您最近半年使用:0次
名校
解题方法
8 . 如图为冰晶体的结构模型,大球代表O原子,小球代表H原子,下列有关说法正确的是
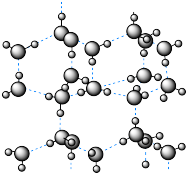
| A.冰晶体中每个水分子与另外四个水分子形成四面体 |
| B.冰晶体具有共价键三维骨架结构,是共价晶体 |
C.水分子间通过 形成冰晶体 形成冰晶体 |
| D.冰晶体融化时,水分子间的空隙增大 |
您最近半年使用:0次
名校
解题方法
9 . 下列说法正确的是
| A.冰融化时,分子中H—O发生断裂 |
| B.共价晶体中,共价键越强,熔点越高 |
| C.分子晶体中,分子间作用力越大,对应的物质越稳定 |
| D.所有分子晶体中都存在化学键 |
您最近半年使用:0次
名校
解题方法
10 . 下列物质的结构或性质与氢键无关的是
| A.冰的密度比水的小 | B.沸点:水 硫化氢 硫化氢 |
| C.水加热到很高温度都难分解 | D.DNA的双螺旋结构 |
您最近半年使用:0次



