名校
1 . 下列叙述中正确的个数有 程中形成的是发射光谱
程中形成的是发射光谱
③第二周期元素中,氟的第一电离能最大
④用红外光谱只能确定有机物中的官能团
⑤ 中
中 键的键长比
键的键长比 中
中 键的键长短
键的键长短
⑥ 的稳定性逐渐减弱,而熔沸点逐渐升高
的稳定性逐渐减弱,而熔沸点逐渐升高
⑦用 射线衍射实验来区分晶体和非晶体
射线衍射实验来区分晶体和非晶体
③干冰升华时,分子内共价键会发生断裂
①氧原子的电子排布图: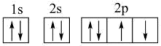 最外层违背了泡利原理
最外层违背了泡利原理
 程中形成的是发射光谱
程中形成的是发射光谱③第二周期元素中,氟的第一电离能最大
④用红外光谱只能确定有机物中的官能团
⑤
 中
中 键的键长比
键的键长比 中
中 键的键长短
键的键长短⑥
 的稳定性逐渐减弱,而熔沸点逐渐升高
的稳定性逐渐减弱,而熔沸点逐渐升高⑦用
 射线衍射实验来区分晶体和非晶体
射线衍射实验来区分晶体和非晶体③干冰升华时,分子内共价键会发生断裂
| A.0个 | B.1个 | C.2个 | D.3个 |
您最近半年使用:0次
名校
2 . 某种电解质的组成如图所示,已知该化合物的五元环上的5个原子共平面,且X、Y、Z、Q、W为原子序数依次增大的短周期元素,下列说法正确的是

| A.Z分别与F、Cl形成最简单的分子中,与F形成的分子键角更大 |
B. 中含有配位键 中含有配位键 |
C.冰的分子间氢键 |
D.在该物质中Z有 , , 的两种杂化方式 的两种杂化方式 |
您最近半年使用:0次
名校
解题方法
3 . 已知 、
、 、
、 、
、 、
、 是原子序数依次增大的五种短周期元素,
是原子序数依次增大的五种短周期元素, 和
和 组成的一种化合物具有强氧化性,可用于自来水消毒,五种元素形成的某种化合物结构如图,下列说法正确的是
组成的一种化合物具有强氧化性,可用于自来水消毒,五种元素形成的某种化合物结构如图,下列说法正确的是
 、
、 、
、 、
、 、
、 是原子序数依次增大的五种短周期元素,
是原子序数依次增大的五种短周期元素, 和
和 组成的一种化合物具有强氧化性,可用于自来水消毒,五种元素形成的某种化合物结构如图,下列说法正确的是
组成的一种化合物具有强氧化性,可用于自来水消毒,五种元素形成的某种化合物结构如图,下列说法正确的是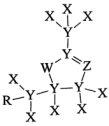
A.原子半径: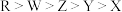 |
B.简单氢化物的沸点: |
C. 单质均为非极性分子 单质均为非极性分子 |
D. 和 和 组成的化合物可能含有非极性键 组成的化合物可能含有非极性键 |
您最近半年使用:0次
7日内更新
|
402次组卷
|
4卷引用:东北三省四城市联考暨沈阳市高三下学期质量监测(二)化学试题
4 . X、Y、Z、W、R为原子序数依次增大的前20号元素,X元素的s轨道电子数是p轨道电子数的2倍,Z元素的最外层电子数是次外层电子数的3倍,常温下,0.05mol/L W的最高价氧化物对应的水化物溶液中,由水电离出的 为
为 ,R是前20号元素中电负性最小的元素。下列说法错误的是
,R是前20号元素中电负性最小的元素。下列说法错误的是
 为
为 ,R是前20号元素中电负性最小的元素。下列说法错误的是
,R是前20号元素中电负性最小的元素。下列说法错误的是| A.简单离子半径:R<W | B.X、Y、Z的氢化物中,沸点最高的是Z的氢化物 |
| C.Y、Z、W中,第一电离能最大的是Y | D.Z分别与W、R均可形成具有漂白性的化合物 |
您最近半年使用:0次
5 .  具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用是科学研究的重要课题。
的合成及应用是科学研究的重要课题。
(1)以 、
、 合成
合成 ,Fe是常用的催化剂。
,Fe是常用的催化剂。
① 分子空间构型为
分子空间构型为________ ,写出 极易溶于水的原因
极易溶于水的原因________ 。
②实际生产中采用铁的氧化物 、FeO,使用前用
、FeO,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:

ⅰ.两种晶胞所含铁原子个数比为________ 。
ⅱ.图1晶胞的棱长为apm( ),则其密度
),则其密度
________  (写出化简的表达式)。
(写出化简的表达式)。
③我国科学家开发出Fe-LiH双中心催化剂,在合成 中显示出高催化活性。第一电离能
中显示出高催化活性。第一电离能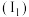 :
: ,从原子结构角度解释原因
,从原子结构角度解释原因________ 。
(2) 、
、 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
① 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为________ 。
② 存在配位键,提供空轨道的是
存在配位键,提供空轨道的是________ 。其他含氮配合物,如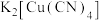 的配离子是
的配离子是________ 、配合物 的配体是
的配体是________ ,配位数为________ 。
(3)常温下 是橙黄色液体,其分子结构如图所示。
是橙黄色液体,其分子结构如图所示。
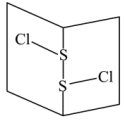
少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。
 分子中含有
分子中含有________ 键(填“极性”、“非极性”,下同),是________ 分子。
(4)已知N、P、As为同一主族元素,则写出三种元素最简单氢化物沸点由高到低的顺序为(用化学式表示)________ 。
 具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用是科学研究的重要课题。
的合成及应用是科学研究的重要课题。(1)以
 、
、 合成
合成 ,Fe是常用的催化剂。
,Fe是常用的催化剂。①
 分子空间构型为
分子空间构型为 极易溶于水的原因
极易溶于水的原因②实际生产中采用铁的氧化物
 、FeO,使用前用
、FeO,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
ⅰ.两种晶胞所含铁原子个数比为
ⅱ.图1晶胞的棱长为apm(
 ),则其密度
),则其密度
 (写出化简的表达式)。
(写出化简的表达式)。③我国科学家开发出Fe-LiH双中心催化剂,在合成
 中显示出高催化活性。第一电离能
中显示出高催化活性。第一电离能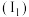 :
: ,从原子结构角度解释原因
,从原子结构角度解释原因(2)
 、
、 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。①
 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为②
 存在配位键,提供空轨道的是
存在配位键,提供空轨道的是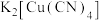 的配离子是
的配离子是 的配体是
的配体是(3)常温下
 是橙黄色液体,其分子结构如图所示。
是橙黄色液体,其分子结构如图所示。
少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。
 分子中含有
分子中含有(4)已知N、P、As为同一主族元素,则写出三种元素最简单氢化物沸点由高到低的顺序为(用化学式表示)
您最近半年使用:0次
解题方法
6 . 下列关于范德华力与氢键的叙述中正确的是
| A.范德华力比氢键的作用还要弱 |
| B.物质的物理性质只与范德华力有关 |
| C.范德华力与氢键的强弱都只与相对分子质量有关 |
| D.任何物质中都存在范德华力,而氢键只存在于含有N、O、F的物质中 |
您最近半年使用:0次
名校
解题方法
7 . 下列说法中,正确的是
A. 空间结构为正四面体形,与VSEPR模型一致 空间结构为正四面体形,与VSEPR模型一致 |
| B.离子晶体中不可能存在共价键 |
| C.共价键和氢键都是化学键,且都具有饱和性和方向性 |
| D.通过X射线衍射实验难以区分玻璃和水晶 |
您最近半年使用:0次
2024-04-03更新
|
595次组卷
|
4卷引用:辽宁省沈阳市东北育才学校高中部2023-2024学年高二下学期第1次月考化学试题
名校
8 . 元素Y最高价氧化物的水化物是强酸,Y的气态氢化物(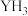 )在水中可形成氢键,其氢键最可能的形式为
)在水中可形成氢键,其氢键最可能的形式为
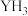 )在水中可形成氢键,其氢键最可能的形式为
)在水中可形成氢键,其氢键最可能的形式为A. | B. |
C.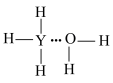 | D.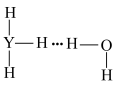 |
您最近半年使用:0次
2024-04-01更新
|
200次组卷
|
2卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高二上学期期末化学试题
解题方法
9 . 中国科学院上海有机化学研究所人工合成了青蒿素,其部分合成路线如图所示:

| A.“乙→丙”发生了消去反应 | B.香茅醛不存在顺反异构现象 |
| C.甲遇浓溴水产生白色沉淀 | D.香茅醛可形成分子内氢键 |
您最近半年使用:0次
10 . X、Y、Z、W为短周期原子序数依次增大的四种主族元素,它们的原子半径与原子序数的关系如图所示(横坐标长度不代表具体数据),W单质遇冷水即可剧烈反应。下列说法不正确的是
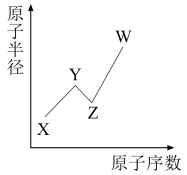

| A.若X、Y、Z均可形成简单阴离子,则离子半径:Y>Z>X |
| B.若Y与W可形成常见的供氧剂,则X与Z形成的化合物水溶液显酸性 |
| C.若Y是形成化合物种类最多的元素,则最简单氢化物的沸点:Y<Z |
| D.若Y和Z是空气中质量分数最大的两种元素,则X、Y、Z只能形成共价化合物 |
您最近半年使用:0次



