名校
1 . 元素Y最高价氧化物的水化物是强酸,Y的气态氢化物(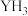 )在水中可形成氢键,其氢键最可能的形式为
)在水中可形成氢键,其氢键最可能的形式为
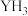 )在水中可形成氢键,其氢键最可能的形式为
)在水中可形成氢键,其氢键最可能的形式为A. | B. |
C.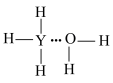 | D.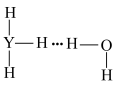 |
您最近半年使用:0次
2024-04-01更新
|
204次组卷
|
2卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高二上学期期末化学试题
名校
2 . 三氯乙酸的结构简式为 ,是有机合成的一种重要中间体。下列有关三氯乙酸的说法正确的是
,是有机合成的一种重要中间体。下列有关三氯乙酸的说法正确的是
 ,是有机合成的一种重要中间体。下列有关三氯乙酸的说法正确的是
,是有机合成的一种重要中间体。下列有关三氯乙酸的说法正确的是| A.难溶于水 | B.所含元素非金属性:Cl>O>C>H |
| C.分子中含有2个π键 | D.分子中碳原子的杂化方式有两种 |
您最近半年使用:0次
名校
3 . 下列有关分子的结构和性质的说法正确的是
A. 和 和 均为直线形的非极性分子 均为直线形的非极性分子 |
B. 和 和 的空间结构均为平面三角形 的空间结构均为平面三角形 |
C.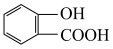 的沸点比 的沸点比 的沸点高 的沸点高 |
D. 和 和 均是极性分子, 均是极性分子, 的键角小于 的键角小于 的 的 |
您最近半年使用:0次
2024-03-02更新
|
310次组卷
|
3卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高二上学期期末化学试题
名校
4 . 正硼酸( )是一种层状结构白色晶体,层内的
)是一种层状结构白色晶体,层内的 分子通过氢键相连(如图)。下列有关说法正确的是
分子通过氢键相连(如图)。下列有关说法正确的是
 )是一种层状结构白色晶体,层内的
)是一种层状结构白色晶体,层内的 分子通过氢键相连(如图)。下列有关说法正确的是
分子通过氢键相连(如图)。下列有关说法正确的是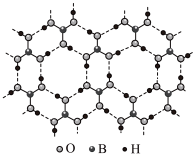
| A.正硼酸晶体属于共价晶体 | B. 分子的稳定性与氢键有关 分子的稳定性与氢键有关 |
C. 分子中B原子采用 分子中B原子采用 杂化 杂化 | D.含1mol 的晶体中有6mol氢键 的晶体中有6mol氢键 |
您最近半年使用:0次
2024-03-02更新
|
301次组卷
|
4卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高二上学期期末化学试题
名校
5 . 已知S4O 的结构为
的结构为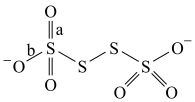 ,下列叙述不正确的是
,下列叙述不正确的是
 的结构为
的结构为 ,下列叙述不正确的是
,下列叙述不正确的是| A.基态S原子核外电子的空间运动状态有9种 |
B.S4O 的结构中,中间的两个S原子均有两对孤对电子 的结构中,中间的两个S原子均有两对孤对电子 |
C.S4O 的结构中a、b为键长,则a<b 的结构中a、b为键长,则a<b |
D.沸点: > > |
您最近半年使用:0次
6 . 下列类比推理结论中正确的是
A. 通入 通入 溶液中无沉淀生成;推出 溶液中无沉淀生成;推出 通入 通入 溶液中无沉淀生成 溶液中无沉淀生成 |
B. 可以改写为 可以改写为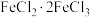 ;推出 ;推出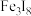 可以改写为 可以改写为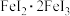 |
C. 的沸点高于 的沸点高于 ;推出 ;推出 沸点高于 沸点高于 |
D.S与Fe反应生成 ;推测S与Cu反应生成 ;推测S与Cu反应生成 |
您最近半年使用:0次
名校
7 . 联氨(N2H4)可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀。其中一种反应机理如图所示。下列叙述正确的是


| A.N2H4分子中σ键与π键的数目之比为5:1 |
| B.1molN2H4可处理水中2molO2 |
| C.O2和O3都是非极性共价键形成的非极性分子 |
| D.氨水中NH3与H2O间存在氢键 |
您最近半年使用:0次
2024-01-22更新
|
124次组卷
|
2卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高二上学期12月月考化学试题
名校
8 . Ⅰ.硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为______ ,基态S原子电子占据最高能级的电子云轮廓图为______ 形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同其他分子的是______ 。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为______ 。
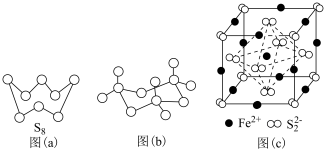
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为______ 形,其中共价键的类型有______ 种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为______
Ⅱ.
(5)气态氢化物热稳定性HF大于HCl的主要原因是______ 。
(6)CaCN2是离子化合物。各原子均满足8电子稳定结构,CaCN2的电子式是______ 。
(7)常温下,在水中的溶解度乙醇大于氯乙烷,原因是______ 。
Ⅲ.
(8)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4.常温常压下SnCl4为无色液体,SnCl4空间构型为______ 。
(9)NH3、PH3、AsH3的沸点由高到低的顺序为______ (填化学式。下同)。还原性由强到弱的顺序为______ 。键角由大到小的顺序为______ 。
| H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同其他分子的是
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为
Ⅱ.
(5)气态氢化物热稳定性HF大于HCl的主要原因是
(6)CaCN2是离子化合物。各原子均满足8电子稳定结构,CaCN2的电子式是
(7)常温下,在水中的溶解度乙醇大于氯乙烷,原因是
Ⅲ.
(8)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4.常温常压下SnCl4为无色液体,SnCl4空间构型为
(9)NH3、PH3、AsH3的沸点由高到低的顺序为
您最近半年使用:0次
2024-01-15更新
|
147次组卷
|
2卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高二上学期12月月考化学试题
解题方法
9 . 下列说法正确的是
| A.由非金属元素组成的化合物一定是共价化合物 |
| B.某化合物在熔融态时能导电,则该化合物一定是离子化合物 |
| C.离子化合物中可能含有共价键,共价化合物中也可能含有离子键 |
| D.一般来说,对于组成和结构相似的分子,相对分子质量越大,分子间作用力越大,熔沸点越高,所以HF、HCl、HBr、HI的沸点依次升高 |
您最近半年使用:0次
2024-01-14更新
|
236次组卷
|
2卷引用:辽宁省部分高中2023-2024学年高一上学期期末考试高化学试题
名校
10 . 下列说法中错误的是
A.根据水的沸点高于氟化氢,推断分子间氢键数目: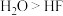 |
B.根据推电子基团种类不同,推断酸性: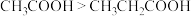 |
C.根据核外电子数不同,推断核外电子空间运动状态种类: |
D.根据中心原子电负性不同,推断键角: |
您最近半年使用:0次
2024-01-13更新
|
1042次组卷
|
6卷引用:辽宁省沈阳市部分高中2023-2024学年高三上学期教学质量监测(一)化学试题



