1 .  具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用是科学研究的重要课题。
的合成及应用是科学研究的重要课题。
(1)以 、
、 合成
合成 ,Fe是常用的催化剂。
,Fe是常用的催化剂。
① 分子空间构型为
分子空间构型为________ ,写出 极易溶于水的原因
极易溶于水的原因________ 。
②实际生产中采用铁的氧化物 、FeO,使用前用
、FeO,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:

ⅰ.两种晶胞所含铁原子个数比为________ 。
ⅱ.图1晶胞的棱长为apm( ),则其密度
),则其密度
________  (写出化简的表达式)。
(写出化简的表达式)。
③我国科学家开发出Fe-LiH双中心催化剂,在合成 中显示出高催化活性。第一电离能
中显示出高催化活性。第一电离能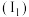 :
: ,从原子结构角度解释原因
,从原子结构角度解释原因________ 。
(2) 、
、 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
① 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为________ 。
② 存在配位键,提供空轨道的是
存在配位键,提供空轨道的是________ 。其他含氮配合物,如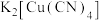 的配离子是
的配离子是________ 、配合物 的配体是
的配体是________ ,配位数为________ 。
(3)常温下 是橙黄色液体,其分子结构如图所示。
是橙黄色液体,其分子结构如图所示。
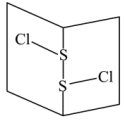
少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。
 分子中含有
分子中含有________ 键(填“极性”、“非极性”,下同),是________ 分子。
(4)已知N、P、As为同一主族元素,则写出三种元素最简单氢化物沸点由高到低的顺序为(用化学式表示)________ 。
 具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用是科学研究的重要课题。
的合成及应用是科学研究的重要课题。(1)以
 、
、 合成
合成 ,Fe是常用的催化剂。
,Fe是常用的催化剂。①
 分子空间构型为
分子空间构型为 极易溶于水的原因
极易溶于水的原因②实际生产中采用铁的氧化物
 、FeO,使用前用
、FeO,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
ⅰ.两种晶胞所含铁原子个数比为
ⅱ.图1晶胞的棱长为apm(
 ),则其密度
),则其密度
 (写出化简的表达式)。
(写出化简的表达式)。③我国科学家开发出Fe-LiH双中心催化剂,在合成
 中显示出高催化活性。第一电离能
中显示出高催化活性。第一电离能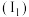 :
: ,从原子结构角度解释原因
,从原子结构角度解释原因(2)
 、
、 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。①
 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为②
 存在配位键,提供空轨道的是
存在配位键,提供空轨道的是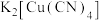 的配离子是
的配离子是 的配体是
的配体是(3)常温下
 是橙黄色液体,其分子结构如图所示。
是橙黄色液体,其分子结构如图所示。
少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。
 分子中含有
分子中含有(4)已知N、P、As为同一主族元素,则写出三种元素最简单氢化物沸点由高到低的顺序为(用化学式表示)
您最近半年使用:0次
解题方法
2 . 下列关于范德华力与氢键的叙述中正确的是
| A.范德华力比氢键的作用还要弱 |
| B.物质的物理性质只与范德华力有关 |
| C.范德华力与氢键的强弱都只与相对分子质量有关 |
| D.任何物质中都存在范德华力,而氢键只存在于含有N、O、F的物质中 |
您最近半年使用:0次
名校
解题方法
3 . 磷酸亚铁锂(LiFePO4)和锰酸锂(LiMn2O4)均可用作锂离子电池正极材料。回答下列问题:
(1)在周期表中,与 化学性质最相似的邻族元素是
化学性质最相似的邻族元素是___________ ,基态P原子电子占据最高能级的电子云轮廓图为___________ 形。
(2)原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数。基态
表示,称为电子的自旋磁量子数。基态 原子的价电子自旋磁量子数的代数和为
原子的价电子自旋磁量子数的代数和为___________ 。
(3) 的空间结构为
的空间结构为___________ 形,其中心原子的杂化轨道类型为___________ 。
(4) 和
和 相比,
相比,___________ 更易液化,原因是___________ 。
(1)在周期表中,与
 化学性质最相似的邻族元素是
化学性质最相似的邻族元素是(2)原子核外电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数。基态
表示,称为电子的自旋磁量子数。基态 原子的价电子自旋磁量子数的代数和为
原子的价电子自旋磁量子数的代数和为(3)
 的空间结构为
的空间结构为(4)
 和
和 相比,
相比,
您最近半年使用:0次
4 . 完成下列填空
(1)某元素基态原子电子排布式为[Ar]3d104s24p1,该元素处于周期表第___________ 周期,第___________ 族,位于___________ 区。
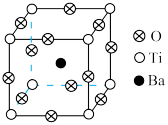
(2)钛酸钡是一种典型钙钛矿型结构晶体,其晶胞如图,写出其化学式:___________ 。
(3)图表法、图像法是常用的科学研究方法。短周期某主族元素M的电离能情况如图A所示。则M元素位于周期表的第___________ 族。图B是研究部分主族元素的氢化物的沸点变化规律的图像,折线c可以表达出第___________ 族元素氢化物的沸点的变化规律。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线,折线a和折线b,你认为正确的是___________ (填“a”或“b”),理由是___________ 。

(1)某元素基态原子电子排布式为[Ar]3d104s24p1,该元素处于周期表第
(2)钛酸钡是一种典型钙钛矿型结构晶体,其晶胞如图,写出其化学式:

(3)图表法、图像法是常用的科学研究方法。短周期某主族元素M的电离能情况如图A所示。则M元素位于周期表的第

您最近半年使用:0次
名校
5 . 下列说法正确的是
| A.分子晶体中分子间作用力越大,该物质越稳定 |
| B.平面三角形分子一定是非极性分子 |
| C.24Mg32S晶体中电子总数与中子总数之比为1:1 |
| D.H2S和SiF4分子中各原子最外层都满足8电子结构 |
您最近半年使用:0次
2024-01-08更新
|
62次组卷
|
2卷引用:辽宁省铁岭市某校2023-2024学年高二上学期第二次阶段考试化学试题
名校
解题方法
6 . 关于 、
、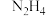 和
和 的结构与性质,下列说法
的结构与性质,下列说法不正确 的是
 、
、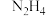 和
和 的结构与性质,下列说法
的结构与性质,下列说法A. 为极性分子 为极性分子 |
B. 空间结构为平面形 空间结构为平面形 |
C. 的沸点高于 的沸点高于 的原因是 的原因是 分子间氢键数目更多 分子间氢键数目更多 |
D. 和 和 中C、O、N杂化方式均相同 中C、O、N杂化方式均相同 |
您最近半年使用:0次
2023-11-23更新
|
178次组卷
|
2卷引用:辽宁省昌图县第一高级中学2023-2024学年高二上学期12月月考化学试卷
7 . 短周期主族元素X、Y、Z、W的原子序数依次增大。元素X在常见化合物中均显负价,X、Y的最外层电子数之和与W的最外层电子数相等,Z的单质能与Y的最高价氧化物对应的水化物反应且有氢气生成。下列说法一定正确的是
A.电负性大小顺序: |
| B.Z最高价氧化物对应水化物是两性氢氧化物 |
| C.X最简单氢化物沸点高于W最简单氢化物沸点 |
D. 和 和 均具有漂白性,但漂白原理不同 均具有漂白性,但漂白原理不同 |
您最近半年使用:0次
名校
8 . 短周期元素W、X、Y和Z的原子序数依次增大。W是宇宙中最丰富的元素,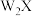 是维持生命过程的必需物质,
是维持生命过程的必需物质,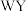 可用于玻璃的刻蚀,
可用于玻璃的刻蚀, 是酸雨的主要形成原因之一,室温下化合物
是酸雨的主要形成原因之一,室温下化合物 是气体。下列说法错误的是
是气体。下列说法错误的是
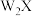 是维持生命过程的必需物质,
是维持生命过程的必需物质,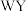 可用于玻璃的刻蚀,
可用于玻璃的刻蚀, 是酸雨的主要形成原因之一,室温下化合物
是酸雨的主要形成原因之一,室温下化合物 是气体。下列说法错误的是
是气体。下列说法错误的是| A.Y的第一电离能在四种元素中最大 | B.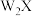 和 和 的中心原子分别为 的中心原子分别为 和 和 杂化 杂化 |
C.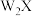 的沸点高于 的沸点高于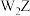 的沸点 的沸点 | D. 分子中原子均为8电子结构 分子中原子均为8电子结构 |
您最近半年使用:0次
2021-01-25更新
|
2173次组卷
|
16卷引用:辽宁省调兵山市第二高级中学2021届高三下学期第一次模拟考试化学试题
辽宁省调兵山市第二高级中学2021届高三下学期第一次模拟考试化学试题湖北省2021年普通高中学业水平选择考适应性测试化学试题江苏省苏州市苏州高新区第一中学2020-2021学年高二下学期期初考试化学试题(已下线)押山东卷第03题 元素周期律、元素周期表-备战2021年高考化学临考题号押题(山东卷)河北省石家庄市第二十四中学2020-2021学年高二第二学期期中考试化学试题江苏省南京师范大学附属中学2021届高三5月模拟考试化学试题广东省东莞市光明中学2021-2022学年高二上学期第一次月考化学试题(已下线)第二单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)(已下线)专题09 物质结构 元素周期律-2022年高考化学二轮复习重点专题常考点突破练河北省武安市第一中学2021-2022学年高三上学期第二次调研考试化学试题第二章 本章达标检测2黑龙江省双鸭山市饶河县高级中学2021-2022学年高二下学期期中考试化学试题四川省内江市第六中学2022-2023学年高二上学期期中考试化学试题湖南省长沙市第一中学2022-2023学年高二下学期第一次月考化学试题(已下线)题型10 物质结构与性质的综合分析与推断-高考必备50个题型广东省惠州市丰湖高级中学2022-2023学年高二下学期第一次段考化学试题



