解题方法
1 . 下列关于氢键X-H…Y的说法中,错误的是
| A.氢键是共价键的一种 |
| B.X、Y元素具有跟大的电负性,是氢键形成的基本条件 |
| C.同一分子内不可能形成氢键 |
| D.氢键能增大很多物质分子之间的作用力,导致沸点升高 |
您最近一年使用:0次
2022-04-24更新
|
289次组卷
|
6卷引用:浙江省诸暨市海亮高级中学2021-2022学年高二上学期期中考试化学试题
浙江省诸暨市海亮高级中学2021-2022学年高二上学期期中考试化学试题人教2019选择性必修2第二章第三节 分子结构与物质的性质课后习题海南省儋州川绵中学2021-2022学年高二下学期期中考试化学试题新疆疏勒县实验学校2021-2022学年高二下学期期中考试化学试题(已下线)2.3.2 分子间作用力 分子的手性-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)海南省儋州川绵中学2021-2022学年高二下学期第二次月考化学试题
名校
2 . 下列叙述中正确的是
| A.冰融化时水分子中共价键发生断裂 |
| B.H2O2、PCl5都是含有极性键的非极性分子 |
| C.HF、HCl、HBr、HI的酸性依次增强 |
| D.对羟基苯甲醛沸点比邻羟基苯甲醛高,是由于前者分子内形成了氢键 |
您最近一年使用:0次
2021-12-02更新
|
529次组卷
|
4卷引用:浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(实验班)化学试题
浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(实验班)化学试题四川省成都市龙泉驿区教育科学研究院2021-2022学年高二下学期期中考试化学试卷(已下线)2.3.2 分子间作用力 分子的手性-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)(已下线)第二章 分子结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)
名校
解题方法
3 . 根据元素性质递变规律,下列判断不正确的是
| A.酸性:H2SiO3<H3PO4<H2SO4 | B.电负性:F>Cl>Br>I |
| C.第一电离能:Na<Mg<Al | D.沸点:NH3>AsH3>PH3 |
您最近一年使用:0次
2021-12-02更新
|
288次组卷
|
2卷引用:浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(实验班)化学试题
名校
4 . 回答下列问题:
(1)NaClO溶液呈碱性,用离子方程式表示其原因___________ 。
(2)5.2g乙炔(C2H2)气体完全燃烧生成二氧化碳和液态水,放出259.9kJ的热量,写出反应的热化学方程式___________ 。
(3)H2O比H2S 的熔沸点高,原因是:___________ 。
(4)25℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,若溶液中c(NH )= c(Cl-),则氨水的电离平衡常数
)= c(Cl-),则氨水的电离平衡常数___________ 。
(5)在25℃时,醋酸和亚硫酸的电离常数如下表:
醋酸滴入Na2SO3溶液中,反应的离子方程式为________
(1)NaClO溶液呈碱性,用离子方程式表示其原因
(2)5.2g乙炔(C2H2)气体完全燃烧生成二氧化碳和液态水,放出259.9kJ的热量,写出反应的热化学方程式
(3)H2O比H2S 的熔沸点高,原因是:
(4)25℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,若溶液中c(NH
 )= c(Cl-),则氨水的电离平衡常数
)= c(Cl-),则氨水的电离平衡常数(5)在25℃时,醋酸和亚硫酸的电离常数如下表:
| 醋酸 | 亚硫酸 |
| K=1.8×10-5 | K1=1.54×10-2 K2=1.02×10-7 |
您最近一年使用:0次
2021-11-20更新
|
158次组卷
|
2卷引用:浙江省衢温市“5+1”联盟2021-2022学年高二上学期期中联考化学试题
5 . 回答下列问题:
(1)已知3种物质的沸点数据如下表:
乙醇沸点比相对分子质量相同的二甲醚、相对分子质量是其三倍多的四氯化碳还要高的原因是_______ 。
(2)金属钠和金属锌分别和硫酸铜溶液作用,前者不能置换出铜,后者能,试解释原因_______ 。
(1)已知3种物质的沸点数据如下表:
| 物质 | 乙醇 | 二甲醚 | 四氯化碳 |
| 相对分子质量 | 46 | 46 | 154 |
| 沸点/℃ | 78 | -23 | 76.5 |
(2)金属钠和金属锌分别和硫酸铜溶液作用,前者不能置换出铜,后者能,试解释原因
您最近一年使用:0次
名校
解题方法
6 . 下列现象与氢键有关的是:
①NH3的熔、沸点比VA族其他元素氢化物的高 ②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小 ④HF、NH3都极易溶于水。
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低 ⑥水分子高温下也很稳定
①NH3的熔、沸点比VA族其他元素氢化物的高 ②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小 ④HF、NH3都极易溶于水。
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低 ⑥水分子高温下也很稳定
| A.①②③④⑤⑥ | B.①②③④⑤ | C.①②③④ | D.①②③ |
您最近一年使用:0次
2021-10-22更新
|
698次组卷
|
5卷引用:浙江省宁波市北仑中学2021-2022学年高二上学期期中考试化学(育英班)试题
浙江省宁波市北仑中学2021-2022学年高二上学期期中考试化学(育英班)试题四川省峨眉第二中学校2021-2022学年高二上学期10月月考化学试题(已下线)2.3.2 分子间作用力 分子的手性-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)河南省新乡市河南师范大学附属中学2021-2022学年高二下学期3月月考化学试题四川省峨眉二中2022-2023学年高二上学期10月月考化学试题
解题方法
7 . (1)乙醇和二甲醚互为同分异构体,乙醇的沸点(78.5℃)远高于二甲醚的沸点(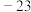 ℃),原因是
℃),原因是_______ 。
(2) 是离子化合物,各原子均满足8电子稳定结构。写出
是离子化合物,各原子均满足8电子稳定结构。写出 的电子式
的电子式_______ 。
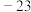 ℃),原因是
℃),原因是(2)
 是离子化合物,各原子均满足8电子稳定结构。写出
是离子化合物,各原子均满足8电子稳定结构。写出 的电子式
的电子式
您最近一年使用:0次
名校
8 . (1)比较结合H+的能力的相对强弱:C6H5O-___________ CO (填“>”、“<”或“=”);用一个离子方程式说明 C6H5OH和 H2CO3给出 H+能力的相对强弱
(填“>”、“<”或“=”);用一个离子方程式说明 C6H5OH和 H2CO3给出 H+能力的相对强弱___________ 。
(2)(CN)2 的性质与氯气相似,又称拟卤素,各原子均满足 8 电子稳定结构。写出 (CN)2 的电子式________ 。
(3)常压下,水的沸点比氟化氢高,其主要原因是___________ 。
 (填“>”、“<”或“=”);用一个离子方程式说明 C6H5OH和 H2CO3给出 H+能力的相对强弱
(填“>”、“<”或“=”);用一个离子方程式说明 C6H5OH和 H2CO3给出 H+能力的相对强弱(2)(CN)2 的性质与氯气相似,又称拟卤素,各原子均满足 8 电子稳定结构。写出 (CN)2 的电子式
(3)常压下,水的沸点比氟化氢高,其主要原因是
您最近一年使用:0次
9 . 氨基氰(CH2N2)中C、N原子均满足8电子稳定结构,福州大学王新晨教授以其为原料制得类石墨相氮化碳(g-C3N4),其单层结构如图所示。下列说法错误的是


A.氨基氰的结构式: |
| B.氮化碳的单层结构中,所有原子可能共平面 |
| C.氨基氰易溶于水,氮化碳能导电 |
| D.氨基氰和氮化碳中,N原子杂化方式均为sp2和sp3 |
您最近一年使用:0次
2021-01-06更新
|
370次组卷
|
7卷引用:浙江省诸暨市海亮高级中学2021-2022学年高二上学期期中考试化学试题
浙江省诸暨市海亮高级中学2021-2022学年高二上学期期中考试化学试题福建泉州实验中学、养正中学2020-2021学年高二下学期期中联考化学试题山东省寿光现代中学2021届高三上学期1月月考化学试题(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)2021年高考化学押题预测卷(辽宁卷)(03)(已下线)第五章 物质结构与性质元素周期律 第29练 化学键 分子的空间结构福建省建瓯市芝华中学2022-2023学年高二下学期第一次月考化学试题
名校
10 . “类推”是一种重要的学习方法,但有时会产生错误,下列类推得到的结论正确的是( )
| A.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
| B.氢化物沸点顺序是:GeH4>SH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
| C.根据对角线规则,元素Li和Mg的某些性质相似,则元素C和P的某些性质也相似 |
| D.SO42﹣和P4都为正四面体形,SO42﹣中键角为109°28′,P4中键角也为109°28′ |
您最近一年使用:0次
2019-10-18更新
|
1553次组卷
|
8卷引用:浙江省诸暨市海亮高级中学2021-2022学年高二上学期期中考试化学试题



