1 . 铜及其化合物在生产生活中有着广泛的应用。请回答:
(1)①基态铜原子价层电子排布图为_______ ;
②已知Cu第一电离能 ,Fe第一电离能
,Fe第一电离能 ,则
,则
_______  (填“>”、“=”或“<”),其主要原因是
(填“>”、“=”或“<”),其主要原因是_______ 。
(2)在碱性条件下 与双缩脲
与双缩脲 生成紫色的配位化合物,该原理可用于检验蛋白质。该配位化合物的阴离子结构如图所示:
生成紫色的配位化合物,该原理可用于检验蛋白质。该配位化合物的阴离子结构如图所示:

①该阴离子中所有非金属元素的电负性从大到小的顺序为_______ ;
②该阴离子中N原子的杂化方式为_______ ;
③1mol该阴离子含有 键的数目为
键的数目为_______ 。
(3)磁性形状记忆材料 合金的晶胞如图a所示(Mn、Al位于Cu形成的立方体体心位置),图b是沿立方格子对角面取得的截图,Cu在沿立方格子对角面取得截图中的相对位置如图c所示。
合金的晶胞如图a所示(Mn、Al位于Cu形成的立方体体心位置),图b是沿立方格子对角面取得的截图,Cu在沿立方格子对角面取得截图中的相对位置如图c所示。


①该合金的化学式为_______ ;
②在图c中画出Al和Mn的相对位置(分别用 表示,不考虑各原子的大小)
表示,不考虑各原子的大小) _______ 。
(1)①基态铜原子价层电子排布图为
②已知Cu第一电离能
 ,Fe第一电离能
,Fe第一电离能 ,则
,则
 (填“>”、“=”或“<”),其主要原因是
(填“>”、“=”或“<”),其主要原因是(2)在碱性条件下
 与双缩脲
与双缩脲 生成紫色的配位化合物,该原理可用于检验蛋白质。该配位化合物的阴离子结构如图所示:
生成紫色的配位化合物,该原理可用于检验蛋白质。该配位化合物的阴离子结构如图所示:
①该阴离子中所有非金属元素的电负性从大到小的顺序为
②该阴离子中N原子的杂化方式为
③1mol该阴离子含有
 键的数目为
键的数目为(3)磁性形状记忆材料
 合金的晶胞如图a所示(Mn、Al位于Cu形成的立方体体心位置),图b是沿立方格子对角面取得的截图,Cu在沿立方格子对角面取得截图中的相对位置如图c所示。
合金的晶胞如图a所示(Mn、Al位于Cu形成的立方体体心位置),图b是沿立方格子对角面取得的截图,Cu在沿立方格子对角面取得截图中的相对位置如图c所示。

①该合金的化学式为
②在图c中画出Al和Mn的相对位置(分别用
 表示,不考虑各原子的大小)
表示,不考虑各原子的大小)
您最近一年使用:0次
2 . 下列说法不正确 的是
A.氧原子可以形成 、 、 ,也可能形成 ,也可能形成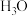 |
B.氯化铯晶体中,每个 周围紧邻且距离相等的 周围紧邻且距离相等的 共有6个 共有6个 |
C.同一原子中, 、 、 、 、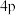 能级的轨道数目相等 能级的轨道数目相等 |
| D.缺角的氯化钠晶体在饱和氯化钠溶液中慢慢变为完美的立方体块 |
您最近一年使用:0次
名校
解题方法
3 . 2022年9月9日,国家航天局、国家原子能机构联合在北京发布嫦娥五号最新科学成果,中核集团核工业北京地质研究院科研团队首次在月球上发现的新矿物,被命名为“嫦娥石”,我国成为世界上第三个在月球发现新矿物的国家。
回答下列问题:
(1)中核集团核工业北京地质研究院科研团队,通过晶体___________ 实验等一系列高新技术手段,成功解译其晶体结构。
(2)嫦娥石是一种陨磷钠镁钙石类矿物,基态P、Na、Mg、Ca四种元素的原子第一电离能由大到小的顺序为___________ 。
(3)从晶体结构上看,嫦娥石可以分为两大部分,其中阴离子结构单元为[Fe(PO4)6]16-,请写出Fe2+的基态价层电子排布式___________ ,PO 的VSEPR模型名称为
的VSEPR模型名称为___________ 。
(4)从结构角度分析Fe3+比Fe2+稳定的原因___________ 。
(5)嫦娥石的一种伴生矿物为方石英,方石英结构和金刚石相似,其晶胞结构如图所示,Si-O键长为anm,∠AED=109°28′,已知阿伏伽德罗常数为NA,则方石英晶体的的密度为___________ g·cm-3(列出计算式即可)。

回答下列问题:
(1)中核集团核工业北京地质研究院科研团队,通过晶体
(2)嫦娥石是一种陨磷钠镁钙石类矿物,基态P、Na、Mg、Ca四种元素的原子第一电离能由大到小的顺序为
(3)从晶体结构上看,嫦娥石可以分为两大部分,其中阴离子结构单元为[Fe(PO4)6]16-,请写出Fe2+的基态价层电子排布式
 的VSEPR模型名称为
的VSEPR模型名称为(4)从结构角度分析Fe3+比Fe2+稳定的原因
(5)嫦娥石的一种伴生矿物为方石英,方石英结构和金刚石相似,其晶胞结构如图所示,Si-O键长为anm,∠AED=109°28′,已知阿伏伽德罗常数为NA,则方石英晶体的的密度为

您最近一年使用:0次
2023-08-12更新
|
399次组卷
|
2卷引用:浙江省金丽衢十二校2022-2023学年高三上学期第一次联考化学试题
4 . 铅磷青铜具有很高的耐腐蚀性和耐磨性,常用于制作耐磨零件和滑动轴承。如图为铅磷青铜的一种晶胞结构,已知A点原子的分数坐标为(0,0,0),B点原子的分数坐标为(1,1,0);下列说法不正确的是
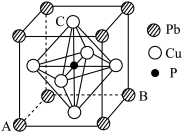
| A.该晶胞的化学式为PbCu3P |
| B.C点原子的分数坐标为(0.5,0.5,1) |
| C.晶胞中,Pb位于第六周期第ⅣA族,Cu属于第ⅠB位于d区 |
| D.晶体中基态磷原子的核外电子共有9种空间运动状态 |
您最近一年使用:0次
2023-08-12更新
|
415次组卷
|
3卷引用:浙江省金丽衢十二校2022-2023学年高三上学期第一次联考化学试题
解题方法
5 . 氧族元素包括氧、硫、硒等,这些元素的单质及其化合物在工农业生产和科学研究中具有广泛的用途。回答下列问题:
(1)下列属于氧原子激发态的轨道表示式的有___________ (填字母,下同),其中失去最外层上一个电子所需能量最低的是___________ 。
a. b.
b.
c.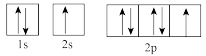 d.
d.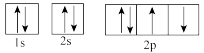
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
① 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的___________ 杂化轨道形成S—S___________ (填“ ”或“
”或“ ”)共价键。
”)共价键。
② 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角___________ (填“=”“>”或“<”) 。
。
③ 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是___________ 。
(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:
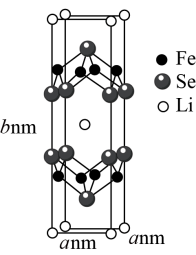
1个晶胞中的Se原子数为___________ 。晶胞的部分参数如图所示,且晶胞棱边夹角均为90°,晶体密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为___________ (列式表示)。
(1)下列属于氧原子激发态的轨道表示式的有
a.
 b.
b.
c.
 d.
d.
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
| 物质 | 熔点/℃ | 沸点/℃ |  制备方法 制备方法 |
 | -90.0 | 71.0 | 加热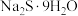 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 |
 | -0.4 | 150.0 |
 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的 ”或“
”或“ ”)共价键。
”)共价键。②
 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角 。
。③
 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:

1个晶胞中的Se原子数为
 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
解题方法
6 . 过渡金属元素铬 是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。三价铬离子的一种配离子结构如图所示,回答下列问题:
是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。三价铬离子的一种配离子结构如图所示,回答下列问题:
(1)下列说法不正确的是
① 在元素周期表中位于
在元素周期表中位于_____________ ;属于硫原子激发态的简化电子排布式且能量较低的是_____________ 。(填标号)
A.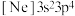 B.
B. C.
C. D.
D.

②配体 中
中 原子的价层孤电子对占据中心三价铬离子的
原子的价层孤电子对占据中心三价铬离子的___________ 杂化轨道。(填标号)
A. B.
B. C.
C. D.
D.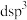 E.
E. F.
F.
③该配离子中所含的 键和
键和 键的个数比为
键的个数比为_____________ ;配体中 三种非金属元素的电负性由大到小的顺序是
三种非金属元素的电负性由大到小的顺序是_____________ 。
(2)两种有机物的相关数据如下表:
常温下,邻羟基苯甲酸的水溶解性比对羟基苯甲酸小,而邻羟基苯甲酸的酸性比对羟基苯甲酸强,原因是_________ 。
(3)利用皮秒激光照射悬浮在中醇溶液中的多臂碳纳米管可以合成 碳,
碳, 碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成)取代,如图所示,已知
碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成)取代,如图所示,已知 碳晶胞参数为
碳晶胞参数为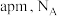 为阿伏加德罗常数。
为阿伏加德罗常数。 碳晶体的摩尔体积
碳晶体的摩尔体积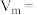
_____________  (列出算式)。
(列出算式)。

 是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。三价铬离子的一种配离子结构如图所示,回答下列问题:
是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。三价铬离子的一种配离子结构如图所示,回答下列问题:(1)下列说法不正确的是
①
 在元素周期表中位于
在元素周期表中位于A.
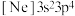 B.
B. C.
C. D.
D.

②配体
 中
中 原子的价层孤电子对占据中心三价铬离子的
原子的价层孤电子对占据中心三价铬离子的A.
 B.
B. C.
C. D.
D.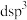 E.
E. F.
F.
③该配离子中所含的
 键和
键和 键的个数比为
键的个数比为 三种非金属元素的电负性由大到小的顺序是
三种非金属元素的电负性由大到小的顺序是(2)两种有机物的相关数据如下表:
| 物质 | 邻羟基苯甲酸 | 对羟基苯甲酸 |
水溶解性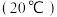 |  |  |
 | 3.91 | 4.48 |
(3)利用皮秒激光照射悬浮在中醇溶液中的多臂碳纳米管可以合成
 碳,
碳, 碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成)取代,如图所示,已知
碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成)取代,如图所示,已知 碳晶胞参数为
碳晶胞参数为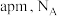 为阿伏加德罗常数。
为阿伏加德罗常数。 碳晶体的摩尔体积
碳晶体的摩尔体积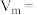
 (列出算式)。
(列出算式)。
您最近一年使用:0次
7 . 下列说法错误 的是
| A.用X射线衍射仪可测定菁蒿素的晶体结构 |
| B.乙醇与氢卤酸的反应中乙醇分子断裂碳氧键而失去羟基 |
| C.苯不能使酸性高锰酸钾溶液褪色,但苯能发生氧化反应 |
| D.煤是复杂的混合物,含有苯、甲苯、二甲苯等一系列重要的化工原料 |
您最近一年使用:0次
8 . 储氢材料的开发为氢气成为广泛使用的能源提供有力保障,镁铁氢化物是一种较稳定的,具有客观储氢量的氢化物。请回答:
(1)基态 原子的核外电子有
原子的核外电子有_______ 种空间运动状态。
(2) 及其同周期相邻元素的逐级电离能如下表所示,元素
及其同周期相邻元素的逐级电离能如下表所示,元素 表示
表示_______ 元素的逐级电离能变化情况。根据表示信息,简述逐级电离能与这三种元素的化合价之间的关系_______ 。
(3)已知镁铁氢化物结构如图所示(氢末示出),晶胞参数为 ,
, 原子间的最近距离为晶胞参数的一半,
原子间的最近距离为晶胞参数的一半, 原子以正八画体的配位模式有序分布在
原子以正八画体的配位模式有序分布在 原子周围。
原子周围。

①请写出该镁铁氢化物的化学式_______ 。
②该镁铁氢化物中氢的密度是标况下的氢气密度的_______ 倍( 为阿伏伽德罗常数的值,列计算式即可)。
为阿伏伽德罗常数的值,列计算式即可)。
(1)基态
 原子的核外电子有
原子的核外电子有(2)
 及其同周期相邻元素的逐级电离能如下表所示,元素
及其同周期相邻元素的逐级电离能如下表所示,元素 表示
表示电离能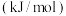 |  |  |  |  | 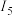 |  |  |
 | 738 | 1451 | 7733 | 10540 | 13630 | 17995 | 21703 |
 | 578 | 1817 | 2745 | 11575 | 14830 | 18376 | 23293 |
 | 496 | 4562 | 6912 | 9543 | 13353 | 16610 | 20114 |
 ,
, 原子间的最近距离为晶胞参数的一半,
原子间的最近距离为晶胞参数的一半, 原子以正八画体的配位模式有序分布在
原子以正八画体的配位模式有序分布在 原子周围。
原子周围。
①请写出该镁铁氢化物的化学式
②该镁铁氢化物中氢的密度是标况下的氢气密度的
 为阿伏伽德罗常数的值,列计算式即可)。
为阿伏伽德罗常数的值,列计算式即可)。
您最近一年使用:0次
名校
解题方法
9 . 纤锌矿型和闪锌矿型结构是典型的离子晶体结构。如图所示,纤锌矿型晶体 采用六方密堆积,
采用六方密堆积, 填充在一部分四面体空隙之中;闪锌矿型晶体
填充在一部分四面体空隙之中;闪锌矿型晶体 呈面心立方堆积,
呈面心立方堆积, 占据半数四面体空隙,其中
占据半数四面体空隙,其中 位置的
位置的 坐标为
坐标为 ,下列叙述不正确的是
,下列叙述不正确的是

 采用六方密堆积,
采用六方密堆积, 填充在一部分四面体空隙之中;闪锌矿型晶体
填充在一部分四面体空隙之中;闪锌矿型晶体 呈面心立方堆积,
呈面心立方堆积, 占据半数四面体空隙,其中
占据半数四面体空隙,其中 位置的
位置的 坐标为
坐标为 ,下列叙述不正确的是
,下列叙述不正确的是
| A.左图所示结构含有三个晶胞单元 |
B.闪锌矿型晶体中,离 最近且等距的 最近且等距的 有8个 有8个 |
C.离 位置 位置 的 的 距离最近的 距离最近的 的坐标参数为 的坐标参数为 |
| D.两种结构对应的物质,化学式相同 |
您最近一年使用:0次
2023-08-08更新
|
505次组卷
|
3卷引用:浙江省金华市十校2022-2023学年高三上学期模拟考试化学试题
10 . 碳及其化合物在生产、生活中有着重要的应用。请回答:
(1) 分子中,C原子的杂化轨道类型为
分子中,C原子的杂化轨道类型为______ ,共价键的类型为______ (填标号)。
A.配位键 B.非极性键 C.离子键 D.极性键
(2)乙烷、乙烯、乙炔中碳碳键键长由长到短的顺序为:______ ;并说明原因:______ 。
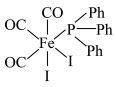
(3)一种羰基配合物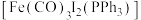 ,Ph表示苯基(
,Ph表示苯基( ),结构如图所示,该配合物巾所有配体原子都满足8电子或2电子稳定结构。基态碘原子的价电子轨道表示式为
),结构如图所示,该配合物巾所有配体原子都满足8电子或2电子稳定结构。基态碘原子的价电子轨道表示式为______ ,配体 的空间构型为
的空间构型为______ ,1 mol 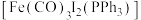 中配位键数目为
中配位键数目为______ 。〔用含 (阿伏加德罗常数的值)来表示〕。
(阿伏加德罗常数的值)来表示〕。
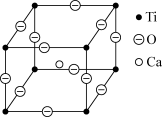
(4)新型碳基复合材料在钙钛矿太阳能电池中具有重要作用,钙钛矿晶胞如图所示,钛离子周围与它最近且相等距离的钛离子有______ 个。氧、钙、钛的微粒个数比是______ 。
(1)
 分子中,C原子的杂化轨道类型为
分子中,C原子的杂化轨道类型为A.配位键 B.非极性键 C.离子键 D.极性键
(2)乙烷、乙烯、乙炔中碳碳键键长由长到短的顺序为:
(3)一种羰基配合物
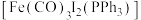 ,Ph表示苯基(
,Ph表示苯基( ),结构如图所示,该配合物巾所有配体原子都满足8电子或2电子稳定结构。基态碘原子的价电子轨道表示式为
),结构如图所示,该配合物巾所有配体原子都满足8电子或2电子稳定结构。基态碘原子的价电子轨道表示式为 的空间构型为
的空间构型为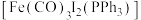 中配位键数目为
中配位键数目为 (阿伏加德罗常数的值)来表示〕。
(阿伏加德罗常数的值)来表示〕。
(4)新型碳基复合材料在钙钛矿太阳能电池中具有重要作用,钙钛矿晶胞如图所示,钛离子周围与它最近且相等距离的钛离子有

您最近一年使用:0次



