13-14高三上·上海·期末
解题方法
1 . 粉煤灰是燃煤电厂的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为38%,还有含量较多的SiO2。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4,有关化学反应方程式如下:Al6Si2O13+3Na2CO3→2NaAlSiO4+4NaAlO2+3CO2↑
结合上述反应完成下列填空:
(1)上述反应所涉及的元素中,原子核外电子运动状态最多的元素在周期表中的位置是___ ,其氧化物属于___ 晶体。
(2)上述元素中有三种元素在元素周期表中处于相邻位置,其原子半径从大到小的顺序为___ >___ >___ (用元素符号表示)。
(3)二氧化碳分子的空间构型为___ 型,碳酸钠溶液显碱性的原因是(用离子方程式表示)___ 。
(4)上述元素中有两种元素是同一主族,可以作为判断两者非金属性强弱的依据的是___ (填编号)。
a.该两种原子形成的共价键中共用电子对的偏向
b.最高价氧化物熔沸点高低
c.最高价氧化物对应水化物的酸性强弱
d.单质与酸反应的难易程度
结合上述反应完成下列填空:
(1)上述反应所涉及的元素中,原子核外电子运动状态最多的元素在周期表中的位置是
(2)上述元素中有三种元素在元素周期表中处于相邻位置,其原子半径从大到小的顺序为
(3)二氧化碳分子的空间构型为
(4)上述元素中有两种元素是同一主族,可以作为判断两者非金属性强弱的依据的是
a.该两种原子形成的共价键中共用电子对的偏向
b.最高价氧化物熔沸点高低
c.最高价氧化物对应水化物的酸性强弱
d.单质与酸反应的难易程度
您最近一年使用:0次
名校
解题方法
2 . 废电池粉[锂、铁、磷、铜、铝和碳(碳粉)的质量分数分别为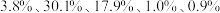 和
和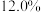 ]回收处理的工艺流程如下:
]回收处理的工艺流程如下: 转化为难溶于水
转化为难溶于水 和可溶于水硫酸锂,写出该反应的化学方程式:
和可溶于水硫酸锂,写出该反应的化学方程式:______________ 。哪些途径可以提高转化的效率(写两条):______________ 。
(2)“净化”步骤可以去除滤液中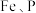 等元素,沉渣1中含
等元素,沉渣1中含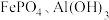 、
、_______ 。沉渣2的主要成分为_______ 。
(3)“电解”可以将溶液中的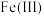 转化为
转化为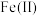 ,溶液中
,溶液中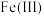 完全转化为
完全转化为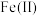 的标志是
的标志是______________ 。甲醇在阳极发生反应生成甲醛,阳极电极反应方程式为_______ 。在电解完成后向溶液中加入 溶液可以将溶液中的
溶液可以将溶液中的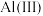 沉淀。
沉淀。
(4)称取一定量的二水磷酸铁,用硝酸溶解后再用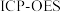 进行分析,得到部分杂质的质量分数
进行分析,得到部分杂质的质量分数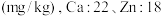 ,评价该制备过程
,评价该制备过程_______ (填“是”或“否”)符合均满足 《电池用磷酸铁》的Ⅱ型标准
《电池用磷酸铁》的Ⅱ型标准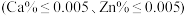 。
。
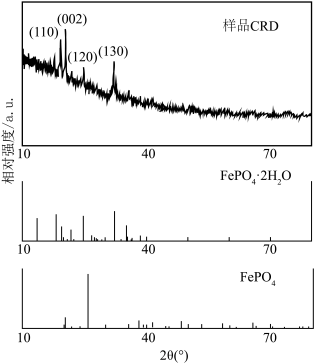
(5) 衍射实验图谱与标准卡片进行对比分析,可判断样品晶体类型。下图分别为样品、
衍射实验图谱与标准卡片进行对比分析,可判断样品晶体类型。下图分别为样品、 和
和 的标准卡片的
的标准卡片的 衍射实验图谱,结合图像内容判断获的样品
衍射实验图谱,结合图像内容判断获的样品_______ (填“是”或“否”) 。
。
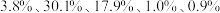 和
和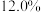 ]回收处理的工艺流程如下:
]回收处理的工艺流程如下: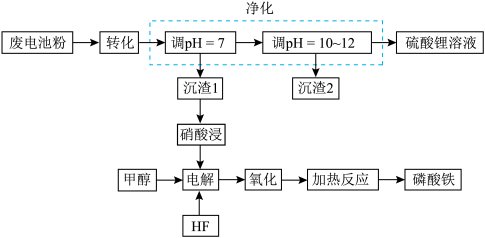
 转化为难溶于水
转化为难溶于水 和可溶于水硫酸锂,写出该反应的化学方程式:
和可溶于水硫酸锂,写出该反应的化学方程式:(2)“净化”步骤可以去除滤液中
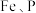 等元素,沉渣1中含
等元素,沉渣1中含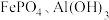 、
、(3)“电解”可以将溶液中的
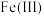 转化为
转化为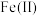 ,溶液中
,溶液中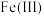 完全转化为
完全转化为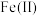 的标志是
的标志是 溶液可以将溶液中的
溶液可以将溶液中的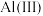 沉淀。
沉淀。(4)称取一定量的二水磷酸铁,用硝酸溶解后再用
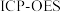 进行分析,得到部分杂质的质量分数
进行分析,得到部分杂质的质量分数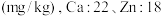 ,评价该制备过程
,评价该制备过程 《电池用磷酸铁》的Ⅱ型标准
《电池用磷酸铁》的Ⅱ型标准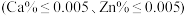 。
。(5)
 衍射实验图谱与标准卡片进行对比分析,可判断样品晶体类型。下图分别为样品、
衍射实验图谱与标准卡片进行对比分析,可判断样品晶体类型。下图分别为样品、 和
和 的标准卡片的
的标准卡片的 衍射实验图谱,结合图像内容判断获的样品
衍射实验图谱,结合图像内容判断获的样品 。
。
您最近一年使用:0次
解题方法
3 . 锡(Sn)是“五金”之一,粗锡电解精炼后的锡阳极泥中金属元素二次回收利用的部分工艺流程如下:
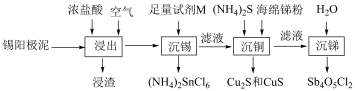
已知:①锡阳极泥中主要成分的质量分数如下表所示
②常温下,锑(Sb)不溶于浓盐酸。
③浸出液中主要存在的阳离子有 和
和 。
。
(1)锡有多种同素异形体,其中灰锡的晶体结构与金刚石类似,灰锡属于___________ 晶体。
(2)锡阳极泥在“浸出”前,进行球磨、筛分有利于___________ 。
(3)“浸出”工序中,吹入适量空气的目的是___________ 。
(4)“沉锡”时需在强酸性环境中进行,最适宜加入的试剂M为___________ 。(填标号)
A. B.
B. C.
C.
(5)“沉铜”工序中,加入海绵锑粉的作用是___________ 。
(6)“沉锑”工序中,生成 的
的离子方程式 为___________ 。
(7)回收得到的 和
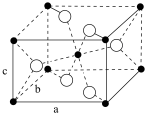
和 可合成纳米锑掺杂二氧化锡(ATO)。二氧化锡的晶胞如图所示,其中位于晶胞体心的原子是
可合成纳米锑掺杂二氧化锡(ATO)。二氧化锡的晶胞如图所示,其中位于晶胞体心的原子是___________ (填元素符号);位于晶胞顶角的原子的配位数是___________ 。

已知:①锡阳极泥中主要成分的质量分数如下表所示
| 成分 | SnO | Cu | Sb |
| 质量分数 | 44.81% | 12.38% | 8.13% |
③浸出液中主要存在的阳离子有
 和
和 。
。(1)锡有多种同素异形体,其中灰锡的晶体结构与金刚石类似,灰锡属于
(2)锡阳极泥在“浸出”前,进行球磨、筛分有利于
(3)“浸出”工序中,吹入适量空气的目的是
(4)“沉锡”时需在强酸性环境中进行,最适宜加入的试剂M为
A.
 B.
B. C.
C.
(5)“沉铜”工序中,加入海绵锑粉的作用是
(6)“沉锑”工序中,生成
 的
的(7)回收得到的
 和
和 可合成纳米锑掺杂二氧化锡(ATO)。二氧化锡的晶胞如图所示,其中位于晶胞体心的原子是
可合成纳米锑掺杂二氧化锡(ATO)。二氧化锡的晶胞如图所示,其中位于晶胞体心的原子是
您最近一年使用:0次
名校
解题方法
4 . 硒被誉为“生命元素”。亚硒酸钙(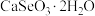 ,难溶于水)常用作饲料添加剂,
,难溶于水)常用作饲料添加剂, 常用作制备含硒营养物质的原料。一种利用含硒废料(主要成分是
常用作制备含硒营养物质的原料。一种利用含硒废料(主要成分是 和
和 )制备亚硒酸钙和二氧化硒的工艺流程如下。
)制备亚硒酸钙和二氧化硒的工艺流程如下。
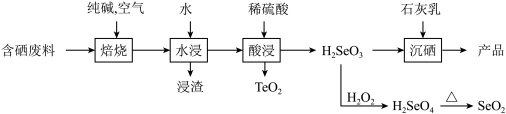
回答下列问题:
(1)“焙烧”常采用逆流操作,即空气从焙烧炉下部通入,废料粉从上部充入,这样操作的目的是_______ ;“焙烧”中固体产物为 和
和 ,“焙烧”时
,“焙烧”时 反应的化学方程式为
反应的化学方程式为_______ 。
(2)水浸时浸渣的主要成分是_______ (填化学式)。
(3)“沉硒”的化学方程式为________ 。
(4)基态 原子核外电子排布式为
原子核外电子排布式为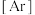
_______ 。
(5)已知 熔点为
熔点为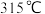 ,
,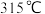 时升华,则
时升华,则 形成的晶体类型为
形成的晶体类型为______ 。
(6)测定 产品纯度。
产品纯度。
称取 产品溶于水,加入足量
产品溶于水,加入足量 溶液和适量稀盐酸,充分反应后,用
溶液和适量稀盐酸,充分反应后,用 标准溶液滴定至终点时消耗
标准溶液滴定至终点时消耗 滴定液。
滴定液。
发生有关反应:① (未配平);
(未配平);
②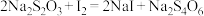 。
。
在下列试剂中,宜选择的指示剂为_____ (填标号)。 产品中
产品中 的质量分数为
的质量分数为______  。
。
A. 溶液 B.
溶液 B. 淀粉溶液
淀粉溶液
C. 酚酞溶液 D.
酚酞溶液 D. 甲基橙溶液
甲基橙溶液
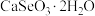 ,难溶于水)常用作饲料添加剂,
,难溶于水)常用作饲料添加剂, 常用作制备含硒营养物质的原料。一种利用含硒废料(主要成分是
常用作制备含硒营养物质的原料。一种利用含硒废料(主要成分是 和
和 )制备亚硒酸钙和二氧化硒的工艺流程如下。
)制备亚硒酸钙和二氧化硒的工艺流程如下。
回答下列问题:
(1)“焙烧”常采用逆流操作,即空气从焙烧炉下部通入,废料粉从上部充入,这样操作的目的是
 和
和 ,“焙烧”时
,“焙烧”时 反应的化学方程式为
反应的化学方程式为(2)水浸时浸渣的主要成分是
(3)“沉硒”的化学方程式为
(4)基态
 原子核外电子排布式为
原子核外电子排布式为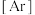
(5)已知
 熔点为
熔点为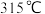 ,
,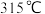 时升华,则
时升华,则 形成的晶体类型为
形成的晶体类型为(6)测定
 产品纯度。
产品纯度。称取
 产品溶于水,加入足量
产品溶于水,加入足量 溶液和适量稀盐酸,充分反应后,用
溶液和适量稀盐酸,充分反应后,用 标准溶液滴定至终点时消耗
标准溶液滴定至终点时消耗 滴定液。
滴定液。发生有关反应:①
 (未配平);
(未配平);②
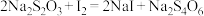 。
。在下列试剂中,宜选择的指示剂为
 产品中
产品中 的质量分数为
的质量分数为 。
。A.
 溶液 B.
溶液 B. 淀粉溶液
淀粉溶液C.
 酚酞溶液 D.
酚酞溶液 D. 甲基橙溶液
甲基橙溶液
您最近一年使用:0次
2024-02-13更新
|
156次组卷
|
2卷引用:河北省沧州市泊头市部分学校2023-2024学年高三上学期12月月考化学试题
名校
解题方法
5 . 碱式碳酸铜[Cu2(OH)2CO3](Mr=222)是一种草绿色晶体,可用于铜盐、油漆和烟花的制备。实验室制备碱式碳酸铜的步骤如下:
I.分别配制0.50mol∙L-1CuSO4溶液和0.50mol∙L-1Na2CO3溶液。
II.将30mLCuSO4溶液和36mL Na2CO3溶液混合、搅拌均匀。
III.将II的混合溶液加热至75℃,搅拌15min。
IV.静置使产物沉淀完全后,抽滤、洗涤、干燥、称重,分析样品组成和晶体结构。
回答下列问题:
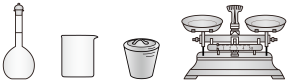
(1)步骤I中,配制0.50mol∙L-1CuSO4溶液时,不需要使用下列仪器中的_______ (填仪器名称)。
(2)步骤II中,若误将CuSO4溶液与Na2CO3溶液等体积混合,二者恰好完全反应,生成蓝色的Cu4(SO4)(OH)6∙2H2O晶体,其反应的离子方程式为_______ 。
(3)步骤III中,若温度高于90℃,产品中混有的黑色固体是_______ 。
(4)步骤IV中,检验沉淀是否洗涤干净的试剂是_______ ;称得产品的质量为1.332g,则该实验所得碱式碳酸铜的产率是_______ 。
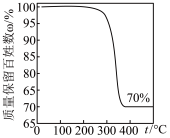
(5)对样品进行热重分析得到的曲线如下图所示,则铜元素的质量分数是_______ ,与理论值相差不大。使用_______ 实验可进一步测定样品的晶体结构。
I.分别配制0.50mol∙L-1CuSO4溶液和0.50mol∙L-1Na2CO3溶液。
II.将30mLCuSO4溶液和36mL Na2CO3溶液混合、搅拌均匀。
III.将II的混合溶液加热至75℃,搅拌15min。
IV.静置使产物沉淀完全后,抽滤、洗涤、干燥、称重,分析样品组成和晶体结构。
回答下列问题:
(1)步骤I中,配制0.50mol∙L-1CuSO4溶液时,不需要使用下列仪器中的

(2)步骤II中,若误将CuSO4溶液与Na2CO3溶液等体积混合,二者恰好完全反应,生成蓝色的Cu4(SO4)(OH)6∙2H2O晶体,其反应的离子方程式为
(3)步骤III中,若温度高于90℃,产品中混有的黑色固体是
(4)步骤IV中,检验沉淀是否洗涤干净的试剂是
(5)对样品进行热重分析得到的曲线如下图所示,则铜元素的质量分数是

您最近一年使用:0次
2022-09-17更新
|
501次组卷
|
3卷引用:湖北省武汉市部分学校2022-2023学年高三上学期9月调研考试化学试题
名校
6 . 2024年央视春晚首次应用5G-A技术,Al含量高,硬科技霸屏,下列有关说法错误的是
| A.舞蹈《瓷影》所诠释的青花瓷,其主要原材料为含水的铝硅酸盐 |
| B.晚会采用的LED屏,其发光材料通常是以Si3N4为基础,用Al取代部分Si,用O取代部分N后所得的陶瓷制作而成 |
| C.5G-A技术所需高频通讯材料之一的LCP(液晶高分子)在一定加热状态下一般会变成液晶,液晶既具有液体的流动性,又表现出类似晶体的各向异性 |
| D.芯片中二氧化硅优异的半导体性能。使得晚会上各种AI技术得以完美体现 |
您最近一年使用:0次
2024-04-13更新
|
394次组卷
|
5卷引用:河北省石家庄市第十七中学2023-2024学年高三下学期第一次月考化学试题
7 . 已知W、X、Y、Z的原子序数依次递增,其元素性质或原子结构特征如下:
下列说法正确的是
| 元素 | 元素性质或原子结构特征 |
| W | 是宇宙中含量最多的元素 |
| X | 元素原子最高能级的不同轨道都有电子,且自旋方向相同 |
| Y | 原子核外s能级上的电子总数与p能级上的电子总数相等,第一电离能低于同周期相邻元素 |
| Z | 价层电子数等于其电子层数 |
A.化合物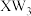 的VSEPR模型名称为三角锥形 的VSEPR模型名称为三角锥形 |
B.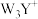 的中心原子采用 的中心原子采用 杂化 杂化 |
C.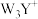 中W-Y-W键角比 中W-Y-W键角比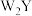 中的小 中的小 |
| D.组成为ZX的化合物属于分子晶体,是新型无机材料 |
您最近一年使用:0次
名校
8 . 某水性钠离子电池电极材料由Na+、Fe2+、Fe3+、CN-组成,其立方晶胞嵌入和嵌出Na+过程中,Fe2+与Fe3+含量发生变化,依次变为格林绿、普鲁士蓝、普鲁士白三种物质,其过程如图所示。下列说法错误的是
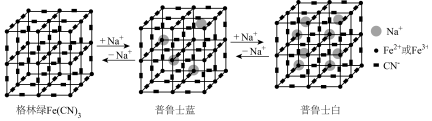

| A.格林绿晶体中Fe3+周围等距且最近的Fe3+数为6 |
| B.普鲁士蓝中Fe2+与Fe3+个数比为1∶2 |
| C.可以通过X射线衍射实验测定晶体结构 |
D.若普鲁士白的晶胞棱长为 pm则其晶体的密度为 pm则其晶体的密度为 ×1030g⋅cm−3 ×1030g⋅cm−3 |
您最近一年使用:0次
9 . 元素是组成我们生活中一切物质的“原材料”。下列说法错误的是
| A.人体中含量最多的元素是O |
B. 中S、C、N三种元素的第一电离能最大的是N 中S、C、N三种元素的第一电离能最大的是N |
| C.金刚石和石墨互为同素异形体 |
| D.LiCl和NaCl的晶体类型不同 |
您最近一年使用:0次
10 . 茶卡盐湖因盛产“大青盐”而闻名,枯水季节湖水中氯化钾含量最高值达 ,下列有关氯化钾的说法不正确的是
,下列有关氯化钾的说法不正确的是
 ,下列有关氯化钾的说法不正确的是
,下列有关氯化钾的说法不正确的是| A.氯化钾晶体属于离子晶体 | B.氯化钾溶液呈中性 |
| C.钾元素和氯元素均位于周期表的p区 | D.饱和氯化钾溶液能使蛋白质发生盐析 |
您最近一年使用:0次



