2023高三·全国·专题练习
解题方法
1 . “天问一号”着陆火星,“嫦娥五号”采回月壤,探索宇宙离不开化学。镍铼合金是制造喷气发动机的燃烧室、涡轮叶片及排气喷嘴的重要材料。75号元素铼Re,熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。
(1)镍原子价电子表示式为___________ ,在元素周期表中,铼与锰在同族,铼在元素周期表中的位置是___________ 。
(2)铼易形成高配位数的化合物如Re2(CO)10,该配合物中___________ (填元素符号)提供孤对电子与铼成键,原因是___________ ,1mol Re2(CO)10中有___________ mol配位键。
(3)锌在潮湿的空气中极易生成一层紧密的碱式碳酸锌[ZnCO3·3Zn(OH)2]薄膜,使其具有抗腐蚀性。碱式碳酸锌中非金属元素的电负性由大到小的顺序为___________ ,CO 的空间构型为
的空间构型为___________ (用文字描述)。与CO 互为等电子体的分子是
互为等电子体的分子是___________ (写一种即可)。
(4)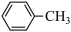 分子中碳原子的杂化类型为
分子中碳原子的杂化类型为___________ ,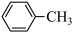 比
比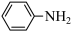 的熔点沸点
的熔点沸点___________ (填“高”或“低”),原因是___________ 。
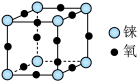
(5)三氧化铼晶胞如图所示,摩尔质量为Mg/mol,晶胞密度为bg/cm3,铼原子填在___________ 个氧原子围成的___________ (填“四面体”“立方体”或“八面体”)空隙中,该晶胞的空间利用率为___________ (铼的原子半径为rRepm,氧原子半径为rOpm,列出计算式)。
(1)镍原子价电子表示式为
(2)铼易形成高配位数的化合物如Re2(CO)10,该配合物中
(3)锌在潮湿的空气中极易生成一层紧密的碱式碳酸锌[ZnCO3·3Zn(OH)2]薄膜,使其具有抗腐蚀性。碱式碳酸锌中非金属元素的电负性由大到小的顺序为
 的空间构型为
的空间构型为 互为等电子体的分子是
互为等电子体的分子是(4)
 分子中碳原子的杂化类型为
分子中碳原子的杂化类型为 比
比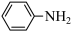 的熔点沸点
的熔点沸点(5)三氧化铼晶胞如图所示,摩尔质量为Mg/mol,晶胞密度为bg/cm3,铼原子填在

您最近一年使用:0次
解题方法
2 . A、B、C、D、E、F六种元素均位于元素周期表的前四周期,且原子序数依次增大。元素A是原子半径最小的元素;B元素基态原子的核外电子占据四个原子轨道;D元素原子的成对电子总数是未成对电子总数的3倍;E与D位于同一主族;F位于第Ⅷ族,在地壳中含量排金属中第二位。
(1)F2+的价电子排布图为_______ 。
(2)B、C、D元素的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(3)B、C、D的某些氢化物的分子中都含有18个电子,B的这种氢化物的中心原子杂化方式为_______ ,等物质的量B、C、D的这种氢化物的分子中含有σ键的个数之比为_______ 。
(4)D常见的两种单质D2和D3,其中_______ (填化学式)在水中的溶解度更大。
(5)B、E可形成分子式为BE2的化合物,其电子式为_______ 。
(6)实验室合成一种由B和C两种元素形成的化合物,该化合物具有三维骨架结构,其中每个B原子与4个C原子形成共价键,每个C原子与3个B原子形成共价键。其化学式为_______ , 预测该化合物熔点_______ 金刚石(填“高于”或“低于”)。
(1)F2+的价电子排布图为
(2)B、C、D元素的第一电离能由大到小的顺序是
(3)B、C、D的某些氢化物的分子中都含有18个电子,B的这种氢化物的中心原子杂化方式为
(4)D常见的两种单质D2和D3,其中
(5)B、E可形成分子式为BE2的化合物,其电子式为
(6)实验室合成一种由B和C两种元素形成的化合物,该化合物具有三维骨架结构,其中每个B原子与4个C原子形成共价键,每个C原子与3个B原子形成共价键。其化学式为
您最近一年使用:0次
名校
解题方法
3 . 现有A、B、C、D、E、F六种短周期元素,其相关性质信息如下。请回答下列问题:
(1)元素B在周期表中的位置为_______ ;D与F原子按个数比为1:1形成物质的结构式为_______
(2)A、C、D对应的简单离子的半径由大到小的排序是_______ (用离子符号表示)。
(3)B元素和A元素能够形成一种超硬物质,沸点为2249℃。该化合物的晶体类型为_______ ;若将C元素最高价氧化物的水化物溶于水,需要破坏的作用力为_______ 。
(4)在含有A的氯化物溶液中滴加过量氨水的离子方程式为_______ 。
(5)用电子式表示化合物FE的形成过程_______ 。
(6)已知CED2是一种强氧化性漂白剂。请写出在碱性条件下,CED2和BD2反应的离子方程式_______ 。
| 元素 | 特征 | 元素 | 特征 |
| A | 常见金属,其最高价氧化物对应的水化物可以溶于强碱 | D | 在地壳中含量最多 |
| B | 常见化肥的主要元素,单质常温下呈气态 | E | 单质为黄绿色有毒气体 |
| C | 在短周期主族元素中,原子半径最大 | F | 原子的核外电子只有1个 |
(2)A、C、D对应的简单离子的半径由大到小的排序是
(3)B元素和A元素能够形成一种超硬物质,沸点为2249℃。该化合物的晶体类型为
(4)在含有A的氯化物溶液中滴加过量氨水的离子方程式为
(5)用电子式表示化合物FE的形成过程
(6)已知CED2是一种强氧化性漂白剂。请写出在碱性条件下,CED2和BD2反应的离子方程式
您最近一年使用:0次
解题方法
4 . X、Y、Z为三种元素,X能与氢形成气态XH4,其中X的质量分数为75%;且X与Y能形成XY2型化合物。Y的原子核内质子数和中子数相等,在Y的氢化物中,Y的质量分数为88.9%。Z的最高价氧化物的水化物是酸性最强的酸。
(1)X的单质叫做______ ,它属于______ 晶体。
(2)Y的氢化物属于______ 晶体,它的电子式是______ 。
(3)Z元素位于周期表的第______ 周期______ 族,它的氢化物是______ 性分子。
(4)X与Z形成的化合物可用电子式表示为______ ,其分子的空间构型是______ 体,属于______ 性分子,它的晶体属于______ 晶体。
(1)X的单质叫做
(2)Y的氢化物属于
(3)Z元素位于周期表的第
(4)X与Z形成的化合物可用电子式表示为
您最近一年使用:0次
5 . 已知:A、B、C、D、E、F六种元素核电荷数依次增大,属元素周期表中前四周期的元素。其中A原子核外有三个未成对电子;B和E可形成离子化合物B2E,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满。请根据以上信息,回答下列问题:
⑴A、B、C、D的第一电离能由小到大的顺序为________ (用元素符号表示)。
⑵E与D的同族短周期元素可形成一种化合物X,X是常见的有机溶剂,X分子的空间构型是________ 。
⑶F原子的核外电子排布式是____________ ,F的高价离子与A的简单氢化物形成的配离子的化学式为________ 。
⑷A、F形成某种化合物的晶胞结构如图所示,则其化学式为________ (黑色球表示F原子)。

⑸A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为________ 。
⑴A、B、C、D的第一电离能由小到大的顺序为
⑵E与D的同族短周期元素可形成一种化合物X,X是常见的有机溶剂,X分子的空间构型是
⑶F原子的核外电子排布式是
⑷A、F形成某种化合物的晶胞结构如图所示,则其化学式为

⑸A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为
您最近一年使用:0次
名校
解题方法
6 . 已知A、B、C、D、E、F六种元素的原子序数依次增大,其中A元素的原子半径在短周期元素中最小,B原子核外电子有6种不同的运动状态;D原子L层上有2对成对电子。E元素在地壳中含量居第二位,F与E位于同一周期,且是该周期元素中电负性最大的元素。根据以上信息回答下列问题:
(1)E元素可分别与D元素、F元素形成两种常见化合物,这两种化合物的熔沸点高低顺序为__ (用化学式表示),原因是___ 。
(2)C的氢化物比下周期同族元素的氢化物沸点还要高,其原因是__ 。
(3)1molB2A2分子中含σ键的数目是__ 。
(4)图(Ⅰ)是B元素的单质晶体的一个晶胞,该晶胞中含有__ 个原子,若设晶胞的棱长为acm,阿伏加德罗常数的值为NA则该晶体的密度表达式为__ 。
(5)E单质存在与金刚石结构类似的晶体,晶体中原子之间以__ 相结合,其晶胞中共有8个原子,其中在面心位置贡献__ 个原子。
(6)BD2在高温高压下所形成的晶体其晶胞如图(Ⅱ)所示。该晶体的类型属于__ (填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子轨道的杂化类型为__ 。

(1)E元素可分别与D元素、F元素形成两种常见化合物,这两种化合物的熔沸点高低顺序为
(2)C的氢化物比下周期同族元素的氢化物沸点还要高,其原因是
(3)1molB2A2分子中含σ键的数目是
(4)图(Ⅰ)是B元素的单质晶体的一个晶胞,该晶胞中含有
(5)E单质存在与金刚石结构类似的晶体,晶体中原子之间以
(6)BD2在高温高压下所形成的晶体其晶胞如图(Ⅱ)所示。该晶体的类型属于

您最近一年使用:0次
7 . 已知X、Y、Z、R都是周期表中前四周期的元素,它们的核电荷数依次增大。X是空气中含量最高的元素,Z基态原子核外K、L、M三层电子数之比为1∶4∶2,R基态原子的3d原子轨道上的电子数是4 s原子轨道上的4倍,Y基态原子的最外层电子数等于Z、R基态原子的最外层电子数之和。(答题时,X、Y、Z、R用所对应的元素符号表示)
(1)X、Y、Z的第一电离能由小到大的顺序为_____ ,写出一种与ZY44-互为等电子体的分子的化学式:_____ 。

(2)R3+基态核外电子排布式为______ 。
(3)化合物Z3X4熔点高达1900℃以上,硬度很大。该物质的晶体类型是_____ 。
(4)Y、Z形成的某晶体的晶胞结构如右图所示,则该化合物的化学式为_____ 。
(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)6]2+,1 mol [R(NH3)6]2+中含有σ键的数目为______ 。
(1)X、Y、Z的第一电离能由小到大的顺序为

(2)R3+基态核外电子排布式为
(3)化合物Z3X4熔点高达1900℃以上,硬度很大。该物质的晶体类型是
(4)Y、Z形成的某晶体的晶胞结构如右图所示,则该化合物的化学式为
(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)6]2+,1 mol [R(NH3)6]2+中含有σ键的数目为
您最近一年使用:0次
10-11高三上·云南昆明·阶段练习
解题方法
8 . 已知A、B、C、D、E为原子序数依次增大的五种短周期元素。其中A与D、B与E同主族,C元素的最外层电子数是内层电子数的3倍,D元素在地壳中的含量仅次于氧,D的单质是良好的半导体材料,E元素的最高正价与最低负价的代数和为2。请回答:
(1)E元素的氢化物是 分子(填“极性”或“非极性”),电子式是 。
(2)A、B、C三种元素形成的氢化物的熔点由高到低的顺序是 。(用化学式表示)
(3)B、D、E三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是 ___ 。(用化学式表示)
(4)工业上用A单质制备D单质的化学方程式是 ,D和C形成的固体物质属于 晶体。
(1)E元素的氢化物是 分子(填“极性”或“非极性”),电子式是 。
(2)A、B、C三种元素形成的氢化物的熔点由高到低的顺序是 。(用化学式表示)
(3)B、D、E三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是 ___ 。(用化学式表示)
(4)工业上用A单质制备D单质的化学方程式是 ,D和C形成的固体物质属于 晶体。
您最近一年使用:0次



