解题方法
1 . 碳族元素中的碳、硅、锗及其化合物在诸多领域有重要用途。
(1)碳族元素位于周期表_______ 区,基态锗原子外围电子的轨道表示式为_______ ,基态锗原子核外有_______ 种空间运动状态不同的电子。
(2)科学家以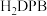 、
、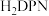 等双吡唑有机物为原料,制备了可去除痕量苯的吸附剂。
等双吡唑有机物为原料,制备了可去除痕量苯的吸附剂。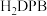 和
和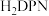 结构中含氮碳环均为平面结构,则N的杂化方式是
结构中含氮碳环均为平面结构,则N的杂化方式是_______ 。
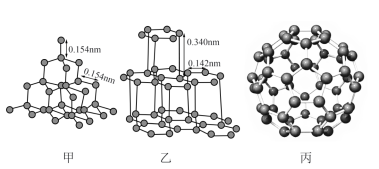
(3)金刚石(甲)、石墨(乙)、C60(丙)的结构如下图所示:
①12g金刚石和石墨中含有的σ键数目之比为_______ 。
②金刚石的熔点高于C60,但低于石墨,原因是_______ 。
③C60的晶胞呈分子密堆积,下列晶体中,与C60具有相同晶体结构的是_______ 。
A.CO2 B.冰 C.Zn D.Ag E.NaCl
(4)一种低温超导体立方晶胞结构如下图所示:
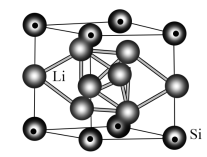
①该晶体的化学式为_______ 。
②若晶胞参数为apm,该晶体的密度ρ=_______  。(列出计算式即可,设NA表示阿伏加德罗常数的值)
。(列出计算式即可,设NA表示阿伏加德罗常数的值)
(1)碳族元素位于周期表
(2)科学家以
 、
、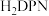 等双吡唑有机物为原料,制备了可去除痕量苯的吸附剂。
等双吡唑有机物为原料,制备了可去除痕量苯的吸附剂。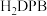 和
和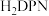 结构中含氮碳环均为平面结构,则N的杂化方式是
结构中含氮碳环均为平面结构,则N的杂化方式是
(3)金刚石(甲)、石墨(乙)、C60(丙)的结构如下图所示:

①12g金刚石和石墨中含有的σ键数目之比为
②金刚石的熔点高于C60,但低于石墨,原因是
③C60的晶胞呈分子密堆积,下列晶体中,与C60具有相同晶体结构的是
A.CO2 B.冰 C.Zn D.Ag E.NaCl
(4)一种低温超导体立方晶胞结构如下图所示:

①该晶体的化学式为
②若晶胞参数为apm,该晶体的密度ρ=
 。(列出计算式即可,设NA表示阿伏加德罗常数的值)
。(列出计算式即可,设NA表示阿伏加德罗常数的值)
您最近一年使用:0次
2 . 常见晶体的结构分析
(1)金刚石晶体



①在晶体中每个碳原子以_______ 个共价单键与相邻的_______ 个碳原子相结合,成为正四面体。
②晶体中C-C-C夹角为_______ ,碳原子采取了_______ 杂化。
③最小环上有_______ 个碳原子。
④晶体中碳原子个数与C-C键数之比为_______ 。
⑤在一个晶胞中,碳原子位于立方体的8个顶点、6个面心以及晶胞内部,由“均摊法”可求出该晶胞中实际含有的碳原子数为_______ 。
(2)二氧化硅晶体

①每个硅原子与相邻的_______ 个氧原子以共价键相结合构成_______ 结构,硅原子在正四面体的中心,4个氧原子在正四面体的4个顶点。晶体中Si原子与O原子个数比为_______ 。
②每个Si原子与4个O原子成键,每个O原子与_______ 个Si原子成键,最小的环是_______ 元环。
③每个最小的环实际拥有的硅原子为_______ ,氧原子数为_______ 。
④1molSiO2晶体中含Si-O键数目为_______ ,在SiO2晶体中Si、O原子均采取_______ 杂化。
⑤SiO2具有许多重要用途,是制造水泥、玻璃、人造红宝石、单晶硅、硅光电池、芯片和光导纤维的原料。
(1)金刚石晶体



①在晶体中每个碳原子以
②晶体中C-C-C夹角为
③最小环上有
④晶体中碳原子个数与C-C键数之比为
⑤在一个晶胞中,碳原子位于立方体的8个顶点、6个面心以及晶胞内部,由“均摊法”可求出该晶胞中实际含有的碳原子数为
(2)二氧化硅晶体

①每个硅原子与相邻的
②每个Si原子与4个O原子成键,每个O原子与
③每个最小的环实际拥有的硅原子为
④1molSiO2晶体中含Si-O键数目为
⑤SiO2具有许多重要用途,是制造水泥、玻璃、人造红宝石、单晶硅、硅光电池、芯片和光导纤维的原料。
您最近一年使用:0次
3 . 下列物质性质与用途不相应的是
| A.SO2具有漂白性,可用于纸浆漂白 |
| B.石墨具有良好的润滑性,可用作电池电极材料 |
| C.液氮的沸点较低,可为超导材料提供低温环境 |
| D.硫酸钡难溶于酸,可作为“胃镜”检查中的内服药剂 |
您最近一年使用:0次
4 . 非金属元素及其化合物在生活、生产中有着重要的用途
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的最外层电子排布式为___________ ,已知3种原子晶体的熔点数据如下表:
金刚石熔点比晶体硅熔点高的原因是___________ 。
(2)CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g) CS2(g)+2H2S(g),CS2分子的空间构型为
CS2(g)+2H2S(g),CS2分子的空间构型为___________ ,用燃煤废气(含N2、O2、SO2、CO2、H2O、NOx等)使尾气中的H2S转化为单质硫,可实现废物利用,保护环境,写出其中一个反应的化学方程式___________ 。
(3)中国传统的农具、兵器曾大量使用铁,铁器的修复是文物保护的重要课题。铁器表面氧化层的成分有多种,性质如下:
在有氧条件下,Fe3O4在含Cl–溶液中会转化为FeOCl,将相关反应的离子方程式补充完整___________ ,4Fe3O4 +_____O2 +______ +_____H2O _____FeOCl +___________,若4mol Fe3O4完全转化为FeOCl,则转移的电子数目为
_____FeOCl +___________,若4mol Fe3O4完全转化为FeOCl,则转移的电子数目为___________ 。
(4)化学修复可以使FeOCl转化为Fe3O4致密保护层:用Na2SO3和NaOH混合溶液浸泡锈蚀的铁器,一段时间后取出,再用NaOH溶液反复洗涤。
①FeOCl在NaOH的作用下转变为FeO(OH),推测溶解度FeOCl___________ FeO(OH)(填“>”或“<”)。
② Na2SO3的作用是___________ 。
③ 检验FeOCl转化完全的操作和现象是___________ 。
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的最外层电子排布式为
| 金刚石 | 碳化硅 | 晶体硅 | |
| 熔点/℃ | >3550 | 2600 | 1415 |
金刚石熔点比晶体硅熔点高的原因是
(2)CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g)
 CS2(g)+2H2S(g),CS2分子的空间构型为
CS2(g)+2H2S(g),CS2分子的空间构型为(3)中国传统的农具、兵器曾大量使用铁,铁器的修复是文物保护的重要课题。铁器表面氧化层的成分有多种,性质如下:
| 成分 | Fe3O4 | FeO(OH) | FeOCl |
| 性质 | 致密 | 疏松 | 疏松 |
在有氧条件下,Fe3O4在含Cl–溶液中会转化为FeOCl,将相关反应的离子方程式补充完整
 _____FeOCl +___________,若4mol Fe3O4完全转化为FeOCl,则转移的电子数目为
_____FeOCl +___________,若4mol Fe3O4完全转化为FeOCl,则转移的电子数目为(4)化学修复可以使FeOCl转化为Fe3O4致密保护层:用Na2SO3和NaOH混合溶液浸泡锈蚀的铁器,一段时间后取出,再用NaOH溶液反复洗涤。
①FeOCl在NaOH的作用下转变为FeO(OH),推测溶解度FeOCl
② Na2SO3的作用是
③ 检验FeOCl转化完全的操作和现象是
您最近一年使用:0次
名校
解题方法
5 . 砷(As)、镓(Ga)等形成的化合物在现代工业中有广泛的用途,其中砷化镓是一种重要的半导体材料,晶胞结构如图所示,其熔点为1238℃,以下说法正确的是


| A.一个晶胞中As原子的个数为4 |
| B.As的配位数是2 |
| C.砷化镓、砷化铝、砷化硼的熔沸点逐渐降低 |
| D.砷化镓晶体中每个原子均形成4个共价键 |
您最近一年使用:0次
2022-07-13更新
|
241次组卷
|
2卷引用:山东省德州市2021-2022学年高二下学期期末考试化学试题



