解题方法
1 . 除去Na2CO3粉末中混有的少量NaHCO3的方法是___________ 。
您最近一年使用:0次
解题方法
2 . 现有A、B、C三种烃,其球棍模型如下图:
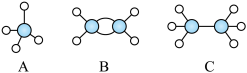
(1)等质量的以上三种物质完全燃烧时消耗O2最多的是___________ (填对应的字母)。
(2)在120℃、101KPa条件下,将以上三种烃和足量O2混合点燃,完全燃烧后恢复到相同条件,测得有些气体在反应前后气体总体积没有发生变化,满足条件的气体是___________ (填对应的字母)。
(3)工业上合成一氯乙烷,应选___________ 为原料(填对应的字母)。
(4)要除去C中混有的B可以采用的方法是___________。
(5)烃D是B的一种同系物,其密度是相同条件下B的2倍,则烃D的同分异构体有___________ 种。(不包括D本身,且不考虑立体异构)

(1)等质量的以上三种物质完全燃烧时消耗O2最多的是
(2)在120℃、101KPa条件下,将以上三种烃和足量O2混合点燃,完全燃烧后恢复到相同条件,测得有些气体在反应前后气体总体积没有发生变化,满足条件的气体是
(3)工业上合成一氯乙烷,应选
(4)要除去C中混有的B可以采用的方法是___________。
| A.将气体通过酸性高锰酸钾溶液 |
| B.将气体通过溴水 |
| C.一定条件下,向混合气体中通入H2 |
| D.将气体通过NaOH溶液 |
您最近一年使用:0次
名校
解题方法
3 . 除去括号中的杂质,填写涉及的反应方程式。
| 编号 | 混合物 | 方程式 |
| ① | 溶液: | |
| ② | 固体: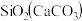 | |
| ③ | 气体: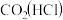 | |
| ④ | 固体: |
您最近一年使用:0次
4 . 为除去粗盐中的Ca2+、Mg2+、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

请回答:
(1)步骤⑦需采用的主要物质分离提纯操作,名称是_______ ,所需要的玻璃仪器除酒精灯、玻璃棒、烧杯外,还要_______ 。
(2)步骤④加入过量Na2CO3的目的是_______ 。
(3)步骤⑥需加入适量的____ (填试剂名称),所发生反应的化学方程式为________ 。
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
请回答:
(1)步骤⑦需采用的主要物质分离提纯操作,名称是
(2)步骤④加入过量Na2CO3的目的是
(3)步骤⑥需加入适量的
您最近一年使用:0次
解题方法
5 . (1)下列A、B、C、D、E是中学化学中常见的混合物分离或提纯的基本方法
A.蒸馏 B.过滤 C.萃取 D.蒸发 E.分液
请根据混合物分离或提纯的原理将所需正确操作的序号填入空格中:
用自来水制取蒸馏水___________ ;分离植物油和水___________ ;除去粗盐中的泥沙___________ 。
(2)实验室配制100mL 1mol/L的NaOH溶液,请回答下列问题:
①配制过程中需要的玻璃仪器除了烧杯、量筒、玻璃棒之外,还需要用到___________ 、___________ 。
②将烧杯中的溶液没有冷却就转移到容量瓶中,最后配成的溶液的物质的量浓度会___________ (填“偏大”、 “偏小”或 “无影响”)。
A.蒸馏 B.过滤 C.萃取 D.蒸发 E.分液
请根据混合物分离或提纯的原理将所需正确操作的序号填入空格中:
用自来水制取蒸馏水
(2)实验室配制100mL 1mol/L的NaOH溶液,请回答下列问题:
①配制过程中需要的玻璃仪器除了烧杯、量筒、玻璃棒之外,还需要用到
②将烧杯中的溶液没有冷却就转移到容量瓶中,最后配成的溶液的物质的量浓度会
您最近一年使用:0次
名校
6 . 根据下列装置填空
(1)分离水和植物油,选用____________ (填序号,下同)。
(2)配制100mL0.1mol·L-1NaOH溶液选用____________
(3)鉴别Na2CO3和NaHCO3固体选用____________
(4)可实现化学能直接转化为电能的是____________ ,该装置为____________ 装置,________ 作负极,外电路电子由 ________ 流向________ 。
(1)分离水和植物油,选用
(2)配制100mL0.1mol·L-1NaOH溶液选用
(3)鉴别Na2CO3和NaHCO3固体选用
(4)可实现化学能直接转化为电能的是
 |  |  |  |
| ① | ② | ③ | ④ |
您最近一年使用:0次
解题方法
7 . 对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发结晶、③蒸馏、④萃取、⑤分液等。写出下列各组混合物的分离或提纯应采用的方法。
(1)提取碘水中的碘,可用__ 法;
(2)从硫酸铜的悬浊液中分离出氧化铜,可用__ 法;
(3)除去食盐中的水,可用__ 法;
(4)分离植物油和水,可用可用__ 法。
(1)提取碘水中的碘,可用
(2)从硫酸铜的悬浊液中分离出氧化铜,可用
(3)除去食盐中的水,可用
(4)分离植物油和水,可用可用
您最近一年使用:0次
名校
8 . 按要求填空
(1)酸雨的pH<___ 。
(2)制造光导纤维的材料是___ ;三硅酸镁(Mg2Si3O8·11H2O)用氧化物表示__ 。
(3)除去NaHCO3溶液中少量的Na2CO3杂质相应的离子方程式为___ 。
(1)酸雨的pH<
(2)制造光导纤维的材料是
(3)除去NaHCO3溶液中少量的Na2CO3杂质相应的离子方程式为
您最近一年使用:0次
名校
9 . 化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,这些废液必须经处理后才能排放。某化学实验室产生的废液中含有两种金属离子:Fe3+、Cu2+,化学小组设计了如下图所示的方案对废液进行处理,以回收金属,保护环境。

(1)操作①的名称是_______ 。
(2)沉淀A中含有的金属单质有_______ 。
(3)操作②中观察到的实验现象是_______ 。
(4)操作③中发生反应的离子方程式为_______ 。

(1)操作①的名称是
(2)沉淀A中含有的金属单质有
(3)操作②中观察到的实验现象是
(4)操作③中发生反应的离子方程式为
您最近一年使用:0次
2019-02-12更新
|
526次组卷
|
3卷引用:新疆阿克苏地区新和县实验中学2020-2021学年高一下学期期末考试化学试题
名校
10 . (1)一个铁原子的质量为m g, 设NA表示阿伏伽德罗常数的值,则铁的摩尔质量为_______ 。
(2)标准状况下4.48L CO和CO2混合气,质量为7.2g 。其中CO的体积分数为__ 。
(3)将饱和FeCl3溶液滴入沸水中,继续加热至液体变为________ 色,得到的是Fe(OH)3胶体,区别Fe(OH)3胶体和饱和FeCl3溶液的方法是_______ ,将Fe(OH)3胶体装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极区域附近的颜色加深,这说明______ ,这种现象称为电泳。
(4)实验室将氯酸钾和二氧化锰固体混合物充分加热至不再产生气体,从所剩固体混合物中提取纯净的二氧化锰的操作依次为_______ 、 ________ 、 ________ 、 ________ 。
(2)标准状况下4.48L CO和CO2混合气,质量为7.2g 。其中CO的体积分数为
(3)将饱和FeCl3溶液滴入沸水中,继续加热至液体变为
(4)实验室将氯酸钾和二氧化锰固体混合物充分加热至不再产生气体,从所剩固体混合物中提取纯净的二氧化锰的操作依次为
您最近一年使用:0次
2019-01-07更新
|
266次组卷
|
3卷引用:新疆生产建设兵团第二中学2019-2020学年高一上学期期末考试化学试题



