名校
1 . 过氧化锶(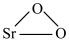 )通常用作分析试剂、氧化剂、漂白剂等。SrO2是一种白色粉末,加热条件下可与CO2、水蒸气反应,室温时在水中逐渐形成无色晶体SrO2·8H2O,与酸作用生成H2O2。
)通常用作分析试剂、氧化剂、漂白剂等。SrO2是一种白色粉末,加热条件下可与CO2、水蒸气反应,室温时在水中逐渐形成无色晶体SrO2·8H2O,与酸作用生成H2O2。
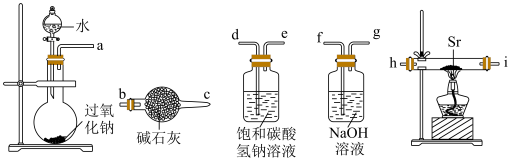
②SrO2在空气中会变质生成碳酸盐,写出该反应的化学方程式
③连接好装置进行实验,实验步骤如下,正确的操作顺序为
a、打开分液漏斗活塞,将水滴入烧瓶中b、检查装置气密性c、在相应装置中装入药品d、加热e、关闭分液漏斗活塞f、停止加热
(2)乙同学在通入氨气的条件下,在水溶液中可制备得到SrO2·8H2O,实验装置如图:
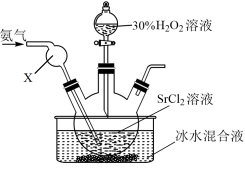
②写出该方法制备SrO2·8H2O的离子方程式
③实验结束后,得到SrO2·8H2O的操作为
(3)除SrO2·8H2O外,请选择下列试剂:FeCl2溶液、HCl溶液、HNO3溶液、KSCN溶液、H2O2溶液设计实验证明SrO2的氧化性比FeCl3的氧化性强:
您最近一年使用:0次
2 . 下列实验能达到实验目的的是
|
|
| A.钠的燃烧反应 | B.关闭止水夹a,打开活塞b,可检查装置气密性 |
|
|
| C.中和滴定 | D.证明非金属性:S>C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 查阅资料得知MnO2+NaBr+H2SO4→Na2SO4+MnSO4+Br2↑+H2O(未配平)。某兴趣小组的同学利用如图所示的装置探究苯与液溴的反应类型。下列说法正确的是


| A.实验装置的连接顺序为c→a→d→b,b中产生淡黄色沉淀,证明苯与液溴发生的是取代反应 |
| B.装置c中发生反应的还原剂与氧化剂物质的量之比为2∶1 |
| C.装置d中仪器G的名称为直形冷凝管 |
| D.反应后装置d中混合液经碱洗、分液后,上层液体蒸馏得到溴苯 |
您最近一年使用:0次
4 . 实验室制取溴苯的装置如图所示。向二颈烧瓶中先滴入0.5 mL Br2,静置,经片刻诱导期后反应开始。再缓慢滴加其余的Br2, 维持体系微沸至Br2加完,70~ 80°C水浴15min。(诱导期:催化反应中形成过渡态且总反应速率为0的时期)反应结束后产品处理:
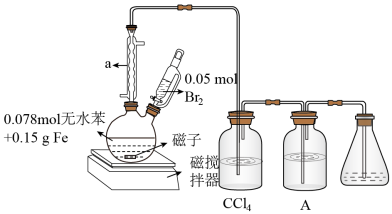
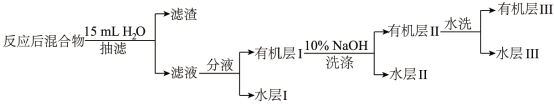
有关数据如下:
回答下列问题:
(1)仪器a的名称是_____________________ 。
(2)溴苯的制备需在无水条件下进行,原因是________________ 。
(3)A装置盛装_______ ( 填试剂)用于检验诱导期已过,反应开始。
(4)当出现_____________ ( 填现象)时,证明反应已结束。
(5)产品后处理阶段,有机层I用10% NaOH溶液洗涤其离子反应方程式为________ ,有机层Ⅱ水洗的目的是____________ 。
(6)有机层Ⅲ经干燥后分离出纯净溴苯的操作名称是_______ 。


有关数据如下:
物质 | 苯 | 溴 | 溴苯 |
密度(g· cm-3) | 0.88 | 3.12 | 1.50 |
沸点/°C | 80 | 59 | 156 |
在水中的溶解性 | 不溶 | 微溶 | 不溶 |
(1)仪器a的名称是
(2)溴苯的制备需在无水条件下进行,原因是
(3)A装置盛装
(4)当出现
(5)产品后处理阶段,有机层I用10% NaOH溶液洗涤其离子反应方程式为
(6)有机层Ⅲ经干燥后分离出纯净溴苯的操作名称是
您最近一年使用:0次
5 . 铋酸钠(NaBiO3)是分析化学中的重要试剂,在水中缓慢分解,遇沸水或酸则迅速分解。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
I.制取铋酸钠。制取装置如图(加热和夹持仪器已略去),部分物质性质如下:

(1)装二氧化锰的仪器名称是_______ ,B装置的作用是_______ 。
(2)C中盛放Bi(OH)3与NaOH的混合物,与Cl2反应生成NaBiO3,反应的化学方程式为:_______ 。
(3)当观察到C中_______ (填现象)时,可以初步判断C中反应已经完成。
(4)拆除装置前必须先除去残留的Cl2,以免污染空气。除去烧瓶A中残留Cl2的操作是:关闭_______ ,打开_______ (填K1、 K2或K3)。
(5)反应结束后,为从装置C中获得尽可能多的产品,需要的操作是_______ 、过滤、 洗涤、干燥。
II.铋酸钠的应用——检验Mn2+
(6)往待检液中加入铋酸钠晶体,加硫酸酸化,生成Bi3+,且溶液变为紫红色,证明待检液中存在Mn2+,产生紫红色现象的离子方程式为_______ 。
III.产品纯度的测定
(7)取上述NaBiO3产品wg,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用a mol·L-1的H2C2O4标准溶液滴定生成的 (已知: 5H2C2O4+ 2
(已知: 5H2C2O4+ 2 + 6H+=10CO2 + 2Mn2+ +8H2O),当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为
+ 6H+=10CO2 + 2Mn2+ +8H2O),当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为_______ (已知NaBiO3摩尔质量为Mg/mol,用含w、a、 b、M的代数式表示)。
I.制取铋酸钠。制取装置如图(加热和夹持仪器已略去),部分物质性质如下:

| 物质 | NaBiO3 | Bi(OH)3 |
| 性质 | 不溶于冷水, 浅黄色 | 难溶于水,白色 |
(2)C中盛放Bi(OH)3与NaOH的混合物,与Cl2反应生成NaBiO3,反应的化学方程式为:
(3)当观察到C中
(4)拆除装置前必须先除去残留的Cl2,以免污染空气。除去烧瓶A中残留Cl2的操作是:关闭
(5)反应结束后,为从装置C中获得尽可能多的产品,需要的操作是
II.铋酸钠的应用——检验Mn2+
(6)往待检液中加入铋酸钠晶体,加硫酸酸化,生成Bi3+,且溶液变为紫红色,证明待检液中存在Mn2+,产生紫红色现象的离子方程式为
III.产品纯度的测定
(7)取上述NaBiO3产品wg,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用a mol·L-1的H2C2O4标准溶液滴定生成的
 (已知: 5H2C2O4+ 2
(已知: 5H2C2O4+ 2 + 6H+=10CO2 + 2Mn2+ +8H2O),当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为
+ 6H+=10CO2 + 2Mn2+ +8H2O),当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为
您最近一年使用:0次
解题方法
6 . 高铁酸钾(K2FeO4)是一种强氧化剂和环境友好型水处理剂,易分解,遇水和酸易变质。某学习小组在实验室对高铁酸钾的制备和一些性质进行探究。回答下列问题:
(1)高铁酸钾的制备,装置如图1所示。
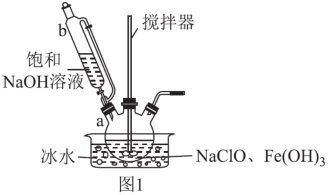
步骤一:将b中饱和NaOH溶液全部逐滴滴入a中,充分反应;
步骤二:由b向a中反应后液体中加入饱和KOH溶液;
步骤三:将a中所得浊液移出,分离提纯。
①仪器b的名称是_______ ,其侧管的作用为_______ 。
②a中制备Na2FeO4反应的离子方程式为_______ 。
③K2FeO4悬浊液经过滤、洗涤,可得粗产品。粗产品中的可溶性杂质可通过_______ 方法进一步提纯。
(2)K2FeO4遇水转化为Fe(OH)3,则其能用于净水的原理为:_______ 。
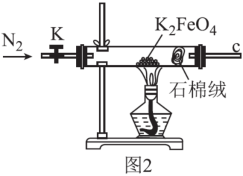
(3)用图2所示装置探究K2FeO4受热分解的产物。设计实验方案证明完全分解后的固体产物中不含Fe(II):取完全分解后的少量固体,溶于稀硫酸,_______ 。
(4)实验室可用间接碘量法测定含少量KCl杂质的K2FeO4样品的纯度:称取0.9000gK2FeO4样品溶于碱性KI溶液中,调节pH使混合液充分反应。用1.000mol·L-1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液15.00mL。请计算K2FeO4样品的纯度:_______ 。
已知: +4I-+8H+=Fe2++2I2+4H2O;I2+2
+4I-+8H+=Fe2++2I2+4H2O;I2+2 =
= +2I-。
+2I-。
(1)高铁酸钾的制备,装置如图1所示。

步骤一:将b中饱和NaOH溶液全部逐滴滴入a中,充分反应;
步骤二:由b向a中反应后液体中加入饱和KOH溶液;
步骤三:将a中所得浊液移出,分离提纯。
①仪器b的名称是
②a中制备Na2FeO4反应的离子方程式为
③K2FeO4悬浊液经过滤、洗涤,可得粗产品。粗产品中的可溶性杂质可通过
(2)K2FeO4遇水转化为Fe(OH)3,则其能用于净水的原理为:
(3)用图2所示装置探究K2FeO4受热分解的产物。设计实验方案证明完全分解后的固体产物中不含Fe(II):取完全分解后的少量固体,溶于稀硫酸,

(4)实验室可用间接碘量法测定含少量KCl杂质的K2FeO4样品的纯度:称取0.9000gK2FeO4样品溶于碱性KI溶液中,调节pH使混合液充分反应。用1.000mol·L-1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液15.00mL。请计算K2FeO4样品的纯度:
已知:
 +4I-+8H+=Fe2++2I2+4H2O;I2+2
+4I-+8H+=Fe2++2I2+4H2O;I2+2 =
= +2I-。
+2I-。
您最近一年使用:0次
7 .  是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备
是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备 ,并探究其有关性质。
,并探究其有关性质。

已知:ⅰ.无水 为蓝色,易溶于水及乙醇等有机溶剂。
为蓝色,易溶于水及乙醇等有机溶剂。
ⅱ. 常用作吸水剂,遇水剧烈水解生成
常用作吸水剂,遇水剧烈水解生成 和
和 ,其熔点
,其熔点 ,沸点
,沸点 ,
, 以上时易分解。
以上时易分解。
回答下列问题:
(1)仪器a的名称是_______ 。
(2)滴加 ,一段时间后容器A中充满白雾,发生反应的化学方程式为
,一段时间后容器A中充满白雾,发生反应的化学方程式为_______ 。
(3)无水 的作用是
的作用是_______ 。
(4)将A中反应混合物隔绝空气减压蒸馏,得到无水 晶体。下列装置适合作为冷凝和接收装置的是
晶体。下列装置适合作为冷凝和接收装置的是_______ (填序号)。

(5)某同学向无水氯化钴中加入95%乙醇溶液,得到蓝色溶液,滴加蒸馏水溶液由蓝色变为粉红色【查阅资料得知 为蓝色、
为蓝色、 为粉红色】。
为粉红色】。
①变色过程中发生反应的离子方程式为_______ 。
②资料显示变色反应为可逆反成,请选取合适试剂设计实验进行证明,简述实验方案_______ (可进用的试剂,浓盐酸、蒸馏水、稀硫酸)。
 是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备
是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备 ,并探究其有关性质。
,并探究其有关性质。
已知:ⅰ.无水
 为蓝色,易溶于水及乙醇等有机溶剂。
为蓝色,易溶于水及乙醇等有机溶剂。ⅱ.
 常用作吸水剂,遇水剧烈水解生成
常用作吸水剂,遇水剧烈水解生成 和
和 ,其熔点
,其熔点 ,沸点
,沸点 ,
, 以上时易分解。
以上时易分解。回答下列问题:
(1)仪器a的名称是
(2)滴加
 ,一段时间后容器A中充满白雾,发生反应的化学方程式为
,一段时间后容器A中充满白雾,发生反应的化学方程式为(3)无水
 的作用是
的作用是(4)将A中反应混合物隔绝空气减压蒸馏,得到无水
 晶体。下列装置适合作为冷凝和接收装置的是
晶体。下列装置适合作为冷凝和接收装置的是
(5)某同学向无水氯化钴中加入95%乙醇溶液,得到蓝色溶液,滴加蒸馏水溶液由蓝色变为粉红色【查阅资料得知
 为蓝色、
为蓝色、 为粉红色】。
为粉红色】。①变色过程中发生反应的离子方程式为
②资料显示变色反应为可逆反成,请选取合适试剂设计实验进行证明,简述实验方案
您最近一年使用:0次
8 . 下列与实验相关的叙述正确的是
| A.碳酸钠溶液应保存在带有玻璃塞的试剂瓶中 |
| B.将氯化铁溶液直接加热蒸干制得氯化铁晶体 |
| C.用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na+,无K+ |
| D.配制0.1mol/L的H2SO4溶液,用量筒量取浓硫酸时,仰视读数,使结果偏高 |
您最近一年使用:0次
2022-09-05更新
|
313次组卷
|
4卷引用:陕西省渭南市大荔县2023届高三一模化学试题
9 . 为完成下列各组实验,所选玻璃仪器和试剂均正确、完整的是(非玻璃仪器任选;不考虑存放试剂的容器)
| 实验 | 玻璃仪器 | 试剂 | |
| A | 食盐精制 | 漏斗、烧杯、玻璃棒 | 粗食盐水、稀盐酸、NaOH溶液、BaCl2溶液、Na2CO3溶液 |
| B | 证明HCN和碳酸的酸性强弱 | 玻璃棒、玻璃片 | 0.lmol·L-1NaCN溶液和0.1mol·L-1 Na2CO3溶液 |
| C | 乙醛官能团的检验 | 试管、胶头滴管、酒精灯 | 乙醛溶液、10%NaOH溶液、2%CuSO4溶液 |
| D | 证Ksp[Mg(OH)2]>Ksp[Cu(OH)2] | 试管、胶头滴管 | 含有少量CuCl2的MgCl2溶液、稀氨水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-03更新
|
1100次组卷
|
3卷引用:山东省济宁市2022届高三下学期3月一模考试化学试题
名校
解题方法
10 . 利用下表提供的主要玻璃仪器(不考虑存放试剂的仪器)和试剂能实现实验目的的是
| 选项 | 实验目的 | 玻璃仪器 | 试剂 |
| A | 乙醛官能团的检验 | 试管、烧杯、胶头滴管、酒精灯 | 乙醛溶液、10% 溶液、2% 溶液、2% 溶液 溶液 |
| B | 制备并分离乙酸乙酯 | 试管、量筒、导管、酒精灯、蒸馏烧瓶 | 冰醋酸、无水乙醇、浓硫酸、 溶液 溶液 |
| C | 证明亚硫酸酸性强于碳酸 | 玻璃棒、表面皿 | pH试纸、饱和 溶液、饱和 溶液、饱和 溶液 溶液 |
| D | 食盐精制 | 漏斗、烧杯、玻璃棒 | 粗食盐水、稀盐酸、 溶液、 溶液、 溶液、 溶液、 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次







