名校
1 . 下列说法不正确的是
| A.容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,容量瓶水洗后不用润洗 |
| B.因为盐的水解是吸热过程,所以加热可提高盐的水解速率 |
C.为了证明氯化铵溶液可促进 固体的溶解,可向两份等量 固体的溶解,可向两份等量 固体中分别加入等体积蒸馏水和 固体中分别加入等体积蒸馏水和 溶液 溶液 |
D.在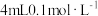 的 的 溶液中滴加数滴1mol/L的NaOH溶液,溶液颜色从橙色变成黄色 溶液中滴加数滴1mol/L的NaOH溶液,溶液颜色从橙色变成黄色 |
您最近一年使用:0次
名校
2 . 下列说法错误的是
| A.用洁净的铂丝蘸取溶液进行焰色试验,火焰呈黄色,证明溶液中有Na+,可能有K+ |
| B.电解质溶于水或受热熔化时,形成自由移动的离子的过程叫做电离 |
| C.容量瓶需要用蒸馏水洗涤、干燥后才可使用 |
| D.不能用澄清的石灰水鉴别Na2CO3和NaHCO3两种溶液 |
您最近一年使用:0次
2021-12-18更新
|
199次组卷
|
2卷引用:贵州省黔南州都匀市都匀第一中学2021-2022学年高一上学期期中化学试题
名校
3 . 实验是研究化学的基础,请回答下列问题:
(1)下列仪器在使用前一定要检查是否漏液的是_____ 。
A.容量瓶 B.冷凝管 C.碱式滴定管 D.长颈漏斗 E.分液漏斗
(2)如图所示是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是____
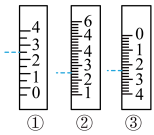
A.①是量筒,读数为2.5mL B.②是量筒,读数为2.5mL
C.③是滴定管,读数为2.4mL D.②是温度计,读数是2.5℃
(3)下列实验不能获得成功的是_____ (填代号)
①用托盘天平称取5.85gNaCl固体,用100mL容量瓶,配制1mol/L的溶液
②一氯丙烷与氢氧化钠溶液共热,水解后加入硝酸银溶液检验氯元素
③做过银镜反应的试管用稀HNO3清洗
④做乙醛的还原性实验:将2mL1mol/L硫酸铜溶液和4mL0.4mol/L氢氧化钠溶液混合后 滴入乙醛溶液,加热至沸
滴入乙醛溶液,加热至沸
⑤用乙醇制乙烯时为便于控制温度,要用水浴加热
(4)下列实验的操作或所用的试剂有错误的是____ 。
A.某些强氧化剂如氯酸钾、硝酸钾、高锰酸钾等,不能研磨,否则将引起爆炸
B.受溴腐蚀可以先用苯洗伤口,再用水洗
C.实验室制溴苯时可以先加铁丝,再加液溴,最后加入苯
D.证明分子CH2=CH-CHO既含有醛基又含有C=C,可先向溶液中加入足量的银氨溶液加热,充分反应后,再加入足量的溴水
E.吸入氯气可以吸入少量酒精或乙醚的混合蒸气解毒
F.可以用新制氢氧化铜检验乙醛、葡萄糖、甘油
(1)下列仪器在使用前一定要检查是否漏液的是
A.容量瓶 B.冷凝管 C.碱式滴定管 D.长颈漏斗 E.分液漏斗
(2)如图所示是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是

A.①是量筒,读数为2.5mL B.②是量筒,读数为2.5mL
C.③是滴定管,读数为2.4mL D.②是温度计,读数是2.5℃
(3)下列实验不能获得成功的是
①用托盘天平称取5.85gNaCl固体,用100mL容量瓶,配制1mol/L的溶液
②一氯丙烷与氢氧化钠溶液共热,水解后加入硝酸银溶液检验氯元素
③做过银镜反应的试管用稀HNO3清洗
④做乙醛的还原性实验:将2mL1mol/L硫酸铜溶液和4mL0.4mol/L氢氧化钠溶液混合后
 滴入乙醛溶液,加热至沸
滴入乙醛溶液,加热至沸⑤用乙醇制乙烯时为便于控制温度,要用水浴加热
(4)下列实验的操作或所用的试剂有错误的是
A.某些强氧化剂如氯酸钾、硝酸钾、高锰酸钾等,不能研磨,否则将引起爆炸
B.受溴腐蚀可以先用苯洗伤口,再用水洗
C.实验室制溴苯时可以先加铁丝,再加液溴,最后加入苯
D.证明分子CH2=CH-CHO既含有醛基又含有C=C,可先向溶液中加入足量的银氨溶液加热,充分反应后,再加入足量的溴水
E.吸入氯气可以吸入少量酒精或乙醚的混合蒸气解毒
F.可以用新制氢氧化铜检验乙醛、葡萄糖、甘油
您最近一年使用:0次
名校
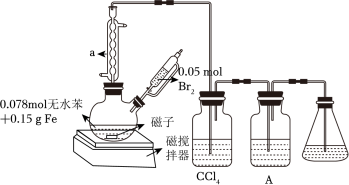
4 . 实验室制取溴苯的装置如图所示。
有关数据如下:
回答下列问题:
(1)仪器a的作用是___________ 。
(2)二颈烧瓶中生成有机物发生反应的化学方程式为___________ 。
(3)A装置盛装___________ (填试剂)用于检验诱导期已过,反应开始。当出现 ___________ (填现象)时,证明反应已结束。
(4)取反应后的混合物,经过一系列操作得到纯净的溴苯:
①水洗除去___________ ,分液;
②用NaOH稀溶液洗涤,除去___________ ,分液;
③水洗,分液;
④用干燥剂干燥,过滤;
⑤___________ ,分离溴苯和苯。
(5)经过一系列操作得到纯净的溴苯5ml,产率为___________ (保留三位有效数字)。
有关数据如下:
| 物质 | 苯 | 溴 | 溴苯 |
| 密度(g•cm﹣3) | 0.88 | 3.12 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 在水中的溶解性 | 不溶 | 微溶 | 不溶 |
(1)仪器a的作用是
(2)二颈烧瓶中生成有机物发生反应的化学方程式为
(3)A装置盛装
(4)取反应后的混合物,经过一系列操作得到纯净的溴苯:
①水洗除去
②用NaOH稀溶液洗涤,除去
③水洗,分液;
④用干燥剂干燥,过滤;
⑤
(5)经过一系列操作得到纯净的溴苯5ml,产率为
您最近一年使用:0次
5 . 下列有关实验操作正确的是
 |  |  |  |
| A.灼烧干海带 | B.证明酸性:盐酸>碳酸>硅酸 | C.制取 | D.检验铜与浓硫酸反应的氧化产物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 .  是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与还原剂接触或加热时会发生燃烧并爆炸。
是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与还原剂接触或加热时会发生燃烧并爆炸。
已知: 的熔点为-116℃,沸点为3.8℃,
的熔点为-116℃,沸点为3.8℃, 的沸点为-34.6℃;
的沸点为-34.6℃;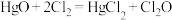 ,液氨是一种制冷剂。制取
,液氨是一种制冷剂。制取 的装置如图所示。
的装置如图所示。
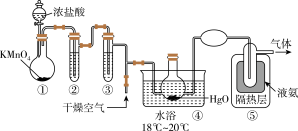
回答下列问题。
(1)①中盛放浓盐酸的仪器名称为_______ ,写出①中发生的化学反应方程式_______ 。
(2)该实验可证明 的氧化性比
的氧化性比 的氧化性
的氧化性_______ (填“强”或“弱”),浓盐酸在反应中表现出的性质有_______ 。
(3)装置②中盛放的试剂为_______ ;装置③的作用_______ 。
(4)产物 在装置
在装置_______ 中收集。
(5)从装置⑤中逸出的气体主要成分为_______ 。
 是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与还原剂接触或加热时会发生燃烧并爆炸。
是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与还原剂接触或加热时会发生燃烧并爆炸。已知:
 的熔点为-116℃,沸点为3.8℃,
的熔点为-116℃,沸点为3.8℃, 的沸点为-34.6℃;
的沸点为-34.6℃;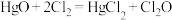 ,液氨是一种制冷剂。制取
,液氨是一种制冷剂。制取 的装置如图所示。
的装置如图所示。
回答下列问题。
(1)①中盛放浓盐酸的仪器名称为
(2)该实验可证明
 的氧化性比
的氧化性比 的氧化性
的氧化性(3)装置②中盛放的试剂为
(4)产物
 在装置
在装置(5)从装置⑤中逸出的气体主要成分为
您最近一年使用:0次
名校
7 . 直接排放含 的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关
的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关 性质的探究活动。
性质的探究活动。
(1)写出证明 弱氧化性的化学方程式
弱氧化性的化学方程式________ 。
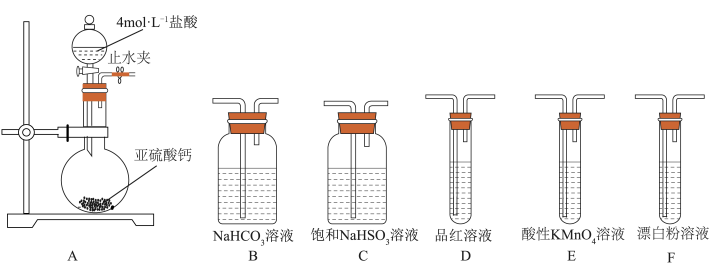
(2)写出下图装置A中滴加盐酸仪器的名称:________ 。
①甲同学认为按照A→C→F顺序连接装置可以比较亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是________ 。
②丙同学设计的合理实验方案为A→________ →尾气处理(填字母)。其中装置C的作用是________ 。证明亚硫酸酸性强于次氯酸的实验现象是________ 。
(4)利用下图的装置可测定装置A残液中 的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使
的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使 全部逸出并与锥形瓶中的
全部逸出并与锥形瓶中的 溶液恰好完全反应,然后用浓度为
溶液恰好完全反应,然后用浓度为 溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
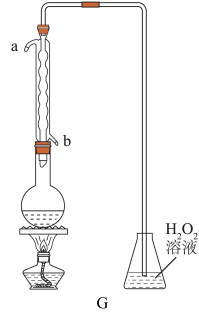
残液中 的含量为
的含量为________  。
。
 的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关
的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关 性质的探究活动。
性质的探究活动。(1)写出证明
 弱氧化性的化学方程式
弱氧化性的化学方程式(2)写出下图装置A中滴加盐酸仪器的名称:
①甲同学认为按照A→C→F顺序连接装置可以比较亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是
②丙同学设计的合理实验方案为A→
(4)利用下图的装置可测定装置A残液中
 的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使
的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使 全部逸出并与锥形瓶中的
全部逸出并与锥形瓶中的 溶液恰好完全反应,然后用浓度为
溶液恰好完全反应,然后用浓度为 溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
残液中
 的含量为
的含量为 。
。
您最近一年使用:0次
8 . 实验室可用下列装置(部分夹持仪器略去)制取SO2并验证其性质。___________ ,则气密性良好。
(2)装置A中滴加硫酸的仪器名称为___________ 。
(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有___________ (填“还原性”、“氧化性”或“漂白性”)。
(4)试管D中反应的离子方程式为___________ 。
(5)用下图所示装置验证H2SO3酸性比H2CO3强。
a.品红溶液 b.酸性KMnO4溶液 c.饱和NaHCO3溶液 d.饱和NaHSO3溶液
X为___________ ,Y为___________ ,Z为___________ 。
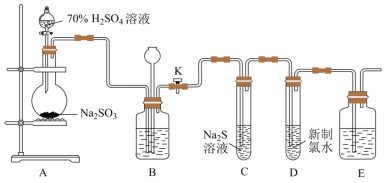
(2)装置A中滴加硫酸的仪器名称为
(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有
(4)试管D中反应的离子方程式为
(5)用下图所示装置验证H2SO3酸性比H2CO3强。
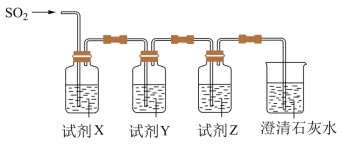
a.品红溶液 b.酸性KMnO4溶液 c.饱和NaHCO3溶液 d.饱和NaHSO3溶液
X为
您最近一年使用:0次
9 . 下列所选仪器或操作符合实验要求的是
| A | B | C | D |
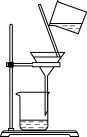 | 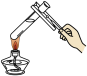 |  | 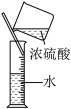 |
| 分离蛋白质胶体和蔗糖溶液 | 给液体加热 | 证明CO2能否溶于水或与NaOH溶液反应 | 稀释浓硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-15更新
|
316次组卷
|
3卷引用:新疆乌鲁木齐八一中学2023-2024学年高一上学期期中考试化学试卷
解题方法
10 . 草酸亚铁晶体( FeC2O4·2H2O,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
I.采用如下装置(可重复选用)进行实验探究纯净草酸亚铁晶体受热分解的产物。

(1)装置D的名称为___________ ,作用是_________________________________ 。
(2)按照气流从左到右的方向,上述装置的连接顺序为a→_____________ →d→e→b→c→尾气处理装置(填仪器接口的小字母编号)。
(3)能证明分解产物中存在CO的现象是_____________________ 。
II.将54.0g草酸亚铁晶体在氮气的氛围中加热分解,得到分解产物的热重曲线(样品质量随温度的变化情况)如图所示:

(4)B点时,固体只含有一种铁的氧化物,则所得固体的化学式为__________ 。
Ⅲ.文献表明:相同条件下,草酸根(C2O )的还原性强于Fe2+。为检验这一结论进行以下实验。
)的还原性强于Fe2+。为检验这一结论进行以下实验。
资料:ⅰ.草酸(H2C2O4)为二元弱酸。
ⅱ.三水三草酸合铁酸钾K3[Fe(C2O4)3]·3H2O为翠绿色晶体,光照易分解。其水溶液中存在:[Fe(C2O4)3] 3− Fe3++ 3C2O
Fe3++ 3C2O K=6.3×10−21
K=6.3×10−21
通过Fe3+和C2O 在溶液中的反应比较Fe2+和C2O
在溶液中的反应比较Fe2+和C2O 的还原性强弱
的还原性强弱
(5)取实验中的少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红。加硫酸后溶液变红的原因是__________________________________ 。
(6)经检验,翠绿色晶体为K3[Fe(C2O4)3]·3H2O。请设计实验,确认实验中没有发生氧化还原反应的操作和现象是_____________ 。
I.采用如下装置(可重复选用)进行实验探究纯净草酸亚铁晶体受热分解的产物。

(1)装置D的名称为
(2)按照气流从左到右的方向,上述装置的连接顺序为a→
(3)能证明分解产物中存在CO的现象是
II.将54.0g草酸亚铁晶体在氮气的氛围中加热分解,得到分解产物的热重曲线(样品质量随温度的变化情况)如图所示:

(4)B点时,固体只含有一种铁的氧化物,则所得固体的化学式为
Ⅲ.文献表明:相同条件下,草酸根(C2O
 )的还原性强于Fe2+。为检验这一结论进行以下实验。
)的还原性强于Fe2+。为检验这一结论进行以下实验。资料:ⅰ.草酸(H2C2O4)为二元弱酸。
ⅱ.三水三草酸合铁酸钾K3[Fe(C2O4)3]·3H2O为翠绿色晶体,光照易分解。其水溶液中存在:[Fe(C2O4)3] 3−
 Fe3++ 3C2O
Fe3++ 3C2O K=6.3×10−21
K=6.3×10−21通过Fe3+和C2O
 在溶液中的反应比较Fe2+和C2O
在溶液中的反应比较Fe2+和C2O 的还原性强弱
的还原性强弱| 操作 | 现象 |
| 在避光处,向10mL0.5mol∙L-1FeCl3溶液中缓慢加入0.5mol∙L-1K2C2O4溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤 | 得到翠绿色溶液和翠绿色晶体 |
(6)经检验,翠绿色晶体为K3[Fe(C2O4)3]·3H2O。请设计实验,确认实验中没有发生氧化还原反应的操作和现象是
您最近一年使用:0次



