名校
1 . AlCl3易水解和升华。二苯甲烷( )是一种重要的有机合成中间体,可通过苯和氯化苄(
)是一种重要的有机合成中间体,可通过苯和氯化苄(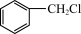 )在一定温度和AlCl3催化下合成二苯甲烷,某化学兴趣小组对二苯甲烷的合成进行实验探究。回答下列问题:已知二苯甲烷常温下为无色针状晶体,沸点为265℃,溶于苯不溶于水;苯的沸点为80.1℃ 。
)在一定温度和AlCl3催化下合成二苯甲烷,某化学兴趣小组对二苯甲烷的合成进行实验探究。回答下列问题:已知二苯甲烷常温下为无色针状晶体,沸点为265℃,溶于苯不溶于水;苯的沸点为80.1℃ 。
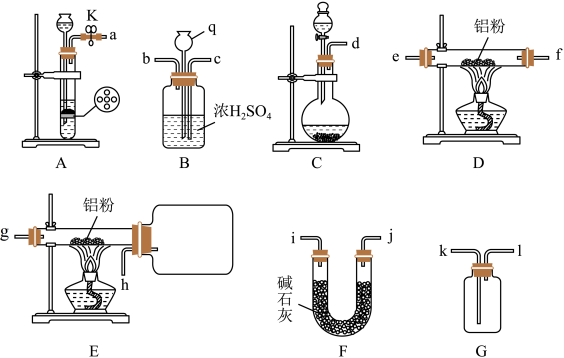
(1)检验装置A的气密性的方法为________ 。
(2)仪器q的名称为_______ ,装置B的作用除干燥气体外,还有_______ 。
(3)选择图中合适的装置,按气流从左到右的方向,合理的连接顺序为_______ (填仪器接口小写字母)。
Ⅱ.合成二苯甲烷。
(4)如图所示,向三颈烧瓶中加入25.0mL苯(ρ=0.87g•cm-3)、20.0mL氯化苄(ρ=1.10g•cm-3)和适量AlCl3,控制温度为80℃左右,回流2h;冷却后依次用水、稀碱液、水洗涤,最后一次水洗的目的为_______ ;再经干燥、_______ 、______ (填操作名称)分离出二苯甲烷。

(5)设计实验证明合成二苯甲烷的反应为取代反应:_______ 。
 )是一种重要的有机合成中间体,可通过苯和氯化苄(
)是一种重要的有机合成中间体,可通过苯和氯化苄( )在一定温度和AlCl3催化下合成二苯甲烷,某化学兴趣小组对二苯甲烷的合成进行实验探究。回答下列问题:已知二苯甲烷常温下为无色针状晶体,沸点为265℃,溶于苯不溶于水;苯的沸点为80.1℃ 。
)在一定温度和AlCl3催化下合成二苯甲烷,某化学兴趣小组对二苯甲烷的合成进行实验探究。回答下列问题:已知二苯甲烷常温下为无色针状晶体,沸点为265℃,溶于苯不溶于水;苯的沸点为80.1℃ 。I.AlCl3的制备。

(1)检验装置A的气密性的方法为
(2)仪器q的名称为
(3)选择图中合适的装置,按气流从左到右的方向,合理的连接顺序为
Ⅱ.合成二苯甲烷。
(4)如图所示,向三颈烧瓶中加入25.0mL苯(ρ=0.87g•cm-3)、20.0mL氯化苄(ρ=1.10g•cm-3)和适量AlCl3,控制温度为80℃左右,回流2h;冷却后依次用水、稀碱液、水洗涤,最后一次水洗的目的为

(5)设计实验证明合成二苯甲烷的反应为取代反应:
您最近一年使用:0次
名校
2 . 苯甲酸是一种重要原料。实验室可以用甲苯与高锰酸钾反应制得苯甲酸,反应装置图和有关数据如下:
合成步骤如下:
①在三颈烧瓶中加入5.4mL甲苯和30mL稀硫酸,放入碎瓷片,加热至沸腾时迅速加入12.8g高锰酸钾固体,继续加热到甲苯层消失,过滤;
②反应后的溶液仍呈紫色,在容器中加入适量亚硫酸氢钠溶液,振荡,直到溶液变为无色,搅拌下向容器中加入足量浓盐酸;待反应完全后,将反应容器放在冰水浴中冷却,析出晶体,过滤,洗涤,干燥,称量。
(1)仪器A的名称是_____ ,它的作用是_____ 。
(2)加入碎瓷片的作用是_____ 。
(3)加入亚硫酸氢钠溶液使紫色褪去时发生反应的离子方程式为_____ 。
(4)若得到的苯甲酸晶体产品不纯,则采用_____ 方法可得到纯度更高的产品,提纯过程中趁热过滤的目的是_____ 。
(5)下列有关苯甲酸提纯实验的说法正确的是_____ (填字母)。
A.粗苯甲酸溶解过程中,加热、玻璃棒搅拌均能提高苯甲酸的溶解度
B.在苯甲酸提纯实验中,粗苯甲酸加热溶解后还需加少量蒸馏水
C.冷却结晶时,温度过低将析出杂质,故此时温度不是越低越好
(6)若最后得到纯净的苯甲酸质量为4.0g,则该反应的产率是_____ (保留一位小数)。

| 物质 | 熔点/℃ | 沸点℃ | 水中溶解度/g(25℃) | 相对分子质量/ | 密度/( ) ) |
| 甲苯 | -94.9 | 110.6 | 难溶 | 92 | 0.85 |
| 苯甲酸 | 122.13 | 249 | 0.344 | 122 | 1.27 |
①在三颈烧瓶中加入5.4mL甲苯和30mL稀硫酸,放入碎瓷片,加热至沸腾时迅速加入12.8g高锰酸钾固体,继续加热到甲苯层消失,过滤;
②反应后的溶液仍呈紫色,在容器中加入适量亚硫酸氢钠溶液,振荡,直到溶液变为无色,搅拌下向容器中加入足量浓盐酸;待反应完全后,将反应容器放在冰水浴中冷却,析出晶体,过滤,洗涤,干燥,称量。
已知:
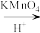
 。
。
(1)仪器A的名称是
(2)加入碎瓷片的作用是
(3)加入亚硫酸氢钠溶液使紫色褪去时发生反应的离子方程式为
(4)若得到的苯甲酸晶体产品不纯,则采用
(5)下列有关苯甲酸提纯实验的说法正确的是
A.粗苯甲酸溶解过程中,加热、玻璃棒搅拌均能提高苯甲酸的溶解度
B.在苯甲酸提纯实验中,粗苯甲酸加热溶解后还需加少量蒸馏水
C.冷却结晶时,温度过低将析出杂质,故此时温度不是越低越好
(6)若最后得到纯净的苯甲酸质量为4.0g,则该反应的产率是
您最近一年使用:0次
3 . 己二酸是合成尼龙-66的主要原料之一。实验室合成己二酸的原理、有关数据及装置示意图如下:3 +8HNO3—→ 3
+8HNO3—→ 3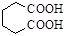 +8NO↑+7H2O
+8NO↑+7H2O

实验步骤如下:
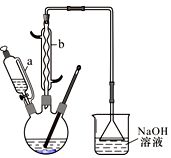
Ⅰ.在三口烧瓶中加入16 mL 50%的硝酸(密度为1.31 g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
Ⅱ.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60 ℃~65 ℃之间。
Ⅲ.当环己醇全部加入后,将混合物用80 ℃~90 ℃水浴加热约10 min(注意控制温度),直至无红棕色气体生成为止。
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重。
请回答下列问题:
(1)装置b的名称为__________ ,使用时要从_____ (填“上口”或“下口”)通入冷水;滴液漏斗的细支管a的作用是_______
(2)本实验所用50%的硝酸的物质的量浓度为_______ ;实验中,氮氧化物废
气(主要成分为NO2和NO)可以用NaOH溶液来吸收,其主要反应为:
2NO2+2NaOH=NaNO2+NaNO3+H2O和NO+NO2+2NaOH=2NaNO2+H2O
其中NaOH溶液可以用Na2CO3溶液来替代,请模仿上述反应,写出Na2CO3溶液吸收的两个方程式:
_______________________________________ ;_________________________
(3)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是__________________ 。
(4)为了除去可能的杂质和减少产品损失,可用_________ 洗涤晶体。
 +8HNO3—→ 3
+8HNO3—→ 3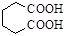 +8NO↑+7H2O
+8NO↑+7H2O
实验步骤如下:

Ⅰ.在三口烧瓶中加入16 mL 50%的硝酸(密度为1.31 g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
Ⅱ.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60 ℃~65 ℃之间。
Ⅲ.当环己醇全部加入后,将混合物用80 ℃~90 ℃水浴加热约10 min(注意控制温度),直至无红棕色气体生成为止。
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重。
请回答下列问题:
(1)装置b的名称为
(2)本实验所用50%的硝酸的物质的量浓度为
气(主要成分为NO2和NO)可以用NaOH溶液来吸收,其主要反应为:
2NO2+2NaOH=NaNO2+NaNO3+H2O和NO+NO2+2NaOH=2NaNO2+H2O
其中NaOH溶液可以用Na2CO3溶液来替代,请模仿上述反应,写出Na2CO3溶液吸收的两个方程式:
(3)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是
(4)为了除去可能的杂质和减少产品损失,可用
您最近一年使用:0次



