1 . 下列实验装置不能达到实验目的的是
| A | B | C | D |
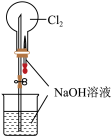 |  | 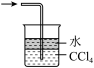 | 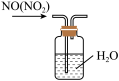 |
| “喷泉实验” | 制备并收集少量氨气 | 吸收氨气,且防止倒吸 | 除去NO中的NO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-03更新
|
311次组卷
|
2卷引用:湖北省仙桃市 2022-2023学年高一下学期3月调研化学试题
解题方法
2 . 用下列实验装置进行相应实验,能达到实验目的的是
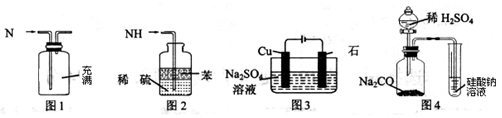

| A.用图1所示装置可收集NO气体 |
| B.用图4装置可证明酸性:H2SO4>H2CO3>H2SiO3 |
C.用图3所示装置可实现反应:2H2O O2↑+2H2↑ O2↑+2H2↑ |
| D.用图2所示装置可吸收多余氨气且能防止倒吸 |
您最近一年使用:0次
2016-12-09更新
|
145次组卷
|
2卷引用:2015届湖北省七市(州)教科研协作体4月高三联合考试理综化学试卷
名校
解题方法
3 . 某学习小组设计如图所示装置改进钠与氯气反应的实验。下列说法正确的是
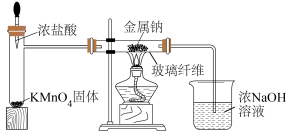

| A.可用MnO2代替KMnO4固体 | B.先点燃酒精灯再滴加浓盐酸 |
| C.钠在氯气中剧烈燃烧产生白烟 | D.实验过程会出现倒吸现象 |
您最近一年使用:0次
2023-09-14更新
|
359次组卷
|
3卷引用:湖北省高中名校联盟2024届高三第一次联合测评化学试题
名校
解题方法
4 . 某兴趣小组用CaS与MgCl2反应制备高纯H2S,实验装置如图所示(装置A内产生的H2S气体中含有酸性气体杂质)不正确 的是
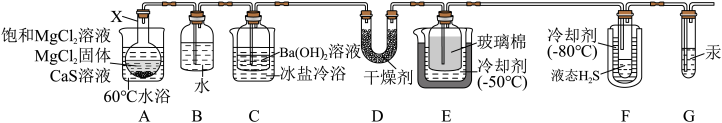
| A.装置A中的反应利用了水解原理 |
| B.为了简化装置,B可以省略 |
| C.装置C中的Ba(OH)2可以换成NaHS |
| D.为了快速排除体系内的空气,可先断开装置F和装置G的连接 |
您最近一年使用:0次
2024-04-10更新
|
583次组卷
|
4卷引用:2024届湖北省荆州中学高三下学期第三次适应性考试化学试卷
2024届湖北省荆州中学高三下学期第三次适应性考试化学试卷浙江省杭州市2024届高三下学期二模化学试题(已下线)压轴题03?物质的制备、检验、分离与提纯(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)(已下线)压轴题03 物质的制备检验分离与提纯(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
5 . 四氯化锡( )是一种重要的化工原料,主要用于有机锡化合物的制造,可由锡单质与氯气在加热时化合生成,某实验小组用如下装置对其进行制备。
)是一种重要的化工原料,主要用于有机锡化合物的制造,可由锡单质与氯气在加热时化合生成,某实验小组用如下装置对其进行制备。
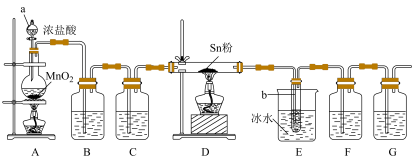
【相关药品性质】
回答下列问题:
(1)“仪器a”的名称是___________ ,A中反应的离子方程式为___________ 。
(2)实验前应进行的操作是___________ ,实验开始时,应先点燃___________ (填“A”或“D”)处的酒精灯。
(3)若无“洗气瓶B”,可能会导致的问题是___________ 。
(4)“装置E”中使用冰水浴的目的是___________ 。实验结束后,“小试管b”内收集到的液体呈淡黄色,其原因是___________ 。
(5)“洗气瓶F”中所盛放的药品是___________ 。
 )是一种重要的化工原料,主要用于有机锡化合物的制造,可由锡单质与氯气在加热时化合生成,某实验小组用如下装置对其进行制备。
)是一种重要的化工原料,主要用于有机锡化合物的制造,可由锡单质与氯气在加热时化合生成,某实验小组用如下装置对其进行制备。
【相关药品性质】
| 药品 | 颜色、状态 | 熔点(℃) | 沸点(℃) | 其他性质 |
| Sn | 银白色固体 | 231 | 2260 | 较活泼金属能与 、HCl等气体发生反应 、HCl等气体发生反应 |
 | 无色液体 | -33 | 114 | 极易与水反应产生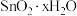 溶胶 溶胶 |
(1)“仪器a”的名称是
(2)实验前应进行的操作是
(3)若无“洗气瓶B”,可能会导致的问题是
(4)“装置E”中使用冰水浴的目的是
(5)“洗气瓶F”中所盛放的药品是
您最近一年使用:0次
6 . 氮元素的单质和常见化合物在工、农业生产中用途广泛。
(1)氮气的化学性质很稳定,可用作灯泡填充气。从分子结构角度解释其原因是_______ 。
(2)N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式_______ 。
(3)NO和NO2可用NaOH溶液吸收主要反应为:
NO+NO2+2OH-=2NO +H2O
+H2O
2OH-+2NO2=NO +NO
+NO +H2O
+H2O
①下列措施可能提高尾气中NO和NO2去除率的有_______ (填字母)
A.加快通入尾气的速率。
B.采用气,液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
D.在尾气中同时通入氧气
②吸收后的溶液经浓缩,结晶,过滤,得到NaNO2晶体,该晶体的主要杂质_______ (填化学式)。
(4)铵盐大多在农业上用作化肥,实验室可用固体NH4Cl与固体Ca(OH)2加热反应来制备氨气,其化学方程式为_______ 。欲吸收尾气中的NH3,下列装置不宜选用_______ (填字母) 。(已知氨气难溶于有机溶剂CCl4)
A.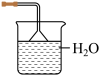 B.
B.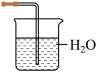 C.
C.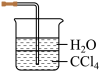 D.
D.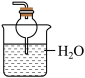
(1)氮气的化学性质很稳定,可用作灯泡填充气。从分子结构角度解释其原因是
(2)N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式
(3)NO和NO2可用NaOH溶液吸收主要反应为:
NO+NO2+2OH-=2NO
 +H2O
+H2O2OH-+2NO2=NO
 +NO
+NO +H2O
+H2O①下列措施可能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率。
B.采用气,液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
D.在尾气中同时通入氧气
②吸收后的溶液经浓缩,结晶,过滤,得到NaNO2晶体,该晶体的主要杂质
(4)铵盐大多在农业上用作化肥,实验室可用固体NH4Cl与固体Ca(OH)2加热反应来制备氨气,其化学方程式为
A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
7 . 某学习小组设计实验制备供氢剂氢化钠(NaH),实验装置如下图所示。

下列说法错误的是

下列说法错误的是
| A.相同条件下,粗锌比纯锌反应速率快 |
| B.装置a还能用来制备CO2和H2S气体 |
| C.实验时先打开活塞K,再点燃c处酒精灯 |
| D.判断钠是否剩余,可取c中固体加水检验 |
您最近一年使用:0次
名校
解题方法
8 . 草酸中滴加浓H2SO4可以制备CO。
H2C2O4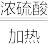 CO2+CO+H2O
CO2+CO+H2O
现拟用CO和Fe2O3(粉)做一个炼铁的实验。CO气体中的杂质气体必须首先除去。现在如图所示装置:
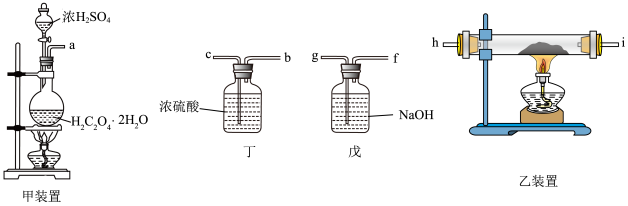
回答下列问题:
(1)请按你的设计方案,把装置正确连接(用管口小写字母表示连接的顺序):__ 。
(2)用A~F正确表示实验操作的先后顺序__ 。
A.点燃甲装置的酒精灯,打开分液漏斗,调节浓H2SO4的滴加速度;
B.点燃乙装置中的酒精灯,加热氧化铁;
C.检查整套装置的气密性;
D.在导口i处连接橡皮管,把排气通入通风厨内;
E.当乙装置玻璃管内的氧化铁变黑时,熄灭乙装置中的酒精灯;
F.关好甲装置中分液漏斗的开关后,再熄灭该装置中的酒精灯。
(3)丁装置的作用是__ 。
(4)导管口i流出的气体通入通风厨并非是好办法,其原因是__ ,简单且有效的方法是__ 。
H2C2O4
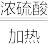 CO2+CO+H2O
CO2+CO+H2O现拟用CO和Fe2O3(粉)做一个炼铁的实验。CO气体中的杂质气体必须首先除去。现在如图所示装置:

回答下列问题:
(1)请按你的设计方案,把装置正确连接(用管口小写字母表示连接的顺序):
(2)用A~F正确表示实验操作的先后顺序
A.点燃甲装置的酒精灯,打开分液漏斗,调节浓H2SO4的滴加速度;
B.点燃乙装置中的酒精灯,加热氧化铁;
C.检查整套装置的气密性;
D.在导口i处连接橡皮管,把排气通入通风厨内;
E.当乙装置玻璃管内的氧化铁变黑时,熄灭乙装置中的酒精灯;
F.关好甲装置中分液漏斗的开关后,再熄灭该装置中的酒精灯。
(3)丁装置的作用是
(4)导管口i流出的气体通入通风厨并非是好办法,其原因是
您最近一年使用:0次
9 . 无水溴化镁常常做催化剂。选用如图所示装置(夹持装置略)采用镁屑与液溴为原料制备无水MgBr2。

已知:
(1)乙醚的熔点为34.6℃,沸点为132℃。
(2)Mg和Br2剧烈反应,放出大量的热;MgBr2具有强吸水性;MgBr2能与乙醚发生反应MgBr2+3C2H5OC2H5→MgBr2•3C2H5OC2H5。
实验主要步骤如下:
Ⅰ.选用上述部分装置,正确连接,检查装置的气密性。向装置中加入药品。
Ⅱ.加热装置A,迅速升温至140℃,并保持140℃加热一段时间,停止加热。
Ⅲ.通入干燥的氮气,让液溴缓慢进入装置B中,直至完全加入。
IV.装置B中反应完毕后恢复至室温,过滤反应物,将得到的滤液转移至干燥的烧瓶中,在冰水中冷却,析出晶体,再过滤得三乙醚合溴化镁粗产品。
V.用苯洗涤粗产品,减压过滤,得三乙醚合溴化镁,将其加热至160℃分解得无水MgBr2。回答下列问题:
(1)步骤I中所选装置的正确连接顺序是a___ (填小写字母)。装置D的作用是___ 。
(2)装置A中使用仪器m的优点是___ 。
(3)若加热装置A一段时间后发现忘记加入碎瓷片,应该采取的正确操作是___ 。
(4)步骤V中用苯洗涤三乙醚合溴化镁的目的是___ 。
(5)步骤V采用减压过滤(使容器内压强降低,以达到固液快速分离)。下列装置可用作减压过滤的是___ (填序号)。

(6)实验中若温度控制不当,装置B中会产生CH2Br—CH2Br。请说明原因___ 。

已知:
(1)乙醚的熔点为34.6℃,沸点为132℃。
(2)Mg和Br2剧烈反应,放出大量的热;MgBr2具有强吸水性;MgBr2能与乙醚发生反应MgBr2+3C2H5OC2H5→MgBr2•3C2H5OC2H5。
实验主要步骤如下:
Ⅰ.选用上述部分装置,正确连接,检查装置的气密性。向装置中加入药品。
Ⅱ.加热装置A,迅速升温至140℃,并保持140℃加热一段时间,停止加热。
Ⅲ.通入干燥的氮气,让液溴缓慢进入装置B中,直至完全加入。
IV.装置B中反应完毕后恢复至室温,过滤反应物,将得到的滤液转移至干燥的烧瓶中,在冰水中冷却,析出晶体,再过滤得三乙醚合溴化镁粗产品。
V.用苯洗涤粗产品,减压过滤,得三乙醚合溴化镁,将其加热至160℃分解得无水MgBr2。回答下列问题:
(1)步骤I中所选装置的正确连接顺序是a
(2)装置A中使用仪器m的优点是
(3)若加热装置A一段时间后发现忘记加入碎瓷片,应该采取的正确操作是
(4)步骤V中用苯洗涤三乙醚合溴化镁的目的是
(5)步骤V采用减压过滤(使容器内压强降低,以达到固液快速分离)。下列装置可用作减压过滤的是

(6)实验中若温度控制不当,装置B中会产生CH2Br—CH2Br。请说明原因
您最近一年使用:0次
名校
解题方法
10 . 乙酰苯胺(C6H5-NHCOCH3)可用作止痛剂退热剂、防腐剂和染料中间体,常用苯胺(C6H5-NH2)与冰醋酸为原料制备,具体流程如下:
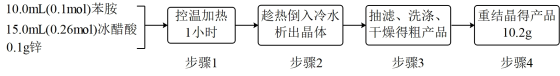
化学原理:C6H5-NH2 + CH3COOH C6H5–NHCOCH3+ H2O,已知:①苯胺易被氧化,乙酰苯胺碱性条件下水解;②部分物质有关性质如下表;③步骤1所用装置如图所示(固定装置、加热装置已略去)。
C6H5–NHCOCH3+ H2O,已知:①苯胺易被氧化,乙酰苯胺碱性条件下水解;②部分物质有关性质如下表;③步骤1所用装置如图所示(固定装置、加热装置已略去)。
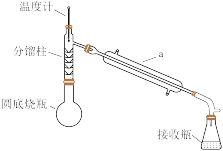
请回答下列问题:
(1)仪器a的名称___________
(2)盛有冰醋酸的容器,最有可能贴有的安全标签是___________ (填标号)。
a. b.
b.  c.
c. d.
d.
(3)加入锌粒,除了防止暴沸外,还能起到的作用是___________
(4)步骤1中控制温度计示数约105 °C的原因是___________
(5)判断反应基本完全的现象是___________ ;步骤3中洗涤乙酰苯胺粗产品最合适的试剂是___________ (填标号)。
a.冰水 b.热水 c.15%的乙醇溶液 d. NaOH溶液
(6)步骤4中重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→___________ →冷却结晶→过滤→洗涤→干燥。
(7)本实验中乙酰苯胺产率为___________ 。

化学原理:C6H5-NH2 + CH3COOH
 C6H5–NHCOCH3+ H2O,已知:①苯胺易被氧化,乙酰苯胺碱性条件下水解;②部分物质有关性质如下表;③步骤1所用装置如图所示(固定装置、加热装置已略去)。
C6H5–NHCOCH3+ H2O,已知:①苯胺易被氧化,乙酰苯胺碱性条件下水解;②部分物质有关性质如下表;③步骤1所用装置如图所示(固定装置、加热装置已略去)。
名称 | 熔点/℃ | 沸点/℃ | 溶解度/g(20℃) | |
水 | 乙醇 | |||
苯胺 | -6.3 | 184 | 3.4 | 任意比混合 |
冰醋酸 | 16.6 | 118 | 任意比混合 | 任意比混合 |
乙酰苯胺 | 114.3 | 304 | 0.46 | 36.9 |
(温度高溶解度大) | ||||
(1)仪器a的名称
(2)盛有冰醋酸的容器,最有可能贴有的安全标签是
a.
 b.
b.  c.
c. d.
d.
(3)加入锌粒,除了防止暴沸外,还能起到的作用是
(4)步骤1中控制温度计示数约105 °C的原因是
(5)判断反应基本完全的现象是
a.冰水 b.热水 c.15%的乙醇溶液 d. NaOH溶液
(6)步骤4中重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→
(7)本实验中乙酰苯胺产率为
您最近一年使用:0次
2021-06-01更新
|
290次组卷
|
4卷引用:湖北省武汉市2020届高三毕业生六月供题(二)理科综合化学试题
湖北省武汉市2020届高三毕业生六月供题(二)理科综合化学试题广东省中山市华南师范大学中山附属中学2020-2021学年高二下学期第二次月考化学试题福建省莆田二中、晋江一中、南安一中2019-2020学年高二下学期三校期末联考化学试题(已下线)考点29 试剂存放与实验安全-备战2022年高考化学一轮复习考点帮(浙江专用)



