23-24高三下·四川成都·开学考试
名校
解题方法
1 . 葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过如下实验流程制得:
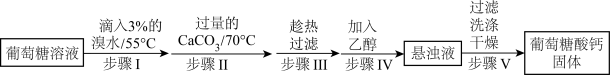
已知:a.反应原理: 。
。
b.相关物质的溶解性如下表:
c.相关物质的酸性:氢溴酸>葡萄糖酸>碳酸。
回答下列问题:
(1)步骤I中溴水氧化葡萄糖时采用了如图所示反应装置,你认为缺少的仪器是___________ ,恒压滴液漏斗使用时需要打开的活塞或玻璃塞是___________ (填“a”“b”或“a和b”)。烧杯中 溶液水浴的作用是
溶液水浴的作用是___________ 。
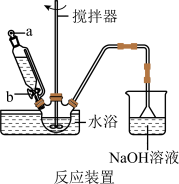
(2)制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是___________(填序号)。
(3)步骤Ⅱ中加入过量的 ,生成葡萄糖酸钙的化学方程式为
,生成葡萄糖酸钙的化学方程式为___________ 。加入过量的 除了能提高葡萄糖酸的转化率,还有的作用是
除了能提高葡萄糖酸的转化率,还有的作用是___________ 。
(4)洗涤操作中最合适的洗涤剂是___________ (填序号),理由是___________ 。
A.冷水 B.热水 C.乙醇
(5)利用重结晶法可除去葡萄糖酸钙粗品中的杂质,提高产品的质量,选出葡萄糖酸钙重结晶过程中合理的操作并排序:___________ (填序号,操作步骤不可重复使用)。
①蒸发浓缩至溶液表面出现晶膜
②待晶体充分析出后,减压过滤
③将滤液冷却至室温,加入 95%的乙醇溶液并搅拌,促进晶体析出
95%的乙醇溶液并搅拌,促进晶体析出
④趁热减压过滤,除去不溶物
⑤在50℃下用恒温干燥箱烘干,称重
⑥取烧杯加入 蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液

已知:a.反应原理:
 。
。b.相关物质的溶解性如下表:
| 物质的名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 |
| 在水中的溶解性 | 可溶于冷水,易溶于热水 | 可溶 | 极易溶 |
| 在乙醇中的溶解性 | 微溶 | 微溶 | 可溶 |
回答下列问题:
(1)步骤I中溴水氧化葡萄糖时采用了如图所示反应装置,你认为缺少的仪器是
 溶液水浴的作用是
溶液水浴的作用是
(2)制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是___________(填序号)。
A.新制 悬浊液 悬浊液 | B.酸性 溶液 溶液 |
C. /葡萄糖氧化酶 /葡萄糖氧化酶 | D. 溶液 溶液 |
(3)步骤Ⅱ中加入过量的
 ,生成葡萄糖酸钙的化学方程式为
,生成葡萄糖酸钙的化学方程式为 除了能提高葡萄糖酸的转化率,还有的作用是
除了能提高葡萄糖酸的转化率,还有的作用是(4)洗涤操作中最合适的洗涤剂是
A.冷水 B.热水 C.乙醇
(5)利用重结晶法可除去葡萄糖酸钙粗品中的杂质,提高产品的质量,选出葡萄糖酸钙重结晶过程中合理的操作并排序:
①蒸发浓缩至溶液表面出现晶膜
②待晶体充分析出后,减压过滤
③将滤液冷却至室温,加入
 95%的乙醇溶液并搅拌,促进晶体析出
95%的乙醇溶液并搅拌,促进晶体析出④趁热减压过滤,除去不溶物
⑤在50℃下用恒温干燥箱烘干,称重
⑥取烧杯加入
 蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
您最近一年使用:0次
2 . 粗盐提纯实验的科学探究。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为___________ (填序号)。
(2)仪器B的名称是___________ ,在实验中三个步骤中都须使用的一种仪器是___________ (填序号)。

Ⅱ.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。
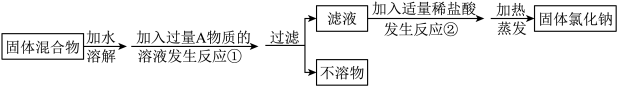
(3)写出A物质的化学式:___________ 。
(4)写出反应②的化学方程式:___________ 。
(5)反应①中加入过量A物质的目的是___________ ;反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度___________ (填“有”或“没有”)影响。
(6)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果___________ (填增大、不变或减少)。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为
(2)仪器B的名称是

Ⅱ.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。

(3)写出A物质的化学式:
(4)写出反应②的化学方程式:
(5)反应①中加入过量A物质的目的是
(6)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果
您最近一年使用:0次
23-24高三上·甘肃金昌·阶段练习
名校
3 . 青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157 ℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35 ℃。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工艺如下图所示:

各步骤所需选用的实验仪器如下:

请回答下列问题:
(1)采用乙醚浸取法的原因①是利用___________ 的化学原理,②乙醚___________ ,能避免青蒿素在高温下分解。
(2)操作Ⅰ需要的主要玻璃仪器有___________ (填序号),操作Ⅱ的名称是___________ 。
(3)操作Ⅲ的主要过程可能是___________ (填字母)。
A.加水溶解,蒸发浓缩、冷却结
B.加入乙醚进行萃取分液
C.加95%的乙醇,浓缩、结晶、过滤
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2 g青蒿素样品放在硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。

①装置E中盛放的物质是___________ (填字母,下同),装置F中盛放的物质是___________ 。
a.浓硫酸 b.无水CaCl2 c.胆矾 d.碱石灰
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是___________ 。
③用合理改进后的装置进行实验,称得:
则测得青蒿素的最简式是___________ 。
(5)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与___________(填字母)具有相同的性质。

各步骤所需选用的实验仪器如下:

请回答下列问题:
(1)采用乙醚浸取法的原因①是利用
(2)操作Ⅰ需要的主要玻璃仪器有
(3)操作Ⅲ的主要过程可能是
A.加水溶解,蒸发浓缩、冷却结
B.加入乙醚进行萃取分液
C.加95%的乙醇,浓缩、结晶、过滤
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2 g青蒿素样品放在硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。

①装置E中盛放的物质是
a.浓硫酸 b.无水CaCl2 c.胆矾 d.碱石灰
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是
③用合理改进后的装置进行实验,称得:
| 装置 | 实验前/g | 实验后/g |
| E | 22.6 | 42.4 |
| F | 80.2 | 146.2 |
(5)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与___________(填字母)具有相同的性质。
| A.乙酸乙酯 | B.乙酸 | C.乙醇 | D.葡萄糖 |
您最近一年使用:0次
22-23高二下·山东日照·期末
名校
解题方法
4 . 某化学兴趣小组设计了研究溴苯制备原理并检验产物的实验,部分物质数据如下:苯密度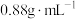 ,沸点
,沸点 ℃:溴苯密度
℃:溴苯密度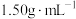 ,沸点
,沸点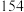 ℃。请回答下列问题:
℃。请回答下列问题:
I.粗溴苯的制备
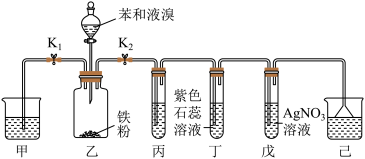
按如图所示的装置连接好各仪器,经检查气密性良好后,加入相应试剂。_______ 。
(2)溴苯的制备需在无水条件下进行,原因是_______ 。
(3)装置丙中应该盛装_______ (填试剂名称)。能够证明该反应为取代反应的实验现象为_______ ;若撤去装置丙,_______ (填“能”或“不能”)证明该反应为取代反应。
Ⅱ.溴苯的精制如下图所示: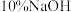 溶液洗涤时,反应的离子方程式为
溶液洗涤时,反应的离子方程式为_______ 。
(5)有机层Ⅲ经干燥后分离出纯净溴苯的操作为_______ (填操作名称)。
(6)若实验时使用 苯,最终精制得到
苯,最终精制得到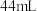 溴苯,则溴苯的产率为
溴苯,则溴苯的产率为_______ (保留两位有效数字)。
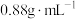 ,沸点
,沸点 ℃:溴苯密度
℃:溴苯密度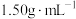 ,沸点
,沸点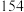 ℃。请回答下列问题:
℃。请回答下列问题:I.粗溴苯的制备
按如图所示的装置连接好各仪器,经检查气密性良好后,加入相应试剂。
(2)溴苯的制备需在无水条件下进行,原因是
(3)装置丙中应该盛装
Ⅱ.溴苯的精制如下图所示:
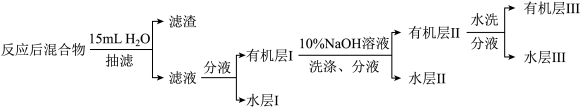
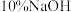 溶液洗涤时,反应的离子方程式为
溶液洗涤时,反应的离子方程式为(5)有机层Ⅲ经干燥后分离出纯净溴苯的操作为
(6)若实验时使用
 苯,最终精制得到
苯,最终精制得到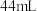 溴苯,则溴苯的产率为
溴苯,则溴苯的产率为
您最近一年使用:0次
2023-07-12更新
|
546次组卷
|
3卷引用:第二章 烃(A卷)
21-22高一下·全国·课时练习
解题方法
5 . I.回答下列问题
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
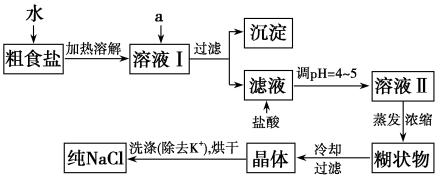
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO ,选出a所代表的试剂,按滴加顺序依次为
,选出a所代表的试剂,按滴加顺序依次为___________ (只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为___________ 。
Ⅱ.工业上用活性炭吸附海带提碘后废水中的I-制取I2,其流程如图:
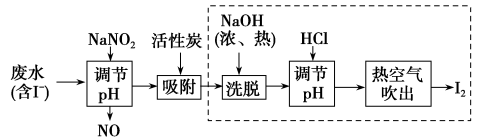
(2)向废水中加入NaNO2并调节pH<4,写出此反应的离子方程式:___________ 。
(3)写出该流程加入HCl调节pH发生的反应的离子方程式:___________ 。
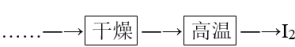
(4)工业上虚线框内流程还可用下图操作代替,试评价图中替代流程的优点:___________ (写出一条即可)。
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO
 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO
 ,选出a所代表的试剂,按滴加顺序依次为
,选出a所代表的试剂,按滴加顺序依次为②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为
Ⅱ.工业上用活性炭吸附海带提碘后废水中的I-制取I2,其流程如图:

(2)向废水中加入NaNO2并调节pH<4,写出此反应的离子方程式:
(3)写出该流程加入HCl调节pH发生的反应的离子方程式:
(4)工业上虚线框内流程还可用下图操作代替,试评价图中替代流程的优点:

您最近一年使用:0次
20-21高一下·江苏南通·期中
名校
解题方法
6 . 海带中含有碘元素。从海带中提取碘的实验过程如下图所示,下列说法正确的是
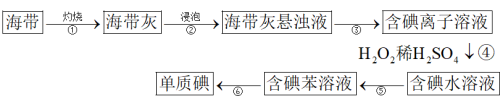

| A.步骤①主要在蒸发皿中进行 |
B.步骤④的离子方程式为 |
| C.步骤⑤中,先从分液漏斗下口放出水,再从下口放出含碘苯溶液 |
| D.步骤⑥的操作为蒸馏 |
您最近一年使用:0次
2021-05-06更新
|
449次组卷
|
7卷引用:第八章 化学与可持续发展【单元测试A卷】
(已下线)第八章 化学与可持续发展【单元测试A卷】(已下线)第八章 化学与可持续发展(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)江苏省南通市启东市、通州区2020-2021学年高一下学期期中联考化学试题(已下线)专题11 自然资源的开发利用【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)江苏省盐城市伍佑中学2021-2022学年高一下学期期中考试化学(选修)试题(已下线)8.1.1 金属矿物和海水资源的开发利用-2021-2022学年高一化学课后培优练(人教版2019必修第二册)(已下线)第13练 自然资源的开发利用-2022年【暑假分层作业】高一化学(人教版2019必修第二册)



