解题方法
1 . 利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等)制取草酸钴的工艺流程如下:
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)为增大水钴矿的浸取效率,可采取的措施为______ 。(任写一条)
(2)向浸出液中加入NaClO3对应的离子反应方程式为______ ,制取NaClO3可以将氯气通入到热的浓氢氧化钠溶液,该反应的离子方程式为______ ;实验需要制取21.3克NaClO3,需要的氯气由电解食盐水生成,若不考虑反应过程中的损失,则同时生成的氢气的体积为______ (标准状况)。
(3)向浸出液中加入碳酸钠后析出的沉淀是______ ,至少调节pH为______ 。
(4)滤液Ⅱ中加入萃取剂的目的是______ 。
(5)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液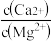 =
=______ 。
(6)取15gCoC2O4样品灼烧(CoC2O4=CoO+CO+CO2,假设杂质不参与变化),将分解产生的气体收集起来得到标况下体积为4.48L的气体,则CoC2O4的纯度为_______ 。
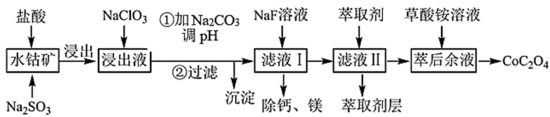
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)为增大水钴矿的浸取效率,可采取的措施为
(2)向浸出液中加入NaClO3对应的离子反应方程式为
(3)向浸出液中加入碳酸钠后析出的沉淀是
(4)滤液Ⅱ中加入萃取剂的目的是
(5)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液
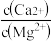 =
=(6)取15gCoC2O4样品灼烧(CoC2O4=CoO+CO+CO2,假设杂质不参与变化),将分解产生的气体收集起来得到标况下体积为4.48L的气体,则CoC2O4的纯度为
您最近一年使用:0次
解题方法
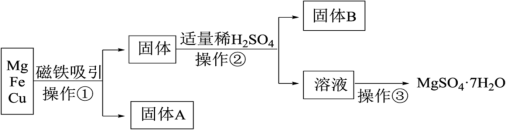
2 . 有Mg、Fe、Cu的混合粉末,分离得到MgSO4·7H2O过程如下:___________ 。
(2)操作②的名称是___________ ,需要用到的主要玻璃仪器有 ___________ 、玻璃棒,其中玻璃棒的作用是___________ 。
(3)操作②发生的离子反应方程式为___________ ,属于___________ 反应。(填基本反应类型)
(4)实验中可选用适量的下列试剂中的代替稀H2SO4___________ (填标号)。
A. CuSO4溶液 B.FeSO4溶液 C.稀盐酸
(5)操作③主要包含蒸发浓缩、___________ 、过滤、洗涤烘干等。
(2)操作②的名称是
(3)操作②发生的离子反应方程式为
(4)实验中可选用适量的下列试剂中的代替稀H2SO4
A. CuSO4溶液 B.FeSO4溶液 C.稀盐酸
(5)操作③主要包含蒸发浓缩、
您最近一年使用:0次
解题方法
3 . 除去下列物质中的杂质,所用试剂和方法正确的是
| 选项 | 物质 | 杂质 | 除杂质所用试剂(过量) | 操作方法 |
| ① | 铝粉 | 铁粉 | NaOH 溶液 | 过滤 |
| ② | KNO3溶液 | K2SO4 | Ba(NO3)2 溶液 | 过滤 |
| ③ | Cl2 | HCl | 饱和 NaCl 溶液、浓硫酸 | 洗气 |
| ④ | FeCl3 | CuCl2 | 铁屑 | 过滤 |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
解题方法
4 . 氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业氧化锌[含有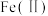 、
、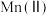 、
、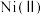 等杂质]的流程如下
等杂质]的流程如下


已知:①在本实验条件下,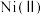 不能被氧化;高锰酸钾的还原产物是
不能被氧化;高锰酸钾的还原产物是 。
。
②不考虑操作过程中引起的质量损失。
回答下列问题:
(1)加稀硫酸酸浸时,常将工业 粉碎,其目的是
粉碎,其目的是_____ 。
(2)过滤时,主要用到的玻璃仪器有烧杯、玻璃棒和________ ,其中玻璃棒的作用为_________ 。
(3)②发生反应的离子方程式有 和
和________ 。
(4)若④中产物仅为 ,则发生反应的离子方程式为
,则发生反应的离子方程式为________ ;取干燥后的滤饼 ,煅烧后可得到产品(
,煅烧后可得到产品( )
) ,则
,则 等于
等于_____ (用含a、m的代数式表示)。
(5)④形成的沉淀要水洗,检验沉淀是否洗涤干净的操作和现象是________ 。
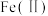 、
、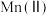 、
、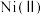 等杂质]的流程如下
等杂质]的流程如下

已知:①在本实验条件下,
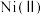 不能被氧化;高锰酸钾的还原产物是
不能被氧化;高锰酸钾的还原产物是 。
。②不考虑操作过程中引起的质量损失。
回答下列问题:
(1)加稀硫酸酸浸时,常将工业
 粉碎,其目的是
粉碎,其目的是(2)过滤时,主要用到的玻璃仪器有烧杯、玻璃棒和
(3)②发生反应的离子方程式有
 和
和(4)若④中产物仅为
 ,则发生反应的离子方程式为
,则发生反应的离子方程式为 ,煅烧后可得到产品(
,煅烧后可得到产品( )
) ,则
,则 等于
等于(5)④形成的沉淀要水洗,检验沉淀是否洗涤干净的操作和现象是
您最近一年使用:0次
解题方法
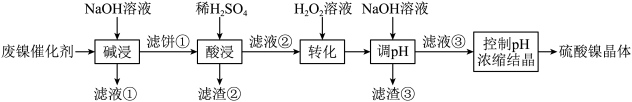
5 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体( ):
):
回答下列问题:
(1)“碱浸”中NaOH溶液可以有效地除去金属铝及其氧化物,写出NaOH溶液除去铝单质的离子方程式___________ 。
(2)“滤液②”中含有的金属离子有Fe2+和___________ ,检验Fe2+的试剂是铁氰化钾溶液,写出Fe2+和铁氰化钾溶液反应的离子方程式___________ 。
(3)利用上述表格数据,计算 的
的
___________ (写出计算结果)。如果“转化”后的溶液中 浓度为
浓度为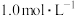 ,则“调pH”应控制的pH范围是
,则“调pH”应控制的pH范围是___________ 。
(4)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的 。写出该反应的离子方程式
。写出该反应的离子方程式___________ 。
 ):
):
| 金属离子 |  |  | Fe3+ |  |
开始沉淀时(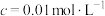 )的pH )的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的pH )的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中NaOH溶液可以有效地除去金属铝及其氧化物,写出NaOH溶液除去铝单质的离子方程式
(2)“滤液②”中含有的金属离子有Fe2+和
(3)利用上述表格数据,计算
 的
的
 浓度为
浓度为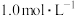 ,则“调pH”应控制的pH范围是
,则“调pH”应控制的pH范围是(4)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的
 。写出该反应的离子方程式
。写出该反应的离子方程式
您最近一年使用:0次
名校
解题方法
6 . 水合硼酸锌(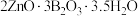 ,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为
,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为 ,以及少量
,以及少量 和
和 等)和菱锌矿(主要成分为
等)和菱锌矿(主要成分为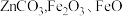 和
和 等)为原料制备水合硼酸锌的工艺流程如下:
等)为原料制备水合硼酸锌的工艺流程如下: 如下表所示:
如下表所示:
回答下列问题:
(1)“酸浸”时, 与硫酸反应的离子方程式为
与硫酸反应的离子方程式为__________ 。为加快“酸浸”时的浸取速率,下列措施中无法达到目的是__________ (填字母)。
a.将样品粉碎 b.延长浸取时间 c.充分搅拌 d.适当增加硫酸浓度 e.适当升高温度
(2)滤渣1的主要成分为__________ (填化学式)。
(3)“氧化”的目的是__________ (语言叙述), 也可以用
也可以用 代替,若“氧化”过程中转移电子数相等,则消耗
代替,若“氧化”过程中转移电子数相等,则消耗 和
和 的物质的量之比为
的物质的量之比为__________ 。
(4)“一次调 ”时,调节溶液的
”时,调节溶液的 ,目的是
,目的是__________ 。“二次调 ”时的
”时的 范围为
范围为__________ 。
(5)“制备”水合硼酸锌的化学方程式为__________ 。
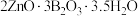 ,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为
,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为 ,以及少量
,以及少量 和
和 等)和菱锌矿(主要成分为
等)和菱锌矿(主要成分为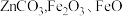 和
和 等)为原料制备水合硼酸锌的工艺流程如下:
等)为原料制备水合硼酸锌的工艺流程如下:
 如下表所示:
如下表所示:金属离子 |
|
|
|
|
|
开始沉淀 | 1.9 | 7.0 | 3.0 | 6.2 | 8.9 |
完全沉淀 | 3.2 | 9.0 | 4.7 | 8.0 | 10.9 |
(1)“酸浸”时,
 与硫酸反应的离子方程式为
与硫酸反应的离子方程式为a.将样品粉碎 b.延长浸取时间 c.充分搅拌 d.适当增加硫酸浓度 e.适当升高温度
(2)滤渣1的主要成分为
(3)“氧化”的目的是
 也可以用
也可以用 代替,若“氧化”过程中转移电子数相等,则消耗
代替,若“氧化”过程中转移电子数相等,则消耗 和
和 的物质的量之比为
的物质的量之比为(4)“一次调
 ”时,调节溶液的
”时,调节溶液的 ,目的是
,目的是 ”时的
”时的 范围为
范围为(5)“制备”水合硼酸锌的化学方程式为
您最近一年使用:0次
2024-04-21更新
|
170次组卷
|
2卷引用:四川省绵阳中学2023-2024学年高三下学期2月开学考理科综合-高中化学
解题方法
7 . 纳米氧化镁广泛应用于电子元器件、催化剂载体等领域,一种利用 制备纳米氧化镁的工艺流程如图所示,下列说法错误的是
制备纳米氧化镁的工艺流程如图所示,下列说法错误的是 不参与化学反应.
不参与化学反应.
 制备纳米氧化镁的工艺流程如图所示,下列说法错误的是
制备纳米氧化镁的工艺流程如图所示,下列说法错误的是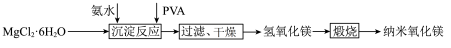
 不参与化学反应.
不参与化学反应.| A.纳米氧化镁分散在空气中能产生丁达尔效应 |
B.“煅烧”时,发生反应的化学方程式为 |
| C.“沉淀反应”时,有共价键的断裂 |
D.可以用坩埚蒸干氯化镁溶液的溶剂获得 |
您最近一年使用:0次
8 . 现有含有 杂质的
杂质的 样品1.95g,某同学在实验室用如图装置(部分夹持仪器已省略)测定其杂质含量:
样品1.95g,某同学在实验室用如图装置(部分夹持仪器已省略)测定其杂质含量:
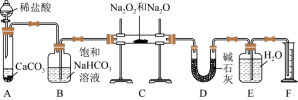
已知:碱石灰主要含有氧化钙和氢氧化钠
回答下列问题:
(1)将仪器连接好后,首先要进行的实验操作是_____ 。
(2)装置B中饱和碳酸氢钠的作用是除去 中HCl气体,该过程涉及的离子反应方程式是
中HCl气体,该过程涉及的离子反应方程式是_____ 。
(3)写出装置C中 和
和 反应的化学方程式:
反应的化学方程式:_____ 。
(4)若无装置D,测得样品中 的质量分数
的质量分数_____ (填“偏高”“偏低”或“无影响”)。
(5)1.95g样品充分反应后,待冷却后读出装置F中水的体积,将其折算成产生气体的质量为0.24g,则样品中 的质量分数为
的质量分数为_____ 。
(6)若除去 粉末中的
粉末中的 ,采用的简单方法为
,采用的简单方法为_____ 。
(7)若将 投入到含有下列离子的溶液中:
投入到含有下列离子的溶液中: 、
、 、
、 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有__________ (填离子符号)。
 杂质的
杂质的 样品1.95g,某同学在实验室用如图装置(部分夹持仪器已省略)测定其杂质含量:
样品1.95g,某同学在实验室用如图装置(部分夹持仪器已省略)测定其杂质含量:
已知:碱石灰主要含有氧化钙和氢氧化钠
回答下列问题:
(1)将仪器连接好后,首先要进行的实验操作是
(2)装置B中饱和碳酸氢钠的作用是除去
 中HCl气体,该过程涉及的离子反应方程式是
中HCl气体,该过程涉及的离子反应方程式是(3)写出装置C中
 和
和 反应的化学方程式:
反应的化学方程式:(4)若无装置D,测得样品中
 的质量分数
的质量分数(5)1.95g样品充分反应后,待冷却后读出装置F中水的体积,将其折算成产生气体的质量为0.24g,则样品中
 的质量分数为
的质量分数为(6)若除去
 粉末中的
粉末中的 ,采用的简单方法为
,采用的简单方法为(7)若将
 投入到含有下列离子的溶液中:
投入到含有下列离子的溶液中: 、
、 、
、 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有
您最近一年使用:0次
2024-04-07更新
|
66次组卷
|
2卷引用:江西省宜春市丰城市第九中学日新班2023-2024学年高二下学期开学考试化学试题
名校
9 . 某含锰废料中主要含 及少量的
及少量的 、
、 、
、 ,以此为原料制备
,以此为原料制备 的流程如下:
的流程如下:

Ⅰ.氢氧化物开始沉淀和完全沉淀的 如下表:
如下表:
Ⅱ.常温下 、
、 。
。
回答下列问题:
(1)写出一种加快酸浸速率的方法______ ,滤渣1的主要成分是______ (填化学式)。
(2)“氧化1”的目的是______ (用离子方程式表示)。
(3)“调 ”时,试剂X为
”时,试剂X为______ (任写一种), 的调节范围为
的调节范围为______ 。
(4)“除铜”时,当溶液中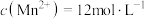 ,溶液中
,溶液中 =
=______  。
。
(5)“氧化2”制备 (恰好完全反应)时,
(恰好完全反应)时,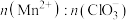 =
=______ 。
 及少量的
及少量的 、
、 、
、 ,以此为原料制备
,以此为原料制备 的流程如下:
的流程如下:
Ⅰ.氢氧化物开始沉淀和完全沉淀的
 如下表:
如下表:氢氧化物 |
|
|
|
|
开始沉淀时 | 8.36 | 6.3 | 2.7 | 4.7 |
完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
 、
、 。
。回答下列问题:
(1)写出一种加快酸浸速率的方法
(2)“氧化1”的目的是
(3)“调
 ”时,试剂X为
”时,试剂X为 的调节范围为
的调节范围为(4)“除铜”时,当溶液中
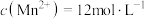 ,溶液中
,溶液中 =
= 。
。(5)“氧化2”制备
 (恰好完全反应)时,
(恰好完全反应)时,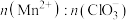 =
=
您最近一年使用:0次
名校
解题方法
10 . 科学家开发的光催化剂BiVO4实现了高选择性制备氢气。某小组以辉铋矿粉(主要成分是Bi2S3,含少量Bi2O3、Bi、FeS2和SiO2等杂质)为原料制备钒酸铋(BiVO4)的流程如图所示。
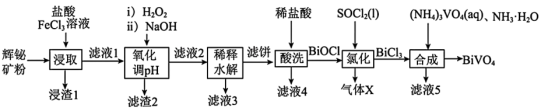
已知部分信息如下:
①滤液1中的主要阳离子有Bi3+、Fe3+、Fe2+和H+。
②常温下,几种离子生成氢氧化物沉淀的pH如表所示。
回答下列问题:
(1)浸取时可以适当加热,但温度不宜过高,其原因是________ 。
(2)浸渣1成分有S和________ ,写出Bi2S3转化的离子方程式:________ 。
(3)加H2O2氧化的目的是________ 。调pH的最低值为________ 。
(4)稀释水解时通入水蒸气的目的是________ 。
(5)将气体X通入酸性KMnO4溶液中,实验现象可能是________ 。
(6)将滤液5经蒸发浓缩、降温结晶、过滤,得到NH4Cl晶体,其晶胞结构如图所示。
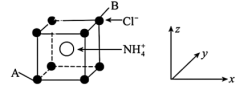
①与氯离子最近且等距离的氯离子有________ 个。
②原子坐标参数表示晶胞内部各原子的相对位置。图中A的坐标参数为 ,B的坐标参数为
,B的坐标参数为 ,则
,则 的坐标参数为
的坐标参数为________ 。

已知部分信息如下:
①滤液1中的主要阳离子有Bi3+、Fe3+、Fe2+和H+。
②常温下,几种离子生成氢氧化物沉淀的pH如表所示。
氢氧化物 |
|
|
|
开始沉淀的pH | 7.6 | 1.6 | 4.0 |
完全沉淀的pH | 9.6 | 3.1 | 5.5 |
(1)浸取时可以适当加热,但温度不宜过高,其原因是
(2)浸渣1成分有S和
(3)加H2O2氧化的目的是
(4)稀释水解时通入水蒸气的目的是
(5)将气体X通入酸性KMnO4溶液中,实验现象可能是
(6)将滤液5经蒸发浓缩、降温结晶、过滤,得到NH4Cl晶体,其晶胞结构如图所示。

①与氯离子最近且等距离的氯离子有
②原子坐标参数表示晶胞内部各原子的相对位置。图中A的坐标参数为
 ,B的坐标参数为
,B的坐标参数为 ,则
,则 的坐标参数为
的坐标参数为
您最近一年使用:0次















